
HOME 研究代表者・研究課題 平成25年度採択 浜地格

生細胞有機化学を基軸とした
タンパク質その場解析のための分子技術
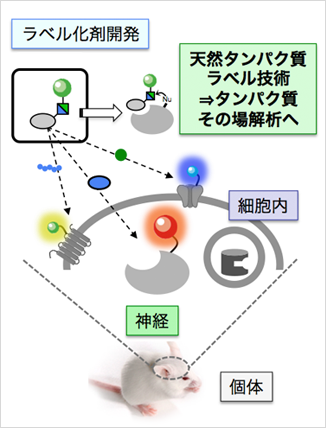
本研究では、生命現象の中心を担うタンパク質およびそれと相互作用する小分子の機能・動的特性を、試験管のような人工的な環境ではなく、それらが働く生体内でそのまま解析・評価することを可能とする生細胞有機化学とも呼べる分子技術の創成を目指します。これは、分子イメージングによる精密で迅速な疾病診断技術、副作用の要因ともなるoff target解析を含む創薬の開発プロセスの精密・効率化を分子レベルで加速する基盤技術になると期待されます。
- 世界初、生きた細胞系で内在性タンパク質を選択的かつ機能を保持したまま修飾する化学の創製
- 脳神経疾患等の精密かつ迅速な疾病診断技術、薬剤のoff target解析を含む創薬開発の精密化・効率化に化学で貢献
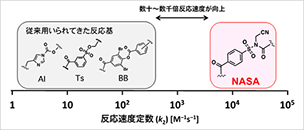
LDNASA化学によるタンパク質
ラベリング速度の飛躍的な改善
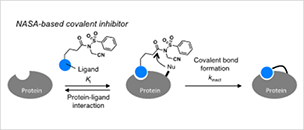
LDNASA化学によるタンパク質の不可逆阻害
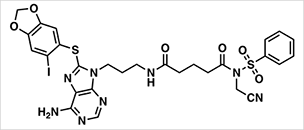
世界初となるHsp90不可逆阻害剤の分子構造
これまでの研究成果(インパクト)
- 我々が開発したリガンド指向性N-acyl-N-alkylsulfonamide化学(LDNASA化学)を用いることで、生細胞内の狙った天然タンパク質を高速かつ高選択的に化学修飾することに成功した。
- 本手法では、従来法より数十倍から数千倍以上速くラベル化反応が進行し、タンパク質表面のリジン残基を選択的に修飾できた 。また、リガンド指向性化学におけるリガンドの親和性と反応特性(反応速度、反応選択性)の関係を初めて明らかにした。
- さらに本手法を応用することで、癌の創薬ターゲットである熱ショックタンパク質90 (Hsp90)の不可逆阻害剤開発に世界で初めて成功した。
今後の進め方
- 本技術の他のタンパク質不可逆阻害剤への拡張
- 組織や生体個体などより夾雑な生体環境への適用
- より不活性なアミノ酸とも反応可能な反応基の開発
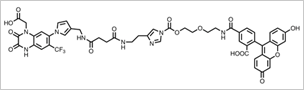
AMPA受容体のケミカルラベルに用いる
LDAI型ラベル化剤CAM2(Fl)の構造

海馬培養神経細胞での
native AMPA受容体のラベル化・可視化
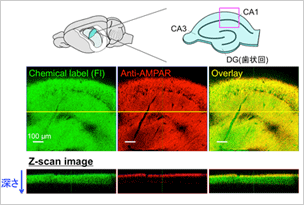
海馬スライス切片での
native AMPA受容体のラベル化・可視化
これまでの研究成果(インパクト)
- 我々が開発したリガンド指向性アシルイミダゾール化学(LDAI化学)を用いることで、培養神経細胞および脳組織において、内在的に発現するAMPA型グルタミン酸受容体を選択的にケミカルラベル化することに成功した。
- 本手法では受容体機能を維持したままでラベル化できるので、神経細胞および脳組織におけるAMPA型グルタミン酸受容体の動態解析が可能となった。
- 我々のラベル化により、内在的に発現するAMPA受容体の動態は広く用いられる蛍光タンパク質を融合した受容体の動態と大きく異なることを明らかにした。
今後の進め方
- 本技術の他のグルタミン酸受容体への拡張
- 記憶・学習時におけるAMPA型グルタミン酸受容体動態変化の可視化
- より迅速なグルタミン酸受容体のケミカルラベル
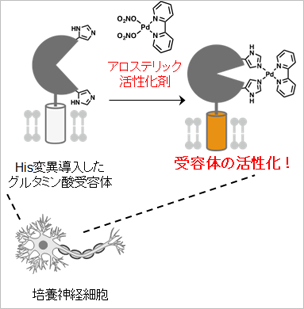
細胞表層配位化学(OcCC)によるグルタミン酸受容体の活性化
これまでの研究成果(インパクト)
- 興奮性神経伝達物質受容体であるグルタミン酸受容体を人工的に活性化できる分子技術として、遺伝子工学と錯体化学を組み合わせた細胞表層配位化学(On-cell Coordination Chemistry, OcCC)を開発した。
- 金属配位性アミノ酸残基であるヒスチジン(His)を部位特異的に変異導入した標的グルタミン酸受容体に対して、Pd(bpy)錯体を作用させることで、受容体の活性化構造を人為的に惹起させる手法を実現した。
- 培養神経細胞において、His変異導入を行ったグルタミン酸受容体のみを選択的に活性化することに成功した。
今後の進め方
- 本分子技術の他の受容体への拡張
- 脳組織や動物個体におけるグルタミン酸受容体の選択的活性化
- 記憶や学習に関与する脳機能の解明
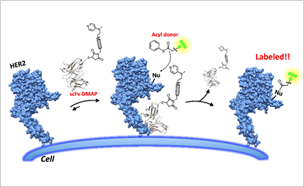
触媒連結抗体による細胞表層受容体のラベル化
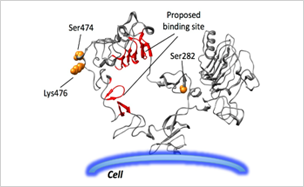
修飾部位解析から推定された
抗原ー抗体相互作用部位(赤色部分)
これまでの研究成果(インパクト)
- 有機合成において汎用されるDMAP(4-Dimethylamino pyridine)触媒を低分子量抗体に繋げた「触媒連結抗体」を作製した。
- 触媒連結抗体を用いて生細胞表層の受容体タンパク質を化学修飾する分子技術の開発に成功した。
- この手法を用いて、腫瘍のバイオマーカーとして知られる受容体(HER2, EGFR)の生細胞イメージングと寿命解析を実現した。
- この手法に質量分析法を組み合わせると、これまで未知であった抗原ー抗体間の相互作用部位(エピトープ)を同定することが可能となった。
今後の進め方
- 触媒連結抗体のライブラリー化による標的受容体の拡張
- 本手法に適用可能な有機触媒分子の探索・開発
- 脳や組織スライスにおける受容体の特異的ラベル
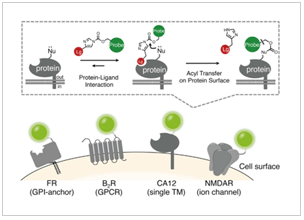
LDAI化学による細胞膜タンパク質ラベル化
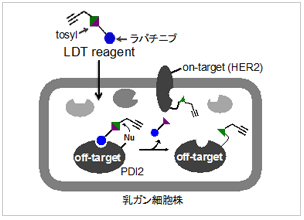
LDT化学による薬剤オフターゲット同定
これまでの研究成果(インパクト)
- 我々が独自に開発したタンパク質ラベル化法である「リガンド指向性アシルイミダゾール(LDAI)化学」が様々なタイプの膜タンパク質に適用可能であることを実証した。特に、記憶・学習に重要な役割を担うAMPA受容体については、小脳あるいは大脳皮質から単離した神経細胞においても特異的にラベル・可視化解析可能であることを確認した。
- フェニルスルホン酸エステルを反応基としたタンパク質ラベル化法である「リガンド指向性トシル(LDT)化学」を応用して、抗がん剤ラパチニブの副作用の原因となりうるオフターゲットの同定に成功した。
今後の進め方
- 小分子リガンドを有さないタンパク質標的に対するラベル化法の開発
- LDAI化学によるAMPA受容体のラベル化法を用いた、神経細胞内在性AMPA受容体の動態解析への展開
- 脳スライスにおけるAMPA受容体の特異的ラベル化の評価
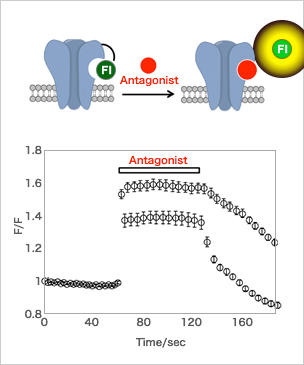
ラベル化AMPA受容体の
リガンド添加に伴う蛍光応答
これまでの研究成果(インパクト)
- 研究基盤となる「リガンド指向性化学」における新規反応部位として、新しい官能基(SP)を組み込んだラベル化剤を開発した。ターゲットタンパク質としては、我々が予備的な知見を豊富に持っている、ヒト由来炭酸脱水酵素(hCA)等を対象として、これらに対応するラベル化剤を設計および合成し、リガンド指向に基づく選択的なラベル化を検証した。その結果、我々がこれまでに有効性が実証している反応基(トシル基、アシルイミダゾール基)に比べて、SPを組み込んだラベル化剤の反応性が高いことを確認した。
- 脳神経系において、シナプス可塑性に重要な働きを示すAMPA型グルタミン酸受容体(AMPA受容体)を標的としてた蛍光ラベル化法の開発を行った。我々が開発した細胞表層タンパク質ラベル化法であるLDAI化学を用いた結果、HEK293T細胞に過剰発現させたAMPA受容体を選択的に蛍光ラベル化できることを確認した。興味深いことに、リガンド添加に伴い、AMPA受容体にラベル化された蛍光団の蛍光強度が変化し、生細胞上においてリガンドの結合を蛍光の変化として検出することが可能となった。
今後の進め方
- 新規リガンド指向型化学(LDSP化学)の細胞内タンパク質ラベル化への展開
- 神経細胞内在性AMPA受容体のケミカルラベル化およびAMPA受容体生理機能解明への応用
- 他の神経伝達物質受容体のケミカルラベル化
