
HOME 研究代表者・研究課題 平成25年度採択 山東信介

超高感度化分子技術により実現する
巨視的ケミカルバイオロジー
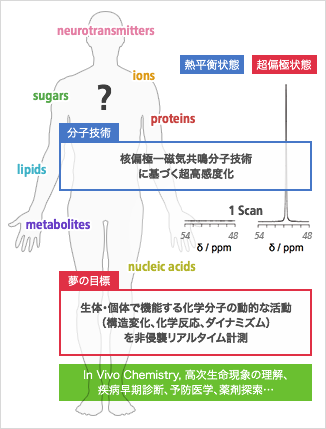
当然の事でありながら忘れがちですが、私たちの体は分子の集まりです。体の中の分子の秩序だった活動は、生物が生命を維持する未解明の仕組みであり、その異常は代謝疾患や精神疾患など様々な病気の原因となります。本研究では、今まで見る事のできなかった、体の中の分子の構造変化、化学反応、ダイナミズムなどの活動を、体を傷つけずに計測できる超高感度分子センシング技術を世界に先駆けて構築します。分子の活動にもとづく「新しい次元での生命の理解」や「疾病超早期診断」など未来サイエンス、未来医療に応用できる革新的分子技術の創製を目指します。
- 分子の核スピン物性を制御する基盤分子技術
- 核偏極ー磁気共鳴分子技術に基づく高感度生体分子解析
- 生体・個体で機能する分子の動的な活動を非侵襲リアルタイム計測
- 高感度生体分子計測に基づく「Science:In Vivo 分子工学」、「Technology:早期予防医学」に繋がる次世代分子技術
- 化学、物理、生物・医学分野を貫通する融合研究
- 山東 信介
- 東京大学
大学院工学系研究科
教授 研究室HP
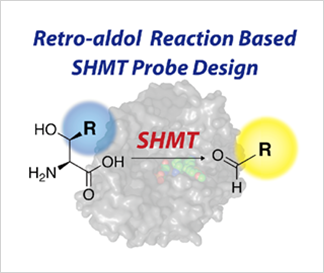
図1
これまでの研究成果(インパクト)
-
生体応用可能な長寿命核偏極分子構造の探索
核偏極状態を極めて長時間維持し、生体適合性のある水溶性15N-分子プローブを用い、動物個体内における分子イメージング(画像化)に成功した。腫瘍モデルマウスを用い、腫瘍環境における高感度計測が可能であることを実証した。また、生体微小環境計測への応用研究を実施した。(未発表のため、図は省略) - SHMT活性を検出する高感度分子プローブ(図1)
セリンヒドロキシメチルトランスフェラーゼ(SHMT)は、セリンーグリシン代謝に関連する酵素であり、抗がん剤や抗マラリア剤の創薬標的として、注目を集めている。SHMTの非標準的な酵素反応機構に着目し分子設計を行うことで、高感度なSHMT検出が可能な蛍光分子プローブを開発した。新たな阻害剤候補化合物の探索に成功した。
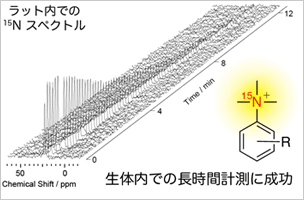
図1
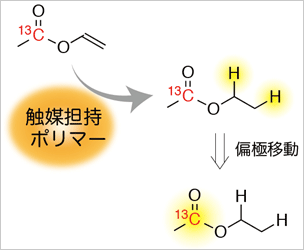
図2
これまでの研究成果(インパクト)
-
生体応用可能な長寿命核偏極分子構造の探索(図1)
毒性が低く、かつ生体条件でも核偏極状態を長時間維持できる水溶性15N核偏極分子構造を用い、実際のVivo条件においても核偏極15N NMRシグナルが計測できることを実証した。核偏極生体イメージングに向けた極めて重要な一歩である。 - 高感度磁気共鳴分子センサーの開発
現在までに開発した疾患関連生体酵素アミノペプチダーゼN、γグルタミルトランスペプチダーゼに応答する13C-核偏極分子センサーを用い、生体での更なる実証実験を進めた。実際に、疾患モデルにおいて、核偏極分子プローブが代謝反応を受け、新たなシグナルが生成することが確認された。 - パラ水素誘導核偏極法の開拓(図2)
有機金属触媒とパラ水素を用いた核偏極法開拓に着手している。実応用に向け不均一触媒系の開発を行った。有機金属触媒を担持したポリマーを用い、標的分子の核偏極を実現した。
今後の進め方
- 長寿命核偏極分子構造の生体応用を進め、評価を行う。
- 高感度磁気共鳴分子センサーの疾患モデルへの応用展開、定量的評価を更に進め、実証に向けた検討を実施する。
- 効率的PHIPに向けた有機金属触媒の開拓を進める。特に、連続生成が可能なフロー反応系、固体触媒系の構築に挑戦する。
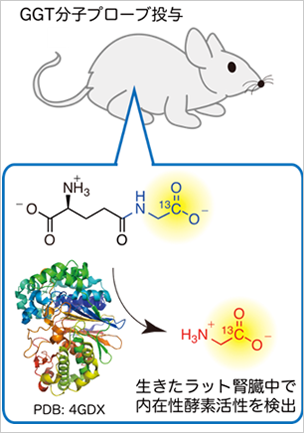
図1
これまでの研究成果(インパクト)
-
生体応用可能な長寿命核偏極分子構造の探索
長寿命核偏極を実現する分子構造の生体応用に向け、種々の誘導体合成、及びそれらの物性評価を行なった。その結果、毒性を低減させた水溶性長寿命核偏極分子構造の開発を実現した。 - 高感度磁気共鳴分子センサーの開発(図1)
腫瘍増殖、腎機能への関連が示唆される重要な生体酵素γグルタミルトランスペプチダーゼ(GGT)を標的とする核偏極分子センサーを用い、実際に生物個体における腎臓GGT活性の計測・イメージングに成功した。 - パラ水素誘導核偏極法の開拓
パラ水素誘導核偏極実験系を確立するとともに、構造活性相関による金属錯体の最適化を実施した。
今後の進め方
- 長寿命核偏極分子構造の生体応用を進め、その結果から課題抽出、更なる分子開発を行う。
- 高感度磁気共鳴分子センサーの疾患モデルへの応用展開を進め、その評価を行う。
- 簡便・簡易なパラ水素誘導法により偏極可能な分子レパートリーの拡張を進める。
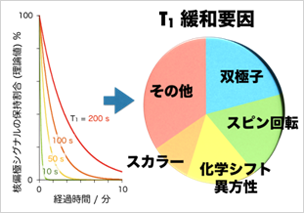
図1
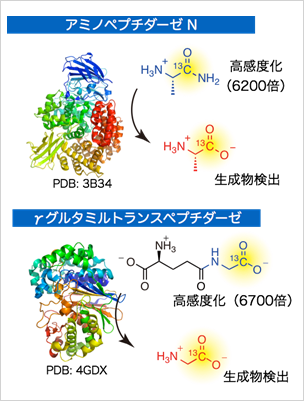
図2
これまでの研究成果(インパクト)
-
長寿命核偏極を実現する分子構造の論理的解釈(図1)
核偏極緩和メカニズムに着目し、各緩和要因の評価法の検討を進めた。その結果、各々の分子構造において偏極緩和を支配する要因を詳細に解析することができるようになった。この成果は、「長寿命核偏極を実現する分子構造の論理的設計」に向けた重要なステップである。 -
高感度磁気共鳴分子センサーの開発(図2)
アミノ酸を用いた高感度NMR分子センサーの開発を進めた。昨年度までに設計した(1)腫瘍増殖、(2)腎機能計測に向けたペプチダーゼ分子センサーが、疑似生体環境でも機能することを確認し、標的酵素活性の高感度リアルタイム計測が可能であることを示した。
今後の進め方
- 核偏極緩和の論理的解釈をもとに、生体応用可能な長寿命核偏極分子構造を探索する。
- 動物個体への応用展開を進め、分子センサーの応用可能性を評価、課題を抽出する。
- パラ水素誘導偏極法をもちいた、より簡便、安価な核偏極システムの構築。
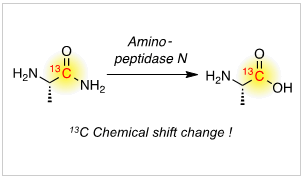
図1:高感度磁気共鳴分子センサーの一例
(アミノペプチダーゼNに対する分子プローブ)
これまでの研究成果(インパクト)
- 長寿命核偏極を実現する分子プラットフォームの提案
核緩和メカニズムをもとに、長寿命核偏極を実現する分子プラットフォームを提案。13C核、15N核それぞれにおいて、核偏極状態維持の目安となる縦緩和時間T1が100秒(9.4 T, MeOD, 25℃)、1,000秒(14.1 T, D2O, 30℃)を超える分子骨格を実現した。本結果は高感度磁気共鳴分子センサー開発の基礎となる重要な成果である。 - 高感度磁気共鳴分子センサーの開発(図1)
分子プラットフォームをもとに、種々の生体分子を標的とする高感度磁気共鳴センサーの開発を進めた。核偏極(高感度化)状態における生体分子センシング機能の評価を実施した。 - 評価系の構築
細胞スフェロイド(細胞塊)を用いた擬似生体評価系など、分子プローブの性能評価に向けたアッセイ系を構築した。
今後の進め方
- シンプルかつ実用性の高い長寿命核偏極分子プラットフォームを探索するとともに、分子設計指針を確立する。
- 高感度磁気共鳴分子センサーの詳細な物性・機能評価を実施する。
- 応用に向け、より簡便な核偏極技術の開拓を進める。

図1
これまでの研究成果(インパクト)
-
長寿命核偏極を実現する分子構造の探索
核偏極状態の緩和には種々の相互作用が寄与することが知られている(図1)。磁気双極子相互作用、及び、スピン回転相互作用を抑制した分子を設計・合成し、13C、15N核それぞれにおいて、核偏極状態をより長時間維持できる分子構造候補の探索に成功した。 -
応用に向けた機器開発
高感度化に必要な核偏極装置など、実験・評価系を立ち上げた。培養細胞を用いた計測に向け、細胞を高密度・3次元的に積層化させたセルカプセルビーズの構築に成功した。また、迅速な分子プローブ投与に向けた液泡分離装置、1.5T MRI装置用13C共振器を試作した。
今後の進め方
- 高感度化状態(偏極状態)を、より長時間維持できる分子構造の探索を引き続き行なう。また、見出した分子構造をもとに、生命現象解明・疾病早期診断を実現する超高感度磁気共鳴分子プローブを設計し、より生体に近い系での性能を評価する。
- セルカプセルビーズなど細胞実験・評価系を確立する。
- 応用に向けて試作した機器・装置の性能を評価し、実応用に向けた改良点、開発ポイントを明らかにする。
