拠点事業紹介
iPS拠点事業
研究課題名
京都大学iPS 細胞研究統合推進拠点
実施体制
研究代表者
| 山中 伸弥 | (京都大学 iPS細胞研究所/京都大学 物質-細胞統合システム拠点 教授) |
分担代表研究者
| 中尾 一和 | (京都大学 大学院医学研究科 教授) |
| 長船 健二 | (京都大学 iPS細胞研究所 准教授) |
| 中川 隆之 | (京都大学 大学院医学研究科 講師) |
| 井上 治久 | (京都大学 iPS細胞研究所 准教授) |
| 櫻井 英俊 | (京都大学 iPS細胞研究所 特定拠点講師) |
| 山下 潤 | (京都大学 再生医科学研究所/iPS細胞研究所 准教授) |
| 戸口田 淳也 | (京都大学 再生医科学研究所/iPS細胞研究所 教授) |
| 中畑 龍俊 | (京都大学 iPS細胞研究所 特定拠点教授) |
| 高須 直子 | (京都大学 iPS細胞研究所 知財契約管理室 室長) |
| 浅香 勲 | (京都大学 iPS細胞研究所 特定准教授) |
| 高橋 淳 | (京都大学 再生医科学研究所/iPS細胞研究所 准教授) ※平成23年11月11日より再生医療の実現化ハイウェイに移行 |
| 澤 芳樹 | (大阪大学 大学院医学系研究科 教授) ※平成23年度より再生医療の実現化ハイウェイに移行 |
最新の研究成果・進捗状況
再生医療に応用できるiPS細胞樹立技術の開発
iPS細胞技術を臨床応用水準にまで高めることを目標に、樹立技術の確立に向け研究を進め、これまでに以下の成果を得ている。・自家フィーダー細胞上でのヒトiPS細胞樹立・培養技術の開発
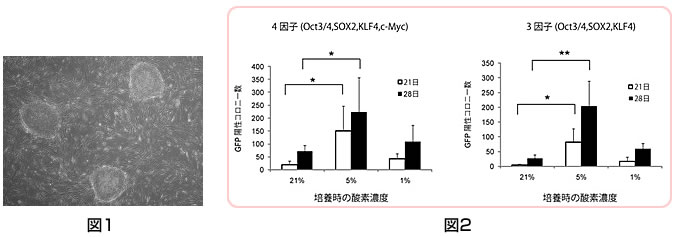
新生児または成人から提供された皮膚線維芽細胞を自己フィーダー細胞として用いてヒトiPS細胞を樹立し、培養できることを見出した。作製されたiPS細胞は正常な核型を示し、分化多能性があることも確認した。(Takahashi, et al., PLoS ONE, 2009)
(図1)皮膚細胞がiPS細胞のソースとしてのみならず、iPS細胞を支持するフィーダー細胞としても有用であることを示した。ES細胞は初期胚から樹立するため、マウスもしくは他人由来のフィーダー細胞上で培養する必要があるが、自己の細胞をフィーダー細胞として用いる技術はこの点を克服し、動物成分や他人由来の感染源のリスクを低減させるのに役立つと考えられる。
(図1)皮膚細胞がiPS細胞のソースとしてのみならず、iPS細胞を支持するフィーダー細胞としても有用であることを示した。ES細胞は初期胚から樹立するため、マウスもしくは他人由来のフィーダー細胞上で培養する必要があるが、自己の細胞をフィーダー細胞として用いる技術はこの点を克服し、動物成分や他人由来の感染源のリスクを低減させるのに役立つと考えられる。
・低酸素環境がiPS細胞樹立を促進
5%の低酸素濃度で培養することで、従来の条件に比べ有意にiPS細胞樹立効率が改善することを見出した。レトロウイルスベクター、プラスミドおよびピギーバックベクター等、いずれの方法でのiPS細胞誘導においても同様の効果が見られた。(Yoshida, et al., Cell Stem Cell., 2009)
(図2)低酸素培養によるマウス線維芽細胞のiPS細胞樹立効率の改善(左:4因子(Oct3/4,Sox2,Klf4,c-Myc)導入、右:c-Mycを除く3因子導入)
(図2)低酸素培養によるマウス線維芽細胞のiPS細胞樹立効率の改善(左:4因子(Oct3/4,Sox2,Klf4,c-Myc)導入、右:c-Mycを除く3因子導入)
・遺伝子挿入のないヒトiPS細胞の効率的で簡便な樹立法の開発
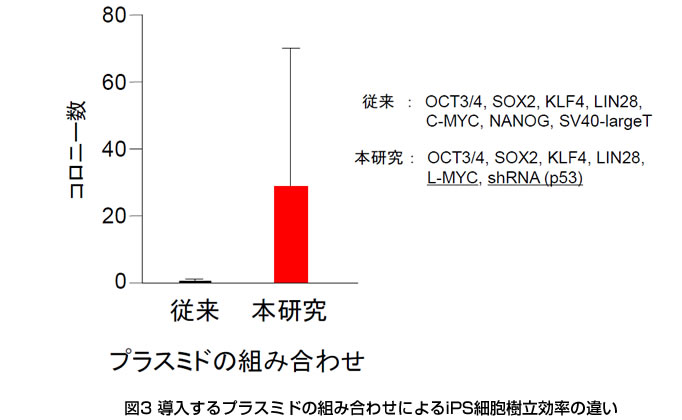
プラスミドを遺伝子導入ベクターとして用いて、ヒト線維芽細胞から効率よくiPS細胞を樹立する方法を開発した。さらに計算上、日本人の約20%への移植適合性を持つHLA3座ホモの歯髄細胞2株から、外来遺伝子の挿入のないiPS細胞の樹立にも成功した。(Okita, et al., Nature Methods, 2011)
・転写因子Glis1により安全なiPS細胞の高効率作製に成功
プcDNAライブラリーを用いたスクリーニングによりiPS細胞の樹立におけるKlf4の代替因子として、卵細胞で強く発現する転写因子Glis1を同定した。この因子を従来の4因子とともに用いると、非常に効率よくマウスおよびヒトiPS細胞を誘導できることを発見した。
iPS細胞からの各種細胞の分化誘導技術開発、および治療技術開発
造血幹細胞や骨格筋、神経細胞、脂肪細胞、肝細胞など、様々な細胞への分化誘導方法の開発を継続して進めている。また、疾患特異的iPS細胞の樹立を進めるなかで、筋ジストロフィーやパーキンソン病などの細胞治療法開発を進めている。・ドーパミン神経前駆細胞の分化とサルモデルでの脳内への生着を検証
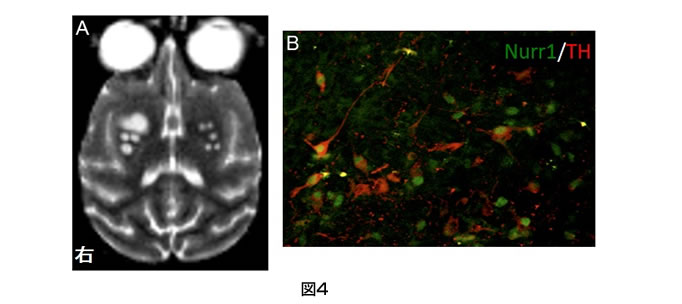
ヒトのiPS細胞からフィーダー細胞を使わず浮遊培養のみでドーパミン神経前駆細胞を誘導することに成功した。さらに、この細胞をパーキンソン病モデルのカニクイザルの脳内に移植し、MRI、PET、免疫組織学的手法を用いてドーパミン神経細胞が6ヶ月間生着することを確認した。(Kikuchi, et al., J. of Parkinson Disease, 2011)
(図4)ヒトiPS細胞から誘導したドーパミン神経細胞がカニクイザルパーキンソン病モデル脳に生着した。A) 6か月後のMRI画像。(右脳には未成熟、左脳には成熟した神経細胞を移植)B) 脳切片の免疫染色。赤はドーパミン神経細胞のマーカー、緑は特に中脳ドーパミン神経細胞のマーカーを示す。
(図4)ヒトiPS細胞から誘導したドーパミン神経細胞がカニクイザルパーキンソン病モデル脳に生着した。A) 6か月後のMRI画像。(右脳には未成熟、左脳には成熟した神経細胞を移植)B) 脳切片の免疫染色。赤はドーパミン神経細胞のマーカー、緑は特に中脳ドーパミン神経細胞のマーカーを示す。
臨床応用に向けた取り組み
GMPに準拠したヒトiPS細胞を調製するための細胞調製施設(FiT)において、品質管理システムの構築を図りつつ、本格的な稼働に向けた準備を進めている。
iPS細胞誘導の技術普及、および研究材料提供
国内外の大学や企業の研究者などを対象としたiPS樹立・維持培養講習会と実技トレーニングを継続して進めると共に、積極的にプロトコールや細胞等の研究材料を発信・提供するなど、技術の普及に向けた取り組みを更に強化した。・プラスミドベクターを用いたマウス人工多能性幹細胞の樹立方法
非ウイルスベクターであるプラスミドを用いたマウスiPS細胞の樹立方法について、使用する試薬やその調製方法、実験手順、作業上の注意点などを記載した詳細なプロトコールを公開した。(Okita, et al., Nature Protocol, 2010)

今年度の展望・最終目標等
① iPS細胞に関する標準化
② 生活習慣病とその合併症を標的とするヒトiPS細胞を用いた再生医療に向けた技術開発
③ iPS細胞を用いた内耳再生医療の開発
④ ヒトiPS細胞を用いた神経再生医療実現化のための技術開発
⑤ 難治性筋疾患に対する細胞移植治療の開発
⑥ iPS細胞を用いた心血管分化機構の解明と創薬・細胞治療による心血管再生治療法の開発
⑦ 前臨床研究および臨床研究の総合的推進
⑧ 疾患特異的iPS細胞の樹立・提供
⑨ 国際競争を見据えた知的財産戦略
⑩ 細胞誘導の技術講習会・培養トレーニングプログラムの実施
⑪ HLAホモ接合体iPS細胞を用いた神経前駆細胞移植による脊髄損傷治療の前臨床研究
② 生活習慣病とその合併症を標的とするヒトiPS細胞を用いた再生医療に向けた技術開発
③ iPS細胞を用いた内耳再生医療の開発
④ ヒトiPS細胞を用いた神経再生医療実現化のための技術開発
⑤ 難治性筋疾患に対する細胞移植治療の開発
⑥ iPS細胞を用いた心血管分化機構の解明と創薬・細胞治療による心血管再生治療法の開発
⑦ 前臨床研究および臨床研究の総合的推進
⑧ 疾患特異的iPS細胞の樹立・提供
⑨ 国際競争を見据えた知的財産戦略
⑩ 細胞誘導の技術講習会・培養トレーニングプログラムの実施
⑪ HLAホモ接合体iPS細胞を用いた神経前駆細胞移植による脊髄損傷治療の前臨床研究
リンク情報
京都大学iPS細胞研究所(CiRA)
http://www.cira.kyoto-u.ac.jp●
http://www.cira.kyoto-u.ac.jp●
文部科学省 iPS細胞等研究ネットワーク iPS Trend
http://www.jst.go.jp/ips-trend/●
http://www.jst.go.jp/ips-trend/●

