拠点事業紹介
iPS拠点事業
研究課題名
京都大学iPS 細胞研究統合推進拠点
実施体制
研究代表者
| 山中 伸弥 | (京都大学 iPS細胞研究所/物質-細胞統合システム拠点 教授) |
分担代表研究者
| 中畑 龍俊 | (京都大学 iPS細胞研究所 特定拠点教授) |
| 戸口田 淳也 | (京都大学 iPS細胞研究所/再生医科学研究所 教授) |
| 林 秀也 | (京都大学 iPS細胞研究所 特定拠点教授) |
| 浅香 勲 | (京都大学 iPS細胞研究所 特定准教授) |
| 井上 治久 | (京都大学 iPS細胞研究所 准教授) |
| 長船 健二 | (京都大学 iPS細胞研究所 准教授) |
| 高橋 淳 | (京都大学 iPS細胞研究所/再生医科学研究所 准教授) |
| 山下 潤 | (京都大学 iPS細胞研究所/再生医科学研究所 准教授) |
| 櫻井 英俊 | (京都大学 iPS細胞研究所 特定拠点講師) |
| 伊藤 壽一 | (京都大学 大学院医学研究科 教授) |
| 中尾 一和 | (京都大学 大学院医学研究科 教授) |
| 瀬原 淳子 | (京都大学 再生医科学研究所 教授) |
| 上杉 志成 | (京都大学 物質-細胞統合システム拠点 教授) |
| 加藤 和人 | (京都大学 人文科学研究所 准教授) |
| 澤 芳樹 | (大阪大学 大学院医学系研究科 教授) |
研究成果・進捗
再生医療に応用できるiPS細胞樹立技術の開発
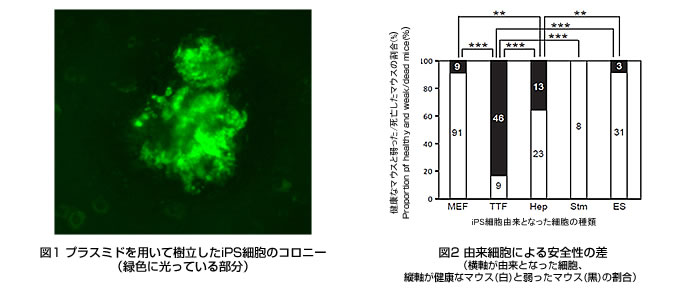
当初iPS細胞技術が開発された際は腫瘍化など様々な問題が指摘されていたが、この3カ年度の成果により、iPS細胞を臨床応用水準の技術とする基礎が整いつつある。| ・ | ウィルスを用いないマウスiPS細胞の樹立法開発に成功 ゲノムへの挿入による腫瘍形成が危惧されていたレトロウィルスベクターに代わり、プラスミドを用いた因子の導入によるマウスiPS細胞の樹立に成功した。今後、iPS細胞応用に向けて安全性の向上につながると期待される。(Okita, et al., Science, 2008) (図1) |
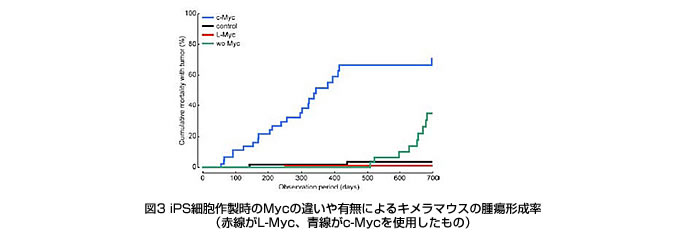
| ・ | 移植安全性におけるiPS細胞の樹立に用いる体細胞の由来の重要性を指摘 皮膚や肝臓など、様々な細胞からiPS細胞を作成しマウスに移植したところ、その安全性は導入因子や樹立方法よりも、由来となる細胞が大きく影響することを示した。(Miura et al., Nat. Biotech., 2009) (図2) |
| ・ | がん抑制遺伝子p53によるiPS細胞の樹立抑制メカニズム解明 p53遺伝子の発現を抑制することで、樹立効率が高まることを示した。また、p53-p21 経路が細胞のがん化抑制のみならず、iPS 細胞樹立においても抑制弁として機能していることを見出した。(Hong, et al. Nature, 2009) |
| ・ | iPS細胞作製に必要な因子の中で、c-Mycは、樹立効率の促進に寄与する一方で、腫瘍形成に働くことが問題とされていた。そこで、c-Mycの代わりにMycファミリーの一つであるL-Mycを用いることで、より高効率にiPS細胞を誘導し、腫瘍原性も低くすることに成功した。iPS細胞技術を臨床応用に用いる際、L-Mycが有用だと考えられる。(Nakagawa, et al. PNAS, 2010.) (図3) |
iPS細胞からの各種細胞の分化誘導技術開発、および治療技術開発
造血幹細胞や骨格筋、神経細胞、脂肪細胞、肝細胞など、様々な細胞への分化誘導方法を開発している。疾患特異的iPS細胞の樹立も進めており、病因解明や創薬応用に結び付けていく他、筋ジストロフィーやパーキンソン病などの細胞治療法開発にも取り組んでいる。
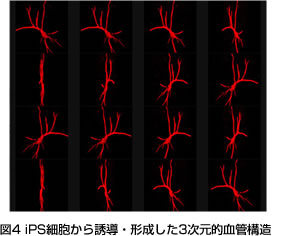
| ・ | マウスiPS細胞からの心血管分化に成功 マウスES細胞を用いて構築した系統的心血管細胞分化誘導法をマウスiPS細胞に適用することにより、マウスiPS細胞を種々の心血管細胞に誘導させること、および血管構造を培養下で形成させることに成功した。(Narazaki, G. et al. Circulation 2008) (図4) |
臨床応用に向けた取り組み
GMPに準拠したヒトiPS細胞を調製するための品質管理システムの検討を行う他、iPS細胞研究所の新棟に細胞調製施設(CPC)を設置。体制強化をはかっている。(図5)iPS細胞誘導の技術普及、および研究材料提供
大学や企業の研究者などを対象にiPS樹立・維持培養講習会と実技トレーニングを実施。webサイトを通じてプロトコールや細胞等の研究材料を発信・提供するなど、技術の普及に向けた取り組みを行っている。(図6)
今後の計画
これまで得られた成果を元に、ヒトiPS細胞技術を更に発展させ臨床応用へ結び付けるため、以下の事項に取り組んでいく。
1. iPS細胞の標準化2. iPS細胞樹立を誘導する低分子化合物の同定
3. 5疾患群に対する再生医療の技術開発
4. 前臨床試験、臨床試験推進
5. 知的財産戦略の構築
6. 倫理的、社会的課題への取り組み
7. iPS細胞技術の指導・普及
8. 疾患iPS細胞の樹立・提供
リンク情報
京都大学iPS細胞研究所(CiRA)
http://www.cira.kyoto-u.ac.jp●
http://www.cira.kyoto-u.ac.jp●
文部科学省 iPS細胞等研究ネットワーク iPS Trend
http://www.jst.go.jp/ips-trend/●
http://www.jst.go.jp/ips-trend/●
