個別事業紹介
幹細胞治療開発領域
研究課題名
脳室周囲白質軟化症の幹細胞治療の実現化
実施体制
研究代表者
| 澤本 和延 | (公立大学法人名古屋市立大学 大学院医学研究科 教授) |
研究成果・進捗(今後の計画)
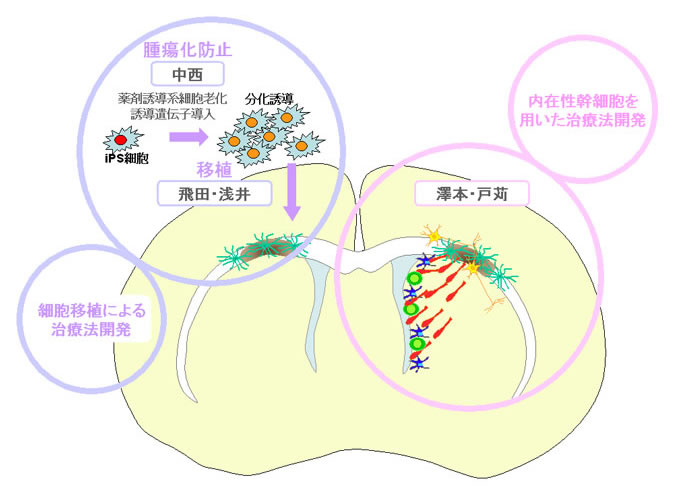
脳疾患はiPS細胞による再生医療の対象としては最も実現が困難なものの一つと考えられる。本課題では、脳室周囲白質軟化症(PVL)を対象として細胞移植による再生医療の可能性を検討するとともに、薬剤投与による再生誘導の技術の開発に取り組んでいる。これらを組み合わせることにより、研究期間終了時までに確実に再生医療の実現化に近づくとともに、脳疾患の再生医療研究が進むべき方向性を示すことができると考えている。
(1)内在性神経幹細胞によるPVL治療法の開発
これまで代表研究者(澤本)らが研究してきた脳室下帯幹細胞による再生機構(Yamashita et al., J Neurosci., 2006など)や脳室下帯で産生された細胞の移動能力(Sawamoto et al., Science, 2006など)に着目し、傷害を受けた脳組織を再生させる方法の開発を試みている。これまでに、PVLモデルマウスを作成し、脳の傷害部における各種細胞の脱落・増殖とその経時的変化、傷害後の脳室下帯における細胞産生・移動とニューロン・オリゴデンドロサイトへの分化の特徴を解析した。(図1)
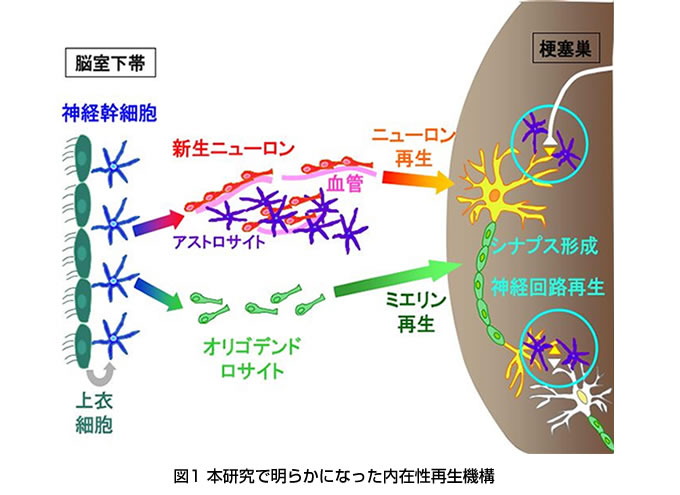 脳内におけるニューロンの移動の新しいメカニズムとして、新生ニューロンが産生する分泌性蛋白質Slit1が、脳内に存在するアストロサイトに作用し、ニューロンの移動に必要な経路を形成させることを明らかにした(Kaneko et al., Neuron, 2010)。さらに、傷害部位へ移動する細胞を蛍光標識して脳スライスを作成し、培養下で観察したところ、これらの細胞が血管を足場にして移動することが明らかになった(Kojima et al., Stem Cells, 2010)。
脳内におけるニューロンの移動の新しいメカニズムとして、新生ニューロンが産生する分泌性蛋白質Slit1が、脳内に存在するアストロサイトに作用し、ニューロンの移動に必要な経路を形成させることを明らかにした(Kaneko et al., Neuron, 2010)。さらに、傷害部位へ移動する細胞を蛍光標識して脳スライスを作成し、培養下で観察したところ、これらの細胞が血管を足場にして移動することが明らかになった(Kojima et al., Stem Cells, 2010)。さらに、低分子化合物ライブラリーの中から、脳室下帯細胞の移動に影響を及ぼす薬剤を探索し候補分子を得た。
コモンマーモセット新生仔および成体の脳室下帯がヒトに類似した構造を有することを明らかにした。慶應義塾大学・実験動物中央研究所と共同でマーモセット脳虚血モデルを作成し、細胞の再生について解析した。
今後は、これらのメカニズムを薬剤を用いて活性化し、再生を誘導する方法の確立を目指す。これらの技術は、細胞移植による治療の効率を高めるためにも役立つ可能性がある。
(2)iPS細胞由来神経系細胞の移植によるPVL治療法の開発
PVLにおいて傷害を受ける脳の組織を細胞移植によって再生させる方法の開発を目指して、ドナー細胞の調製とモデル動物への移植を行っている。これまでに、慶應義塾大学が開発したES細胞およびiPS細胞からの神経幹細胞の誘導方法を習得し、名古屋市立大学において培養技術を確立した。これらの細胞を飛田・戸苅らが近年開発したラットPVLモデル(Mizuno et al., Neonatology, 2008)へ移植し、治療効果を組織学的・行動学的に解析している。今後は移植後の細胞および動物の行動を詳細に解析し、PVLの治療に適した細胞の種類や移植に適した時期などについて検討を行う。
(3)腫瘍化防止技術の開発
脳疾患への細胞移植による再生医療を実現するためには、腫瘍化を防止する方法の開発が必須である。しかし、残存未分化幹細胞のみを標的として効率的に細胞死あるいは細胞分裂停止を誘導することは非常に困難である。本研究の特徴は、移植された細胞すべてに恒久的な細胞増殖停止状態である老化形質を誘導することで、再生した細胞の分化機能に影響を及ぼさずに腫瘍形成を完全に防ぐ技術を開発する点にある。本研究では、中西らが近年明らかにした細胞増殖制御機構(Shimada et al., Cell, 2008など)を応用して幹細胞に強制的な早期老化形質を導入し、移植後の腫瘍化を防止する方法の開発に取り組んでいる。既に、iPS細胞またはES細胞に老化誘導遺伝子を薬剤誘導プロモーター制御下で発現誘導することによって、細胞の増殖を停止させることに成功した。今後は、免疫不全マウスに細胞を移植した後で老化を誘導し、腫瘍化と治療効果への影響を詳細に解析していく予定である。リンク情報
名古屋市立大学大学院医学研究科再生医学分野
http://k-sawamoto.com/●
http://k-sawamoto.com/●
