事業成果
世界初の快挙
iPS細胞を用いた臨床手術に成功!2017年度更新

- 髙橋 政代(理化学研究所 生命機能科学研究センター 網膜再生医療研究開発プロジェクト プロジェクトリーダー)
- 戦略的イノベーション創出推進プログラム(S-イノベ)
- iPSを核とする細胞を用いた医療産業の構築「細胞移植による網膜機能再生」プロジェクトマネージャー(H21-23)
- 再生医療の実現化ハイウェイ
- 「iPS細胞由来網膜色素上皮細胞移植による加齢黄斑変性治療の開発」プロジェクトリーダー(H23-26)※
※当事業は2015年度より、国立研究開発法人 日本医療研究開発機構に移管されました
iPS細胞の登場から7年、実用化へのマイルストーン
世界に衝撃を与えた山中伸弥教授によるiPS細胞の樹立から7年後の2014年9月12日、滲出型加齢黄斑変性の患者に、患者自身のiPS細胞由来の網膜色素上皮(RPE)細胞のシートを移植する手術が行われた。iPS細胞から作製した組織を使用した臨床手術として、世界初の事例である。
滲出型加齢黄斑変性とは
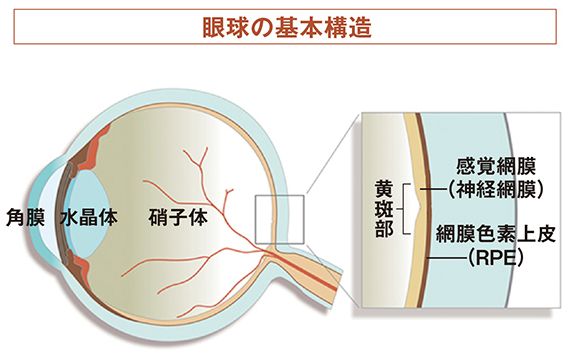
網膜は視細胞を含む感覚網膜(神経網膜)と網膜色素上皮(RPE)から構成される。RPEは感覚網膜への栄養補給や老廃物の消化を担っている。
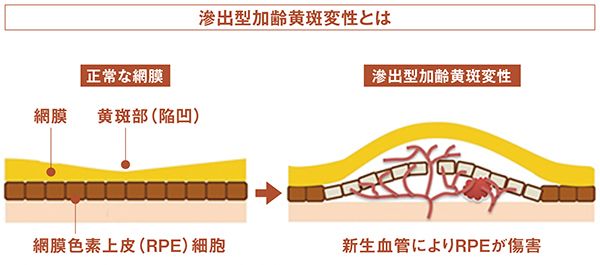
脈絡膜新生血管と呼ばれる異常な血管によりRPEや感覚網膜が傷害され、黄斑部の機能が低下する。
大きな壁もいつかは乗り越えられる——
目の網膜の中心部は黄斑と呼ばれ、ものを見る際に重要な働きをする。滲出型加齢黄斑変性は、その黄斑部の網膜の下から、新たに異常な血管が発生してくる病気だ。視力が低下し、やがて失明状態に陥る。発症の詳しい原因はわかっていないが、網膜色素上皮(RPE)細胞の老化が関連していると考えられる。血管の発生を抑える治療薬は開発されているが、傷んだRPE細胞や組織を元に戻すことはできない。根治のためにはRPE細胞の移植が必要だ。
髙橋政代プロジェクトリーダーは、生殖細胞由来の多能性幹細胞であるES細胞(胚性幹細胞)をRPE細胞へと分化誘導する研究を進め、成果を挙げてきたが、ES細胞は規制上の問題から日本では使用が認められず、RPE細胞への分化誘導技術が確立したとしても、実用化への道は開かれなかった。
iPS細胞実用化のフロントランナーに
そんな時、救世主のように現れたのがiPS細胞だった。患者自身の体細胞から作製できるから、倫理面の問題は小さく、拒絶反応の心配も少ない。「光が差し込むような思いがした」という髙橋リーダーは、S-イノベの研究リーダーとなり、iPS細胞からRPE細胞への分化誘導と臨床応用のための技術の確立に取り組んだ。幸い、分化誘導法がES細胞と大きく変わらなかったこともあり、研究は順調に進展。同時期にスタートしたほかのiPS細胞関連再生医療研究のなかでも頭一つ抜けた存在となり、iPS細胞実用化の先駆けとして注目を浴びた。
2011年に新成長戦略に基づく「再生医療の実現化ハイウェイ」がスタートすると、その課題「iPS細胞由来網膜色素上皮細胞移植による加齢黄斑変性治療の開発」として採択され、研究はさらに加速。臨床研究実施計画が2013年7月に厚生労働省から了承され、いよいよ臨床研究がスタートした。
iPS細胞からRPE細胞を作製
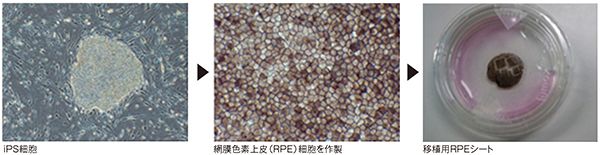
「最初の一歩」の意義は大きい
移植手術に先立ち、患者の腕の皮膚組織を採取して培養し、iPS細胞を作製。これをRPE細胞に分化誘導し、1.3mm×3mmのシート状にした。手術当日は、視力低下の要因となる異常な血管を取り除き、シート状のRPE細胞を移植。1年間の経過観察を終え、追跡調査を行っている。
今回の手術は、初期段階の臨床研究として行われた。主な目的は安全性の確認で、大幅な視力改善といった顕著な治療効果を期待するものではない。新規治療法として確立し、一般化されるまでには、今後長期にわたる臨床研究が不可欠だ。世界に衝撃を与えたiPS細胞は、人類に大きな恵みをもたらすための初めの一歩を踏み出した。
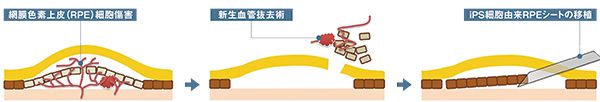
iPS細胞由来網膜色素上皮(RPE)シートの移植