事業成果
細胞生物学の基礎研究全般の推進にも貢献する成果
オートファジーを制御する重要な仕組みを解明2021年度更新

- 野田 展生(微生物化学研究所 部長)
- CREST
- [構造生命] ライフサイエンスの革新を目指した構造生命科学と先端的基盤技術「オートファジーの膜動態解明を志向した構造生命科学」研究代表者(2013-2020)
オートファジーの機能を担う構造体の仕組みや実体を解明
栄養飢餓の状態のとき、細胞内のタンパク質を分解するオートファジー。酵母からヒトに至るまですべての真核生物に備わった基本的かつ主要な機能だ。また、オートファジーの異常は神経変性疾患やがんを引き起こすことから、そのメカニズムを知ることは疾病の治療や予防法の開発にも不可欠だ。しかし、細胞内でオートファジーを担う構造体の仕組みや実体は長年不明だった。特にオートファジーにおいて、分解する対象物を包む袋状の脂質膜であるオートファゴソームが伸びていく仕組みについてはほとんどわかっていなかった。
それに対し、CRESTの野田展生氏らの研究グループは、オートファジーを担う構造体が、Atgタンパク質が「液-液相分離※1」した液滴※2であることを解明した(図1)。これは、液-液相分離という現象がオートファジーを直接制御しているということを示す新発見だ。また、野田らは、膜タンパク質Atg9がオートファゴソームの伸展に働くことも明らかにした。
今後、オートファジーを制御する新薬の開発などが期待される。
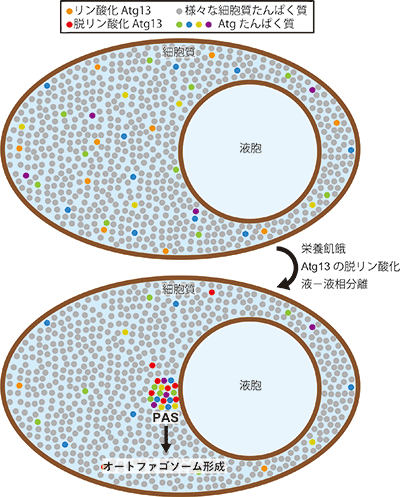
図1 オートファジーを担う構造体は「液-液相分離」した液滴だった
栄養豊富な条件では、Atgタンパク質は細胞質中に分散しているが、栄養飢餓になり、Atg13が脱リン酸化されると、Atg13は他のAtgタンパク質とともに「液-液相分離」して液胞膜上に新たな液相(液滴)を形成。その液滴からオートファゴソームが形成される
※1 液-液相分離
均質の溶液が2つ以上の液相に分離する現象のこと。細胞内には核やミトコンドリアなど膜で仕切られたオルガネラがあるが、近年、核酸やタンパク質の液滴が「膜のないオルガネラ」としてさまざまな役割を担っていることが考えられるようになった。膜のないオルガネラは、環境の変化に応じて迅速に形成、解消できることから、さまざまな役割があると予想される。
※2 液滴
タンパク質や核酸が液-液相分離することで形成した液体状の会合体。液滴は「膜のないオルガネラ」とも呼ばれ、細胞内でさまざまな機能を担っている。液滴は自発的に球形になる性質があり、内部流動性が高く、周囲とも活発な分子交換を行うなどの性質を持つ。
Atgタンパク質が液-液相分離した液滴がオートファジーを制御
オートファジーにおいては、細胞が栄養飢餓になるとオートファゴソームと呼ばれる脂質膜の袋が作られ、分解する対象物を包み込む。そして、分解の場であるリソソームに輸送され分解される。このオートファゴソームが作られる過程においては、約20種類のAtgタンパク質が関与していることがわかっていた。また、Atgタンパク質が集まり、PAS※3と呼ばれる構造体を形成することも知られていた。しかし、Atgタンパク質が集まる仕組みや、形成されたPASの実体はよくわかっていなかった。
それに対し、野田らの研究グループは、Atgタンパク質の一種であるAtg13を蛍光顕微鏡を使って詳細に調べた。さらに、PASを試験管内で再構成して挙動を調べた。加えて、高速原子間力顕微鏡※4を用いてPASを解析した。
その結果、PASの実体は、Atg13が他のAtgタンパク質とともに液-液相分離して形成された液滴であり、この液滴が液胞膜上に濃縮してPASを形成し、オートファゴソーム形成に働くことを明らかにした。
※3 PAS
「プレオートファゴソーム構造体」の略。酵母において、栄養飢餓になると液胞近傍の1カ所にAtgタンパク質が集まる。この集まった構造のこと。オートファゴソームはPASを起点として形成されると考えられる。
※4 高速原子間力顕微鏡
原子間力顕微鏡(AFM)は探針と試料の間に働く原子間力を基に分子の形状を可視化する顕微鏡。その中で、高速AFMは溶液中で動いているタンパク質などの生体分子をナノメートルの空間分解能とサブ秒の時間分解能で観察することができる装置。
Atg9がオートファゴソーム膜の伸展を引き起こすことが判明
オートファジーの最大の特徴は、オートファゴソームを新たに作り出す点にある。オートファゴソームを作る過程が分解する対象物を決定する。オートファゴソームの形成に関与しているのは、約20種類のAtgタンパク質で、そのほとんどは構造と機能の解析が進んでいる。以前野田らは、脂質輸送タンパク質Atg2がオートファゴソームを作るためのリン脂質を小胞体から運んでいることを発見した。しかし、運ばれたリン脂質を使ってどのようにオートファゴソームの脂質膜が伸展するのかについてはまったくわかっていなかった(図2)。
そこで、オートファジーを担うAtgタンパク質の中で、唯一機能がわかっていなかった膜タンパク質Atg9に着目した。酵母由来のAtg9を使い、試験管内で働きを丹念に調べた。その結果、Atg9がオートファゴソームの膜を構成する脂質を、リポソームを作る「脂質二重層」の二つの層の間で往来させる働きを持っていることを発見した。また、酵母のAtg9の立体構造をクライオ電子顕微鏡で調べたところ、Atg9は脂質二重層の2つの層をつなぐ細孔を持っていることが判明した(図3)。
これらの発見から、Atg9がオートファゴソーム膜の伸展を引き起こしていることを明らかにした。Atg9はAtg2と協力して、オートファゴソーム膜の形成に働いていたのだ(図4)。今回の発見はこれまで予想されてこなかった新たな仕組みであり、オートファジーの基礎研究の方向性を変える画期的な成果である。
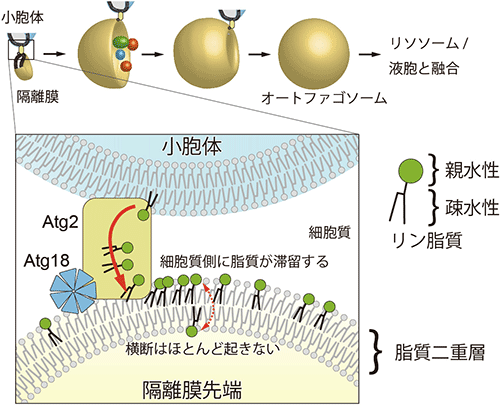
図2 オートファゴソーム形成過程の模式図
オートファジーが誘導されると、突如細胞質中に膜構造が出現し(隔離膜)、それが分解する対象物を包み込みながら伸展し、閉じてオートファゴソームとなる。隔離膜が伸展するために必要なリン脂質はAtg2が小胞体から供給すると考えられるが、それだけでは隔離膜の細胞質側の層に脂質が溜まり、膜が伸展しない
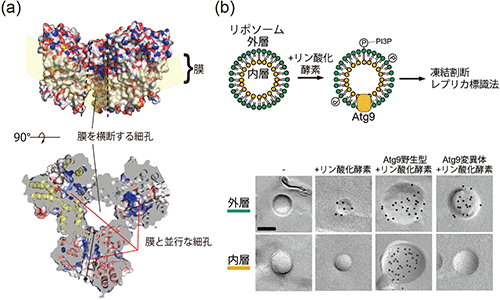
図3 Atg9の構造とその機能
(a)Atg9は中心に膜を貫通する細孔とそれぞれの分子に膜と並行な細孔が存在。それらがつながることで、脂質の通路を形成している。(b)Atg9はオートファゴソームの膜を構成する脂質(PI3P)を、リポソームの外層から内層に移動させる活性を持っている。しかし、その活性は細孔の変異体により阻害される。黒のドットはPI3Pの分布を表す
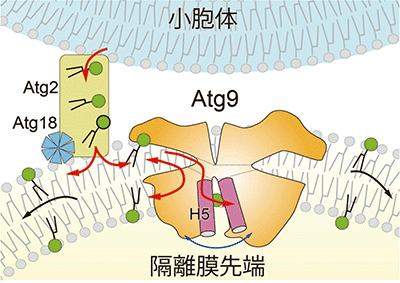
図4 Atg9とAtg2による隔離膜の伸展機構
Atg2は小胞体膜と隔離膜をつなぎ、小胞体膜に含まれるリン脂質を隔離膜の細胞質側の層へと輸送する。Atg9はAtg2、Atg18とともに隔離膜先端に局在し、Atg2が輸送したリン脂質を反対側の層へと移動させることで、隔離膜を伸展する
細胞生物学の基礎研究全般の推進に貢献する成果
液-液相分離によるオートファジーの直接制御の発見は、液-液相分離が細胞内の生命現象全般に広く関与していることを再認識させた成果である。また、オートファジーにおける長年の課題であったオートファゴソーム膜の伸展の仕組みが解明されたことで、今後、極めて複雑なオートファジーの仕組みの解明が一挙に進むことが予想される。仕組みの解明によって、オートファジーが関係するさまざまな疾病の治療法や予防法の研究が促進されることが期待される。さらに、今回発見した脂質輸送タンパク質と脂質スクランブラーゼの協働による膜伸展の機構は、オートファジーだけでなく、細胞生物学全般においても初めて明らかとなった現象であり、細胞生物学の基礎研究全般の推進に貢献することが期待される。
- ライフサイエンスの成果一覧へ
- 事業成果Topへ
- English