ポイント
- 腸内細菌は、胃切除を含むさまざまな治療と関連する可能性があることが知られていますが、治療による腸内環境への影響は詳細には明らかになっていませんでした。
- 本研究では、便検体を用いたメタゲノム解析およびメタボローム解析により、健常者と胃切除術を受けた患者を比較し、胃切除術後の患者に特徴的な腸内細菌叢やその機能、代謝物質の変化を明らかにしました。
- 胃切除後の患者にみられる腸内細菌の豊富さと多様さは、腸内細菌の代謝機能の変化を反映していると考えられます。
- また、大腸がんに関連する細菌や代謝物質の量が、胃切除後の患者、特に胃全摘術後の患者では相対的に多いことも確認されました。
- 便検体を用いた腸内環境の評価は今後、胃切除後の低栄養や貧血などの併発症の要因を解析する非侵襲な手法としての応用が期待されます。
東京工業大学 生命理工学院 生命理工学系の山田 拓司 准教授と大阪大学 大学院医学系研究科の谷内田 真一 教授(ゲノム生物学講座 がんゲノム情報学、前 国立がん研究センター 研究所 ユニット長)、慶應義塾大学 先端生命科学研究所の福田 真嗣 特任教授、国立がん研究センター 中央病院 内視鏡科の斎藤 豊 科長らの研究グループは、胃がんの治療として胃切除注1)の手術を受けた患者を対象に、凍結便を収集しメタゲノム解析注2)やメタボローム解析注3)を行いました。
腸内細菌は、病気の発症や進行だけでなく術後の病状にも関与しています。本研究では、胃切除後の患者の併発症や栄養状態などの改善を目的として、これまでほとんど解明されていない、胃切除の影響による腸内細菌叢注4)の構造や代謝物質の変化を調べ、術後の併発症注5)との関連性を検討しました。その結果、胃切除術を受けた患者は健常者と比較して腸内環境に大きな違いがあり、大腸がんと関連する細菌や代謝物質が増加していることを明らかにしました。この成果は、便検体を用いて腸内環境を評価することにより、胃切除後の併発症の要因を理解し個々人の腸内環境を評価することで、胃切除後の併発症の予防や治療に貢献する医薬品などを生み出す可能性を示すものです。
本研究は2020年1月17日(英国時間)に英国学会誌「Gut」に掲載されます。
本研究は以下の支援を受けて行われました。
- 戦略的創造研究推進事業 さきがけ
研究領域 「ビッグデータ統合利活用のための次世代基盤技術の創出・体系化」
(研究総括:喜連川 優 国立情報学研究所 所長/東京大学 生産技術研究所 教授)研究課題名 「ヒト腸内環境ビッグデータ」 研究者 山田 拓司(東京工業大学 生命理工学院 生命理工学系 准教授) - 戦略的創造研究推進事業 AIP加速課題
研究課題名 「ヒト腸内環境ビッグデータを基軸としたMicrobiome-based Precision Medicine」 研究代表者 山田 拓司(東京工業大学 生命理工学院 生命理工学系 准教授)
<背景>
ヒト一人の細胞数が約37兆個であるのに対し、ヒト一人あたりの腸内細菌数はおよそ40兆個、重さにして約1~1.5kgとされています。これらの腸内細菌叢の乱れが炎症性腸疾患注6)などさまざまな疾患と関係することが、最近になって分かってきました。また腸内細菌が、胃切除を含むさまざまな治療と関連する可能性があることも報告されています。胃切除は胃がんや重篤な肥満の治療法であり、欧米における肥満の治療のための胃切除手術の場合、術後の体重減少が腸内細菌叢の変化と関連することが報告されています。しかしながら、胃がんの治療のための胃切除による腸内環境への影響は、これまでほとんど明らかになっていませんでした。胃切除術後には、低栄養や貧血、ダンピング症候群注7)などの併発症があります。また胃がんの患者は、腸内細菌との関連が指摘されている異時性大腸がん注8)を術後に発症するリスクが高いことが知られています。従って、胃切除術を受けた患者における腸内環境を探索することは重要と考えられました。
<研究成果>
研究グループでは、国立がん研究センター 中央病院 内視鏡科(斎藤 豊 科長ら)を受診し、大腸内視鏡検査(大腸カメラ)を受けた106名の受検者(胃切除した患者50人と健常者56人)を対象として、食事などの「生活習慣などに関するアンケート」調査、凍結便、大腸内視鏡検査所見などの臨床情報を収集しました。この凍結便に対して、東京工業大学(山田 拓司 准教授ら)や慶應義塾大学 先端生命科学研究所(福田 真嗣 特任教授ら)と共同で、メタゲノム解析とメタボローム解析を行いました。その上で、胃切除した患者50人と健常者56人の腸内細菌叢を比較し胃切除後の患者に特徴的な細菌や代謝物質を探索しました。
その結果、胃がんの治療のための胃切除術と、それに伴う消化管の再建が、患者の腸内環境に大きな影響を与えることが明らかになりました。これを踏まえて、胃切除後の生理学的な変化が、腸内細菌叢や代謝物質にどのような変化をもたらし、それが術後の病態にどのように影響するのかという、それぞれの変化の関連性について検討しました(図1)。
本研究で行った解析では、胃切除後の患者は健常者と比較して、腸内細菌の種の豊富さ注9)と種の多様性注10)の高さが確認されました(図2A、B)。これらの違いは、胃切除による腸内環境の変化を反映している可能性があります。その変化の1つとして、胃切除後の患者では、口腔内でよく検出される細菌の相対的な量が多いことが確認されました(図2C)。
胃切除術は、栄養障害、貧血、下痢、ダンピング症候群などを引き起こすなど、術後の患者の代謝に影響を及ぼすことも広く知られています。本研究の解析でも、術後の患者の代謝の変化に関連する、腸内細菌の代謝機能の変化が見られました。例えば、胃切除後の患者では、小腸でのビタミンB12の吸収不足が知られていますが、今回の解析でも、ビタミンB12が小腸で吸収されずに大腸まで残り、それを細菌が利用するべく、ビタミンB12の摂取能力を持つ細菌が増加することが観察されました。
胃がんの患者は、異時性大腸がんを発症するリスクが高いことも報告されています。胃切除後の発がんメカニズムは、散発性大腸がん(通常の大腸がん)とは異なる可能性がありますが、本研究では、散発性大腸がんに関連することが知られている細菌の種類や代謝物質が胃切除後に多いことが観察されました。研究チームは最近、大腸がんの発生の初期にのみ増加する細菌を同定しています(「Nature Medicine」2019年6月号)。今回の解析でも、その1つであるAtopobium parvulum(図2D)や、発がんの初期から関連することが知られているFusobacterium nucleatum(図2E)が、胃切除後の患者で増加していることが認められました。特に、胃全摘術を受けた患者では、Fusobacterium nucleatumの量が多いことも確認されました(図2F)。さらに、肝臓がんおよび散発性大腸がんにおいて発がん性が知られているデオキシコール酸も、胃切除後の患者の便中に多く含まれていました(図3)。こうした結果は、胃切除後の患者に対する定期的な全身のフォローアップの重要性を示しています。
<今後の展開>
本研究では、胃切除後の病態メカニズムを腸内環境の変化という観点から検討しました。その成果は、胃切除だけではなく、他の疾患の治療後の長期的な併発症にも応用可能なフレームワークの可能性を示しています。また、本研究成果は、胃切除後の患者に定期的に大腸内視鏡検査を行って、異時性大腸がんの発生を早期に発見する必要性がある可能性を示唆しています。本研究で明らかになった知見は、便検体を用いた腸内環境の観点から、胃切除後の低栄養や貧血などの病態を理解し、今後、その病態を非侵襲的に評価する手法として応用される可能性や、術後の栄養状態の改善などに腸内細菌の観点から介入し、それらを改善する医薬品や健康食品などを生み出す可能性があります。
<参考図>
-
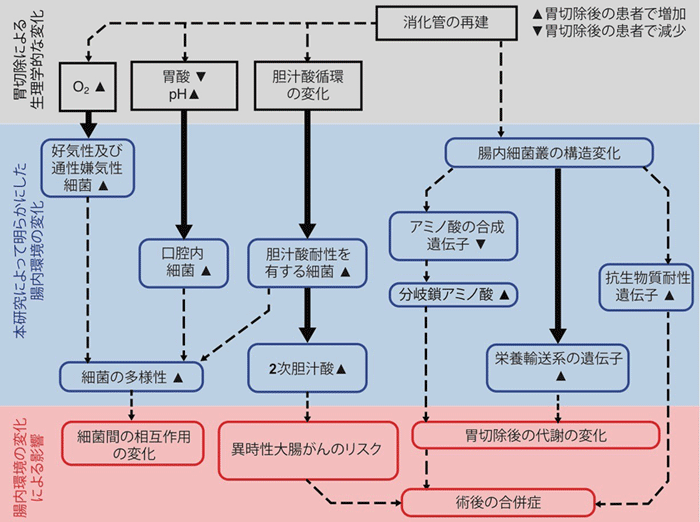
図1 本研究によって得られた仮説の概略図 胃切除による生理学的な変化を灰色、本研究により明らかになった腸内環境の変化を青色、その腸内環境の変化による影響を赤色で示しています。点線の矢印は、本研究の結果から説明できるつながりを表しています。実線の矢印は、それぞれのつながりが先行研究によって得られた仮説であることを表しています。
-
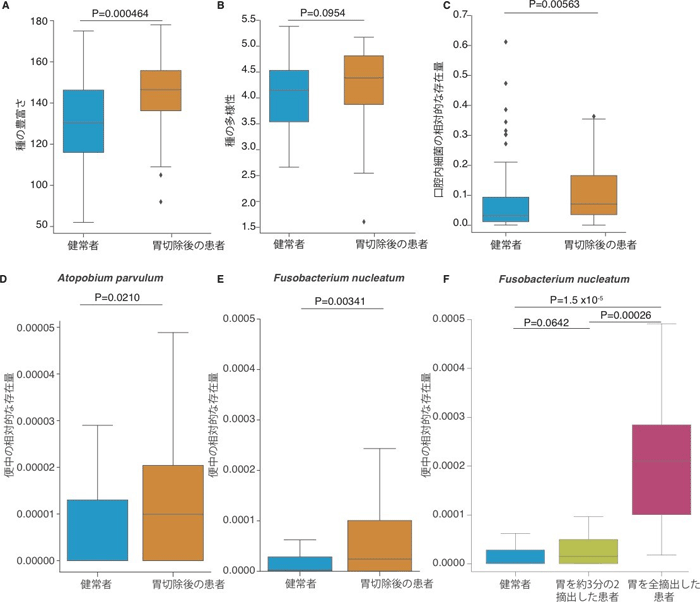
図2 胃切除後の患者の腸内細菌叢の変化 腸内細菌の種の豊富さ(A)とその多様性(B)はどちらも、胃切除後の患者で多いことが確認されました。D、E、Fは、大腸がんの発がんとの関連性が報告されている細菌の一部の相対的な存在量を表しています。発がんの初期にのみ量が多いAtopobium parvulum(D)と、発がんの初期に関係することが知られているFusobacterium nucleatum(E)は胃切除後の患者で多いことが分かりました。また、Fusobacterium nucleatumは胃を全摘出した患者で特に多いことが確認されました(F)。D、E、Fでは図中の外れ値を省略して表示しています。
-
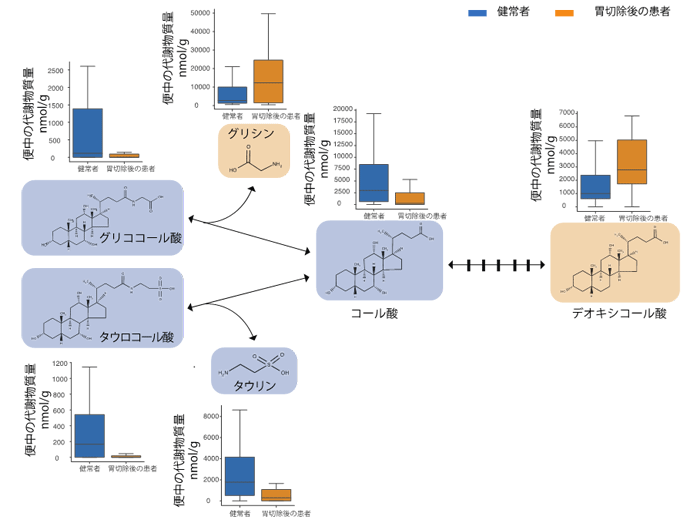
図3 散発性大腸がんと関連する代謝物質の変化 メタボローム解析により、胆汁酸注11)と関連がある代謝物質が胃切除後の患者で変化していることが認められました。肝臓がんおよび散発性大腸がんで発がん性が知られているデオキシコール酸は、胃切除後の患者で多いことが確認されました。一次胆汁酸であるタウロコール酸とグリココール酸は肝臓で生成され、その後腸肝循環注12)によって腸管内へ移動され、腸内細菌によってコール酸と二次胆汁酸の1つであるデオキシコール酸へ代謝されることが知られています。図中の代謝物質の箱ひげ図は外れ値を省略して表示しています。
<用語解説>
- 注1)胃切除
- 胃がんの外科治療法で、主に幽門側胃切除術(胃の出口側の約3分の2を切除)と胃全摘術がある。最近では病的な肥満の治療としても使われる。
- 注2)メタゲノム解析
- 環境(例えば腸管内の便)中の細菌群集からDNAを丸ごと抽出し、ゲノム配列を次世代シークエンサーで網羅的に解読し(全ゲノムショットガンシークエンス解析と呼ぶ)、情報解析の専門家が系統組成(どのような種類の細菌がいるか)と機能(どのような機能を有する細菌がいるか)の解析を行う技術。
- 注3)メタボローム解析
- 糖やアミノ酸など体内にある代謝物質(メタボライト)数百種類以上の含有量を、質量分析計を用いて一度に丸ごと成分を分析する技術。
- 注4)腸内細菌叢
- ヒトまたは動物の腸内に生息し、共生関係にある細菌の総称。
- 注5)術後の併発症
- 病気の初期状態とは別に、外科的処置後に発生した他の症状または合併症。
- 注6)炎症性腸疾患
- 宿主であるヒトの免疫システムの異常により、消化管で炎症が生じる腸疾患。主に潰瘍性大腸炎とクローン病に区別される。
- 注7)ダンピング症候群
- 胃切除後に、胃内の食物が急速に小腸に流れ込んでしまうために生じる一連の症状。冷や汗、動悸、めまい、顔面紅潮、全身倦怠感、全身脱力感、全身熱感など。晩期では、高血糖または低血糖が生じることがある。
- 注8)異時性大腸がん
- 原発がんの6ヵ月以上後に発生する大腸がん。
- 注9)種の豊富さ
- 特定のサンプル、コミュニティー、またはエリア内で観察される種の数。Chao1インデックスは、コミュニティー内の種の豊富さを推定する方法の1つとして用いられる。
- 注10)種の多様性
- 種の豊富さと、特定のコミュニティー内での分布を説明する指標。シャノンインデックスやシンプソンインデックスなどが広く用いられる。
- 注11)胆汁酸
- 酸は通常、肝臓でアミノ酸のグリシンとタウリンまたは硫酸塩に結合して、結合した胆汁酸を形成する。一次胆汁酸は、腸内細菌によって代謝されて、デオキシコール酸などの二次胆汁酸を形成する。
- 注12)腸肝循環
- 肝臓で代謝される薬や生体物質などが胆汁と共に腸管から十二指腸に分泌され、その後腸管から吸収され、門脈を経て再び肝臓に排出される一連の循環サイクル。
<論文タイトル>
- “Influence of gastrectomy for gastric cancer treatment on faecal microbiome and metabolome profiles”
- DOI:10.1136/gutjnl-2019-319188
<お問い合わせ先>
-
<研究に関すること>
山田 拓司(ヤマダ タクジ)
東京工業大学 生命理工学院 生命理工学系 准教授
Tel:03-5734-3591 Fax:03-5734-3591
E-mail:takujibio.titech.ac.jp
谷内田 真一(ヤチダ シンイチ)
大阪大学 大学院医学系研究科 がんゲノム情報学 教授
Tel:06-6879-3360 Fax:06-6879-3369
E-mail:syachidacgi.med.osaka-u.ac.jp
斎藤 豊(サイトウ ユタカ)
国立がん研究センター 中央病院 内視鏡科 科長
Tel:03-3542-2511 Fax:03-3542-3815
E-mail:ysaitoncc.go.jp
-
<AMED事業に関すること>
難治性疾患実用化研究事業
日本医療研究開発機構 戦略推進部 難病研究課Tel:03-6870-2223
E-mail:nambyo-infoamed.go.jp
次世代がん医療創生研究事業(P-CREATE)
日本医療研究開発機構 戦略推進部 がん研究課Tel:03-6870-2221
E-mail:canceramed.go.jp
-
<JST事業に関すること>
科学技術振興機構 戦略研究推進部 ICTグループ
Tel:03-3512-3525 Fax:03-3222-2066
E-mail:prestojst.go.jp
-
<報道担当>
東京工業大学 広報・社会連携本部 広報・地域連携部門
Tel:03-5734-2975 Fax:03-5734-3661
E-mail:mediajim.titech.ac.jp
大阪大学 大学院医学系研究科 広報室
Tel:06-6879-3388 Fax:06-6879-3399
E-mail:medproffice.med.osaka-u.ac.jp
慶應義塾大学 先端生命科学研究所 渉外担当
Tel:0235-29-0802 Fax:0235-29-0809
E-mail:officettck.keio.ac.jp
国立がん研究センター 企画戦略局 広報企画室
Tel:03-3542-2511 Fax:03-3542-2545
E-mail:ncc-adminncc.go.jp
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail:jstkohojst.go.jp
