<ポイント>
- 鏡像異性体(右手と左手の関係)を持つアミン化合物は、医薬品原料などとして重要です。
- 2つの鏡像異性体のうち1つだけに作用する自然界には存在しないアミン酸化酵素を開発し、目的とする100%の鏡像異性体を生産する方法を開発しました。
- アルツハイマー治療剤など鏡像異性体を持つ医薬品生産への応用が期待されます。
JST 課題達成型基礎研究の一環として、富山県立大学の浅野 泰久 教授、安川 和志 研究員らは、アミン化合物((R )-α-メチルベンジルアミン)注1)に作用する自然界には存在しない新しいアミン酸化酵素を世界で初めて開発し、さらにこの酵素を用いてS型のα-MBAを高収率、高純度で生産する方法の開発に成功しました。
医薬品などに使われる化合物には、右手と左手の関係のように構造は同じであるのに働き方が違う鏡像異性体注2)が存在する場合があります。鏡像異性体の中には、体に悪影響を与えるものもあるため、医薬品開発では目的の鏡像異性体だけを作り分ける技術が必要です。有機合成化学の手法では、一方の鏡像異性体だけを生産する触媒が高価であることや、精製工程の収率が低いといった課題が存在しますが、酵素を利用した合成では、有用な鏡像異性体だけを低コスト・高収率に合成できることが知られています。α-MBAは鏡像異性体としてR型とS型があり、それぞれが医薬品の原料となるなど産業用にも重要です。しかし、これまでに見つかっている酵素はS型のみに働くもので、R型のα-MBAは得られても、S型のα-MBAを得ることはできませんでした。
本研究グループは、α-MBAから100%のS型のα-MBAを作る方法の開発を目指し、たんぱく質工学的手法注3)を用いて、ブタ腎臓由来のD-アミノ酸酸化酵素からR型のα-MBAに特異的に作用するR-立体選択的アミン酸化酵素を開発しました。さらにこの酵素を低分子の還元剤と併用することにより、R型とS型が混在したラセミ体注4)から100%S型に変換する「デラセミ化法」の開発にも成功しました。
これらの成果は、今後α-MBA以外の鏡像異性体を持つアミン化合物に対しても応用可能であり、アルツハイマー型認知症治療剤など、一方の鏡像異性体のみを構造中に含む医薬品などの生産に、安価でクリーンな技術として役立つことが期待されます。
本研究成果は、ドイツの科学雑誌「Angewandte Chemie International Edition」のオンライン速報版で近日中に公開されます。
本成果は、以下の事業・研究プロジェクトによって得られました。
戦略的創造研究推進事業
| 研究プロジェクト |
「浅野酵素活性分子プロジェクト」 |
| 研究総括 |
浅野 泰久(富山県立大学 生物工学研究センター 教授) |
| 研究期間 |
平成23年8月~平成29年3月 |
上記研究課題では、微生物のみならず植物や動物などにおける高活性な酵素分子が示す反応を探究し、有用物質生産や健康診断法などに資する手法の基盤創出への展開を目標としています。
<研究の背景と経緯>
鏡像異性体は、平面的には全く同じ構造でありながら、立体的には鏡に映したように対象の構造を持つ有機化合物のことです(図1)。それぞれの鏡像異性体は働きが全く異なる場合もあり、生物の体内では、おおむね一方の鏡像異性体のみが存在しているとされています。このため、両方の鏡像異性体が混ざったものを医薬品などとして使用した場合、サリドマイド事件注5)のように、重篤な副作用の原因となることがあります。
従って、医薬品などの開発では、鏡像異性体のうち目的にあったものだけを生産することは非常に重要です。一般的な有機合成化学的手法では、一方の鏡像体だけを合成することができる不斉触媒注6)を用いる方法と、2つの鏡像異性体を分離する方法があります。しかし、不斉触媒は一般に高価です。また分離する方法では理論的にラセミ混合物の半分しか純粋な鏡像異性体が得られずに収率が低いといった問題がありました。
一方、生物の体内で化学反応を触媒する酵素の多くは、一方の鏡像異性体のみに作用することができます。この性質を利用することで、安価に効率よく有用な鏡像異性体を生産する方法が知られています。
今回の実験で用いたα-MBAは、医薬品などの原料や光学分割剤注7)として有用な物質であることから、鏡像異性体の選択的な生産技術の開発は産業的にも重要です。すでにある種の酵素を用いて、ラセミ体から一方の鏡像異性体のみを他の物質へ変換する光学分割が報告されていますが、この方法では、理論上50%しか目的とする鏡像異性体を得ることができませんでした。また、一方の鏡像異性体S型のα-MBAに選択的に作用する酸化酵素は報告されていましたが、R型のα-MBAに選択的に作用する酵素は報告されていませんでした。
<研究の内容>
本研究グループは、ラセミ体のα-MBAから100%S型のα-MBAを作る方法の開発を目指し、ブタ腎臓由来のD-アミノ酸酸化酵素からたんぱく質工学的手法を用いて自然界には存在しないR型のα-MBAに選択的に作用する酸化酵素を世界で初めて開発しました(図2)。
この酵素をラセミ混合物のα-MBAに作用させると、R型のみがアセトフェノンへと変換されるため、理論上50%の収率でS型のα-MBAを得ることができます。さらに、低分子の還元剤と併用することにより、(S型のα-MBAのみが100%の収率で蓄積されるデラセミ化法の開発にも成功しました(図3)。
このデラセミ化法では、R型のα-MBAが酵素により酸化される反応の途中で、低分子還元剤によりα-MBAに強制的に戻されます。この時、反応途中で戻されたα-MBAは、S型とR型が同じ確率で生じるので酵素により酸化されたR型のα-MBAがS型とR型が同じ割合でα-MBAに戻されることになります。反応により生じるα-MBAのうちR型は、再度酵素反応で使用されるため、このサイクルが繰り返されることで酵素が作用しないS型の比率が上昇し、最終的に副反応や精製工程の損失により収率は、65%でしたが純度100%のS型のα-MBAを得ることができました。
このように、今回開発したデラセミ化法により従来の光学分割的手法と比べ、倍の収率でS型のα-MBAを生産できます。
<今後の展開>
α-MBAは、光学分割剤や医薬品原料として使用される物質であり、鏡像異性体の選択的生産の高効率化、低コスト化は産業上有用です。また、今回開発した酵素は、広い基質特異性注8)を持っており、さらに改良することで、例えばアルツハイマー型認知症治療剤リバスチグミンや過敏性膀胱治療薬ソリフェナシンなど、鏡像異性体を持つさまざまなアミン化合物の生産に応用できる可能性があります。本研究で開発されたデラセミ化法は、光学純度の高い製品の生産法としても利用可能です。さらに、本研究で開発したアミン酸化酵素は、デラセミ化以外の反応にも利用可能と考えられ、新たな有用物質生産用の酵素など産業利用も期待されます。
<参考図>
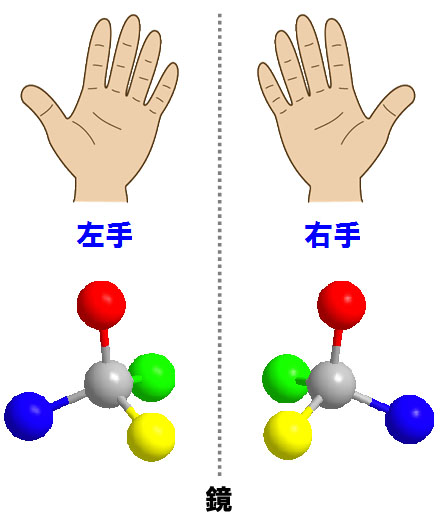
図1 鏡像異性体(光学異性体)
右手と左手は5本の指があって、手のひらがあってという具合に、一見、同じ形をしているように見えます。しかし、手のひらを上にして両手を重ねてみても、同じ方向ではどんなに回転させても、同じ指が同じ位置に重なることはありません。鏡に映った鏡像のような関係になっています。同様に、構成する元素や官能基は全く同じでも、立体的にみると鏡に映ったように対象の関係で、同じ方向に重ね合わせることができない化合物を鏡像異性体と呼びます。
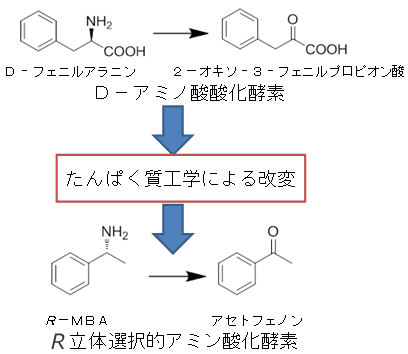
図2 R 立体選択的アミン酸化酵素の創製
ブタ腎臓由来D-アミノ酸酸化酵素にたんぱく質工学による改変を行い世界で初めてR型のα-MBAに立体選択的に作用する自然界には存在しないアミン酸化酵素の作成に成功しました。
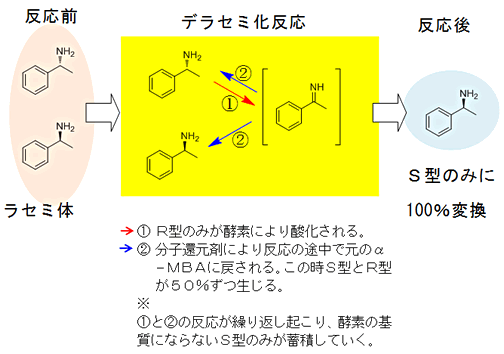
図3 デラセミ化反応によるラセミ体からのS型のα-MBAの生産
<用語解説>
- 注1)アミン化合物((R)-α-メチルベンジルアミン)
- アミン化合物とは、炭化水素にアミノ基が置換した化合物の総称です。α-MBAは、エチルベンゼンのα位(ベンゼン環に直接結合している炭素原子)にアミノ基が置換しており、鏡像異性体(注2参照)が存在します。
- 注2)鏡像異性体
- 構成する元素や官能基が全く同じであるが、立体的にみると鏡に映ったように対象の関係でちょうど右手と左手の様に、同じ方向では重ね合わせることができない化合物。平面上の構造は、全く同じであるため、物理化学的な性質は、旋光度という分光学的な性質を除き全く同一です。2つの鏡像異性体をそれぞれDとLやSとRで表記しますが、DL標記とSR標記では、定義が異なります。
- 注3)たんぱく質工学的手法
- 組み換えDNA技術、遺伝子の化学合成技術などを用いてたんぱく質の性質を異なるものに改変し、新しい性質のたんぱく質を作成する学術領域。また、改変する際には、アミノ酸配列の他、立体構造(たんぱく質の結晶構造)や計算機化学などの情報と合わせてたんぱくを設計することもあります。
- 注4)ラセミ体
- 2つの鏡像異性体が等量存在している状態。ラセミ混合物ともいう。
- 注5)サリドマイド事件
- 催眠鎮静薬サリドマイドが、副作用として四肢の発達などを阻害する催奇性を持つことから、世界的に被害が出ました。日本では、1959年に胃腸薬「プロバンM」にサリドマイドを配合して販売されたものが、妊婦のつわり防止などに使用された結果、多くの奇形児が発生する被害がでました。サリドマイドは、鏡像異性体を持ちますが、当時は、ラセミ体として合成されていました。のちにR型は無害であるが、S型に高い催奇性があることが示されました。この事件をきっかけに鏡像異性体による副作用に注意が払われるようになりました。
- 注6)不斉触媒
- 有機合成において不斉合成、つまり鏡像異性体の一方のみを作るために用いる触媒。一般的に高価なものが多い。
- 注7)光学分割剤
- ラセミ体をそれぞれの鏡像異性体に分離する操作を光学分割といいます。光学分割の方法には、いくつかありますが、α-MBAのような鏡像異性体を持つアミン化合物でSもしくはR型のみを含むものを光学分割剤を使用し、ラセミ体の酸を塩に誘導して分別結晶する方法が知られています。
- 注8)基質特異性
- ある酵素反応が特定の基質構造を識別し、その基質のみ化学反応が起こることを基質特異的であるといい、このような酵素の性質を基質特異性といいます。
<論文名>
“Tailoring D-amino acid oxidase from the pig kidney to R-stereoselective amine oxidase and its use in deracemization of a-methylbenzylamine”
(ブタ腎臓由来D-アミノ酸酸化酵素からR選択的アミン酸化酵素への変換とこの酵素を用いたα-メチルベンジルアミンのデラセミ化)
doi: 10.1002/anie.201308812
<お問い合わせ先>
<研究内容に関すること>
浅野 泰久(アサノ ヤスヒサ)
富山県立大学 浅野酵素活性分子プロジェクト
〒939-0398 富山県射水市黒河5180 富山県立大学 生物工学研究センター
Tel:0766-88-2280 Fax:0766-88-2422
E-mail:
<JSTの事業に関すること>
中村 幹(ナカムラ ツヨシ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
富山県立大学 教務課情報研究係
〒939-0398 富山県射水市黒河5180
Tel:0766-56-7500(229) Fax:0766-56-6182