ポイント
- 水素の工業的利用には白金などの希少な触媒が使われており、その代替が急務である。
- 温和な条件で水素を活性化する新規の半合成型の鉄ヒドロゲナーゼ酵素の作製に成功した。
- 水素の工業的利用を可能にする酵素の大量生産や機能改良への応用が期待できる。
JST 戦略的創造研究推進事業において、マックスプランク陸生微生物学研究所の嶋 盛吾 グループリーダーらは、大量合成が可能なたんぱく質中に化学的に合成した金属化合物を取り込むことで、温和な条件で水素ガスを生産または分解する半合成型注1)鉄ヒドロゲナーゼ酵素の創出に成功しました。
常温常圧の温和な条件で水素ガスを生産/利用している微生物は「ヒドロゲナーゼ」酵素と呼ばれる生体触媒を使って水素ガスの活性化を行っています。なかでも鉄ヒドロゲナーゼ酵素は、さまざまな有機物に水素添加の化学反応を促進することから、化学工業への利用や水素生産への活用が期待されています。その鉄ヒドロゲナーゼ酵素はメタン生産菌で生産され、温和な条件で水素ガスを活性化する生体触媒です。ヒドロゲナーゼ酵素の中でも比較的シンプルな構造で、耐久性も高いことから、触媒機能を利用した技術の開発が望まれていますが、メタン生産菌の大量培養が難しいことから、実現は困難とされていました。
嶋グループリーダーらは、大量培養可能な大腸菌に遺伝子を組み込み、鉄ヒドロゲナーゼ酵素を構成するたんぱく質を生合成し、そのたんぱく質に、化学的に合成したコンパクトな金属化合物を取り込ませる方法を見いだすことで、水素を生産または分解する機能を持つ、半合成型鉄ヒドロゲナーゼ酵素の作製に成功しました。
将来的に、鉄ヒドロゲナーゼ酵素の触媒機能を持つ生体触媒の大量生産につながることが期待できます。また、反応活性中心となる金属化合物を自由に設計・取り込むことが可能になり、より優れた酵素触媒の開発も可能になります。
本研究成果は、2015年11月2日(英国時間)に英国科学誌「Nature Chemistry」のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 個人型研究(さきがけ)
| 研究領域 |
「光エネルギーと物質変換」
(研究総括:井上 晴夫 首都大学東京 人工光合成研究センター センター長/特任教授) |
| 研究課題名 |
「[Fe]-ヒドロゲナーゼの活性中心鉄錯体の生合成」 |
| 研究者 |
嶋 盛吾(マックスプランク陸生微生物学研究所 グループリーダー) |
| 研究実施場所 |
マックスプランク陸生微生物学研究所 |
| 研究期間 |
平成21年10月~平成27年3月 |
JSTはこの領域で、人類にとって理想的なエネルギー源である太陽光による広義の物質変換を介して、光エネルギーを化学エネルギーに変換・貯蔵・有効利用し得る高効率システムの構築を目指した、独創的で挑戦的な研究を実施しています。
<研究の背景と経緯>
水素は今後の社会を支えるエネルギー源として注目されています。例えば、燃料電池で水素を電気エネルギーへ変換する技術が製品化されており、光や電気を使って水から水素ガスを生産する研究が進んでいます。そのための鍵となるのが、水素ガスを生産できる、あるいは水素ガスを分解できる水素活性触媒の開発です。現在、水素活性触媒として使われている白金などの希少元素は高価であるだけでなく、供給量が限られており、工業レベルの技術開発に向けて新しい材料の開発が急務となっています。
一方で、自然界に目を転ずると、さまざまな微生物が常温常圧の温和な条件で水素ガスを生産したり利用したりしています。これらの微生物は「ヒドロゲナーゼ」酵素と呼ばれる生体触媒を用いて水素ガスの活性化を行っています。世界では3種類のヒドロゲナーゼ酵素が知られていますが、なかでも鉄ヒドロゲナーゼ酵素は、さまざまな有機物に水素添加の化学反応を促進することから、有用物質生産やエネルギー貯蔵など化学工業に有効利用でき、また水素生産にも活用できる可能性が指摘されてきましたが、工業的利用のためには、高い水素活性を示す酵素を大量に生産することが必要です。
自然界では、鉄ヒドロゲナーゼ酵素はメタン生産菌で生産(生合成)されますが、メタン生産菌は大量培養が難しい微生物であるため、本酵素の大量生産が実現していません。一方で、大量培養が可能な大腸菌などの遺伝子組み換え技術によってさまざまな酵素を大量生産できることが知られていますが、鉄ヒドロゲナーゼ酵素は、たんぱく質の部分と水素反応活性を左右する、反応活性中心注2)と呼ばれる鉄化合物の部分で構成されており(図1)、既知の遺伝子情報では、大腸菌がこの鉄化合物を合成することはできないため、触媒機能を持つ鉄ヒドロゲナーゼ酵素の生合成は成功していません。
<研究の内容>
今回、マックスプランク陸生微生物学研究所の嶋 盛吾 グループリーダーらは、天然の酵素に含まれる反応活性中心を模擬したコンパクトな鉄化合物を化学合成し、遺伝子組み換えを行った大腸菌が合成したたんぱく質に取り込ませることによって、触媒活性を示す半合成型鉄ヒドロゲナーゼ酵素の作製に世界で初めて成功しました(図2)。
反応活性中心となる鉄化合物は、スイス連邦工科大学 ローザンヌ校のシーレ フー(Xile Hu) 教授が、化学合成手法を用いて作製しました。しかし、この化合物単体では触媒活性が認められず、たんぱく質の部分と組み合わせて初めて、触媒活性が確認できました。今回の発見により、酵素が触媒する反応においては、反応活性中心だけではなく、たんぱく質の創出する環境が触媒活性発現に重要であることも見いだしました。
<今後の展開>
大腸菌でたんぱく質を作ることおよび、金属化合物を化学合成することは容易であるため、この半合成型酵素は大量生産が可能です。
今回得られた半合成型酵素の活性はまだ低く、天然の酵素のわずか1%程度ですが(図3)、この性能は、これまでに開発されているほとんどの人工ヒドロゲナーゼ触媒の性能を凌駕しています。化学合成方法を工夫することにより、金属化合物の構造を変化させ、天然酵素の機能を改良することも可能であるため、将来的に、この技術が、酵素の工業的利用に結びつくことが期待されます。
<付記>
本研究は、スイス連邦工科大学ローザンヌ校のシーレ フー(Xile Hu) 教授と共同で行ったものです。
<参考図>
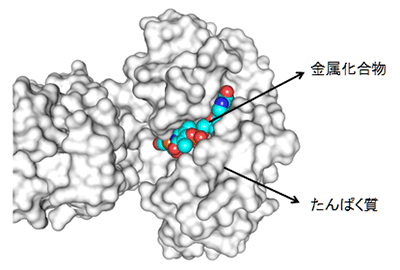
図1 天然の鉄ヒドロゲナーゼ酵素の構造の模式図(金属化合物の部分)
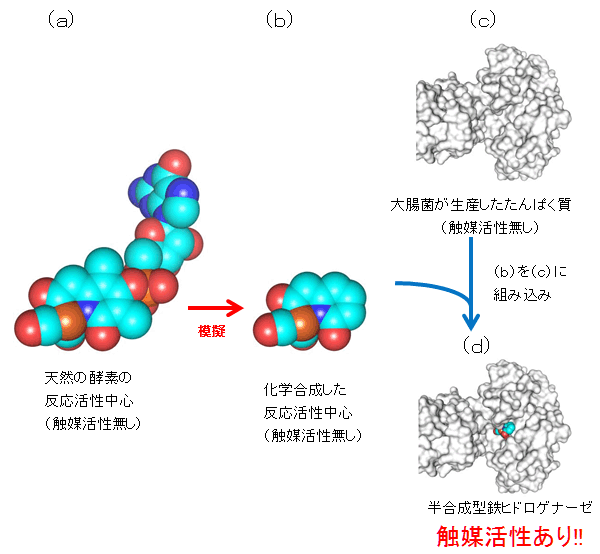
図2 鉄ヒドロゲナーゼ酵素の半合成
- (a)天然の鉄ヒドロゲナーゼ酵素の反応活性中心化合物(単体では触媒活性無し)
- (b)基本構造だけを化学合成で模擬したコンパクトな反応活性中心化合物(単体では触媒活性無し)
- (c)大腸菌が生産したたんぱく質
- (d)大腸菌で生産したたんぱく質に化学合成した金属化合物を取り込んだ半合成型鉄ヒドロゲナーゼ酵素(触媒活性あり)
- 解説:水色は炭素、青色は窒素、赤色は酸素、オレンジ色はリンを表します。
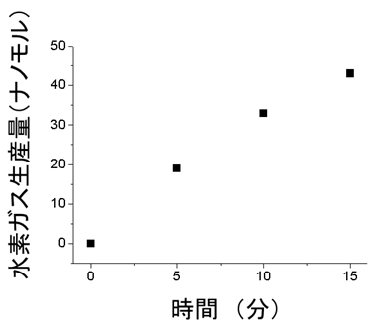
図3 半合成型鉄ヒドロゲナーゼ酵素の触媒活性
メチレンテトラヒドロメタノプテリン(メチレン-H4MPT)と半合成型ヒドロゲナーゼ酵素を含むリン酸緩衝液(pH7.5)を40℃で反応させて、水素ガス発生量をガスクロマトグラフィーで測定したところ、天然の酵素の約1%の活性を観察できました。
水素発生反応式:メチレン-H4MPT+H+→メテニル-H4MPT++H2
<用語解説>
- 注1) 半合成型酵素
- 酵素のような複雑な構造を合成する場合は微生物による生合成が有効ですが、完全な生合成が難しい場合は、部分的に生合成を用い、残りの部分を別の手法で合成することが可能です。このような手法は半合成型と呼ばれます。
- 注2) 反応活性中心
- 酵素において、反応に必要な基質や補酵素などが結合する部分で、触媒反応の活性を左右します。
<論文タイトル>
“Reconstitution of [Fe]-hydrogenase using model complexes”
(モデル錯体を用いた鉄ヒドロゲナーゼの再構成)
Seigo Shima, Dafa Chen, Tao Xu, Matthew D. Wodrich, Takashi Fujishiro, Katherine M. Schultz, Jörg Kahnt, Kenichi Ataka and Xile Hu
doi :10.1038/NCHEM.2382
<お問い合わせ先>
<研究に関すること>
嶋 盛吾(シマ セイゴ)
マックスプランク陸生微生物学研究所 グループリーダー
Karl-von-Frisch Straβe 10, 35043 Marburg, Germany
Tel:+49-6421-178122 Fax:+49-6421-178199
E-mail:
<JST事業に関すること>
鈴木 ソフィア沙織(スズキ ソフィアサオリ)
科学技術振興機構 戦略研究推進部 グリーンイノベーショングループ
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3531 Fax:03-3222-2066
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: