ポイント
- 本技術「Intelligent Image-Activated Cell Sorter」は細胞の高速イメージングと深層学習を用いた画像解析で細胞を一つ一つ網羅的に高速識別し、その解析結果に応じて所望の細胞を分取する世界初の基盤技術です。
- 免疫学、病理学、微生物学、分子生物学、遺伝学、再生医学、移植など多岐にわたる分野で基盤技術として不可欠である高速細胞分取技術「Fluorescence-Activated Cell Sorter」(開発者のHerzenberg氏は本貢献により2006年に京都賞を受賞)に顕微イメージング活性化(Image-Activated)と深層学習(Intelligent)を融合する飛躍的な発展であります。
- 本技術の原理実証として微生物や血液を用いて細胞の内部分子構造や形態などのさまざまな空間的情報に基づいた高速細胞分取を実現したことから、今後は生命科学(分子生物学、微生物学、医学、薬学など)における科学的発見およびバイオ産業や医療の発展への寄与が期待されます。
ImPACTプログラム「セレンディピティの計画的創出」の合田 圭介 プログラムマネージャーが率いる研究グループは、細胞の高速イメージングと深層学習を用いた画像解析で細胞を高速に識別し、その解析結果に応じて所望の細胞を分取する基盤技術「Intelligent Image-Activated Cell Sorter」の開発に世界で初めて成功しました。さらに本技術を用いて、微生物や血液細胞をその形状や内部構造を指標として分取する原理実証を行い、本技術の有用性や汎用性が確認されました。この快挙は、超高速蛍光イメージング技術注1)、10ギガビットイーサーネット注2)による高速データ処理システム、マイクロ流体技術注3)を活用した高速分取技術や細胞制御技術など、複数分野にまたがる異分野融合での大規模な共同研究によって達成されました。
本研究成果は、2018年8月27日(米国時間)に米科学誌「Cell」のオンライン版で公開されます。
本成果は、以下のプログラムによって得られました。
内閣府 革新的研究開発推進プログラム(ImPACT)https://www.jst.go.jp/impact/
研究開発プログラム「セレンディピティの計画的創出による新価値創造」
(プログラムマネージャー:合田 圭介、研究期間:平成26年10月~平成31年3月)
本プログラムでは、膨大な細胞集団から単一の目的細胞を発見する技術の開発に取り組んでいます。
<合田 圭介 プログラム・マネージャーのコメント>
本成果は、内閣府 革新的研究開発推進プログラム(ImPACT)「セレンディピティの計画的創出」に参画する、光量子科学、電気工学、機械工学、化学、情報科学、医学、生物学など多くの異分野にわたる研究者の共同開発によるものです。今回開発したIntelligent Image-Activated Cell Sorterは、延べ200名以上の研究者の2年半にわたる要素技術開発と、そこで生み出された最先端技術を組み合わせた2年にわたる統合システム開発により実現した、本プログラムの集大成の1つの成果となります。本研究成果により、本技術は、微生物や血液などさまざまな大きさや形状の細胞集団に対して、一つ一つの細胞の画像を網羅的に調べあげて解析し、必要な細胞を分取することができる汎用的な装置であることが示されました。今後、生物学、創薬、医学など幅広い分野においてこれまで膨大な時間や手間がかかり偶然の幸運な発見「セレンディピティ」が必要とされていた事象について、本技術により計画的に発見できるようになると期待されます。本技術をオープン利用展開することで、国内外の多数の研究者が新たな科学的発見を行うプラットフォームとしての活躍を期待します。
<研究の背景と経緯>
多種多様な細胞の組成や構造、形態などと生理機能の関係を調べることは、生物学における主題の1つです。こうした細胞ごとの振る舞いの違いは、均一であるはずの細胞群からも観察されることから生命現象の理解を困難にしており、医療やバイオ産業の発展の妨げになっています。しかしながら従来の技術では、個々の細胞から得られる情報量と、解析可能な細胞数がトレードオフの関係となっており、多様な細胞を網羅的に研究するうえで限界となっていました。ImPACTプログラム「セレンディピティの計画的創出」では合田プログラムマネージャーが中心となり、この限界を突破するべく研究開発を進めていました。
<研究の内容>
本研究では光学や電気工学、情報科学、機械工学、生物学、医学など多分野にまたがる専門家を結集して、大量な細胞集団に含まれる一つ一つの細胞を高速に撮像し、深層学習注4)など最先端の情報処理技術でそれらの画像をリアルタイムに判別して、細胞集団の中から特定の細胞を分取する基盤技術「Intelligent Image-Activated Cell Sorter」を確立しました(図1、動画1、動画2)。本技術は、免疫学、病理学、微生物学、分子生物学、遺伝学、再生医学、移植など多岐にわたる分野で基盤技術として活用されている高速細胞分取技術「Fluorescence-Activated Cell Sorter」(開発者のHerzenberg氏は本貢献により2006年に京都賞を受賞)に顕微イメージング活性化(Image-Activated)と深層学習(Intelligent)を融合することによる飛躍的な発展であります。
加えて、技術の汎用性を示す実験として、3マイクロメートルから30マイクロメートル程度の異なるサイズの種々の細胞の高速撮像、がん患者の血液中にわずかに含まれる循環がん細胞様細胞の画像による発見などの例を示しました(図2)。細胞を識別するアルゴリズムとしても、従来の画像処理アルゴリズムから最先端のコンボリューショナル・ニューラル・ネットワーク注5)まで幅広く対応可能であることもビーズや細胞を用いた実験で実証しました。
さらに本技術の実用的な展開として、光合成やバイオ燃料の研究に使われる緑藻類クラミドモナス注6)と血液中に含まれる血小板を1秒間に約100回のスピードで撮像・判別・分取できることを示しました。そして、クラミドモナスの実験においては、20万個以上の細胞の中に1%程度含まれる希少な遺伝子変異を引き起こした細胞を分取・培養することに成功しました(図3)。また、血小板の実験においては、血小板の複数の形態を見分けて血液中に含まれる凝集血小板注7)を分取する実験に成功しました(図4)。これにより、本技術の実用性と有効性が示されました。
<今後の展開>
本研究で開発した装置は分子生物学、微生物学、医学、薬学など基礎研究の発展に寄与し、さらに医療やバイオ産業などへの社会実装を加速することを目指して、国内外の研究者に広く活用していただくためにオープン利用展開を始めました(http://www.goda.chem.s.u-tokyo.ac.jp/intelligentIACS)。さらに、本研究で開発した技術をより多くの方々に広くご利用いただくことを目標として、関連技術の事業化を進めるために株式会社CYBO(https://www.cybo.jp/)をImPACT発ベンチャーとして設立しました。
この新たな基盤技術により、これまで膨大な時間や手間がかかり偶然の幸運な発見「セレンディピティ」が必要とされていた事象が計画的に発見できるようになると期待されます。そして、従来の細胞計測技術では検出・分取できなかった細胞を分取して解析することで、生命科学分野におけるさまざまな発見やバイオ産業や医療分野での開発が大きく発展すると期待されます(図5)。
<付記>
本研究チームは、新田 尚(東京大学 大学院理学系研究科 客員研究員)、杉村 武昭(東京大学 大学院理学系研究科 客員研究員)、磯崎 瑛宏(東京大学 大学院理学系研究科 特任研究員)、三上 秀治(東京大学 大学院理学系研究科 助教)、平木 敬(東京大学 大学院情報理工学研究科 名誉教授)、佐久間 臣耶(名古屋大学 大学院工学研究科 助教)、飯野 敬矩(東京大学 大学院工学系研究科 主任研究員)、Dino Di Carlo(カリフォルニア大学 ロサンゼルス校工学部 バイオエンジニアリング学科 教授)、細川 陽一郎(奈良先端科学技術大学院大学 先端科学技術研究科 教授)、上村 想太郎(東京大学 大学院理学系研究科 教授)、小関 泰之(東京大学 大学院工学系研究科 准教授)、合田 圭介(東京大学 大学院理学系研究科 教授)、他39名で構成されています。
<添付資料>
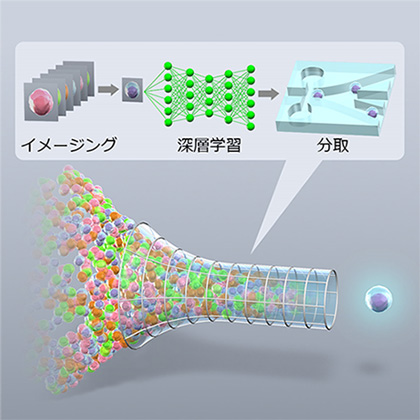
図1 本研究で開発したIntelligent Image-Activated Cell Sorterの模式図
大規模な細胞集団に含まれる一つ一つの細胞を高速に撮像し、深層学習など最先端の情報処理技術でそれらの画像をリアルタイムに判別して、細胞集団の中から特定の細胞を分取します。
動画1 本技術の機能
超高速蛍光イメージング技術、10ギガビットイーサーネットによる高速データ処理システム、マイクロ流体技術を活用した高速分取技術や細胞制御技術など、複数分野にまたがる異分野融合により実現しました。
動画2 本技術の運用
異分野融合による専門家チームにより運用しています。
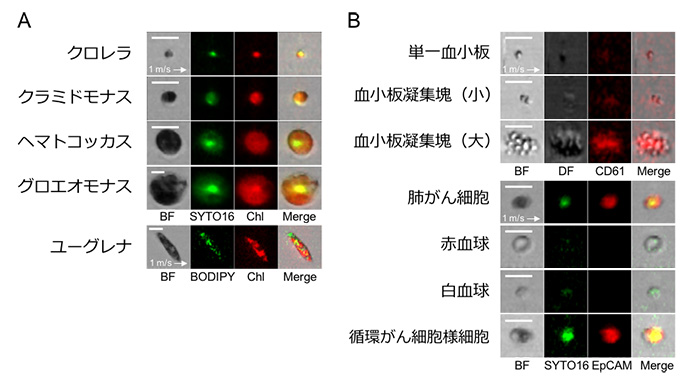
図2 本技術の汎用性実証のための撮像例
3マイクロメートルから30マイクロメートル程度にわたるさまざまな大きさや形の異なる細胞を高速撮像しました。
- A.微細藻類の観察。
- B.血液に含まれる細胞の観察。BFは明視野、SYTO16は核染色による蛍光、BODIPYは油滴染色による蛍光、Chlはクロロフィルの自家蛍光、DFは暗視野、CD61は血小板表面染色による蛍光、EpCAMはがん細胞表面染色による蛍光のイメージを示します。循環がん細胞様細胞はがん患者の血液から撮像しました。
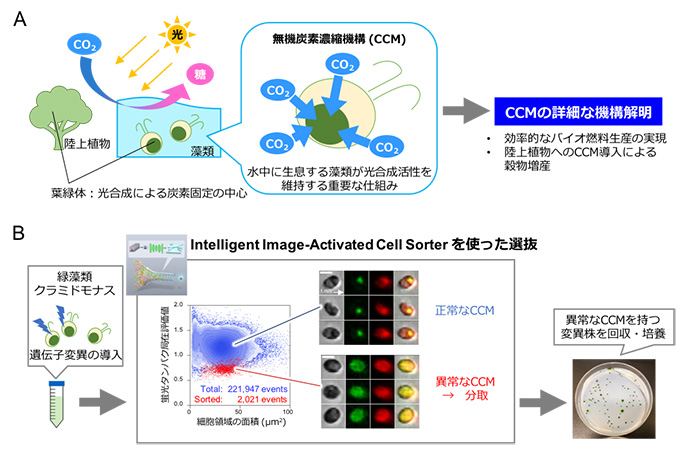
図3 緑藻類クラミドモナスを用いた本技術の微生物学への展開
- A.葉緑体はあらゆる光合成生物における炭素固定の中心です。水中に生息する藻類では、葉緑体中のルビスコ(CO2固定酵素)注8)へCO2を濃縮する無機炭素濃縮機構(CCM)注9)が、高い光合成効率を維持するために重要な役割を果たしています。この機構の解明は、藻類による効率的なバイオ燃料生産の実現のみならず、陸上植物へCCMを導入することによる穀物生産の増大などに寄与すると期待されます。
- B.20万個以上の藻類細胞クラミドモナスの中に1%程度含まれる希少な遺伝子変異を引き起こした細胞を分取・培養することに成功し、分取装置としての実用性と有効性を示しました。得られた変異株を詳細に解析することで、CCMの分子機構の解明が進むと期待されています。
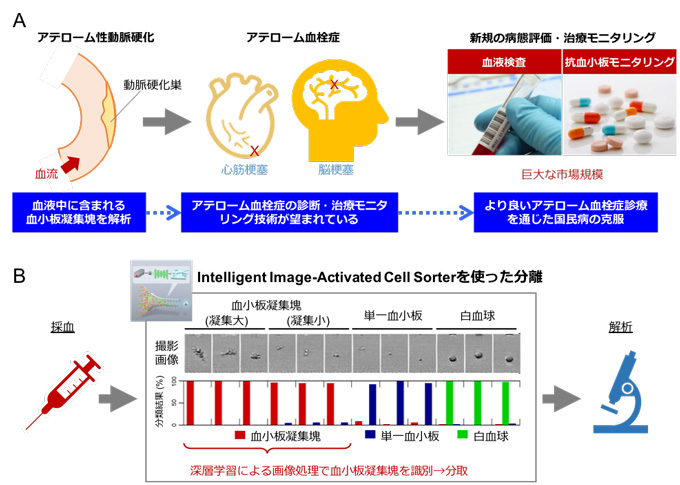
図4 血液細胞を用いた本技術の医学への展開
- A.血小板凝集塊は心筋梗塞や脳梗塞を含むアテローム血栓症に関連するバイオマーカーとして期待されており、その高精度な定量や詳細解析はアテローム血栓症の診断・治療モニタリング技術の開発につながる可能性があります(臨床診断への応用)。
- B.本研究では細胞画像の解析に深層学習を応用することで、血液中に含まれる血小板凝集塊を単一血小板や白血球などから高精度に識別し、さらにその識別をリアルタイムで行うことで血小板凝集塊を分取・濃縮することに成功しました。分取したサンプルのオミックス解析などを通じて病態生理の解明が進むと期待されます。

図5 今後の展望
開発した装置のオープン利用とベンチャー事業化を進めており、本基盤技術の活用が広く進むことで、幅広い分野の基礎科学の発展やバイオ産業、医療などの発展に大きく寄与するものと期待されます。
<用語解説>
- 注1)超高速蛍光イメージング技術
- 情報通信技術を用いて共焦点蛍光顕微鏡に応用することで、従来よりも桁違いに高速に生体試料の撮像する技術。平成30年1月30日に本研究グループよりプレスリリースしている。
- https://www.jst.go.jp/pr/announce/20180130/
- 注2)10ギガビットイーサーネット
- コンピューター間で1秒間に約10ギガビットのデータを送信できる極めて高速な通信規格。
- 注3)マイクロ流体技術
- マイクロ加工技術を用いて数マイクロメートル~数百マイクロメートル程度の微細な流路構造を形成し、その流路内に流す液体の挙動を制御する技術。インクジェットプリンターや診断装置などに応用されている。
- 注4)深層学習
- 機械学習手法の1つで多層のニューラルネットワークを用いて学習する。近年、急速に発展しており、画像や音声、自然言語などの問題に対し高い能力を示すようになった。ディープラーニングとも言う。
- 注5)コンボリューショナル・ニューラル・ネットワーク
- 深層学習の1つで、畳み込みニューラルネットワークとも言う。画像を複数のカテゴリに分類する用途などで活用が進められている。
- 注6)クラミドモナス
- 光合成、鞭毛運動、バイオ燃料などの基礎研究のモデル生物として世界中で使われている単細胞緑藻。和名はコナミドリムシ。
- 注7)凝集血小板
- 血小板は活性化されると凝集反応を起こし、凝集塊を形成する。心筋梗塞、脳梗塞の基盤となるアテローム血栓症には血小板活性化が大きく関与し、抗血小板療法がその治療の中心となっている。凝集血小板の検出が、アテローム血栓症の診断的応用につながることが期待される。
- 注8)ルビスコ(Rubisco)
- 地球上で最も多く存在するタンパク質と言われており、光合成の暗反応においてCO2を直接固定する酵素である。正式名はリブロース1,5-ビスリン酸カルボキシラーゼ/オキシゲナーゼ(ribulose 1,5-bisphosphate carboxylase/oxygenase)。
- 注9)無機炭素濃縮機構(CCM)
- 光合成に不利なCO2欠乏環境においても高い光合成活性を維持するために、積極的にCO2を細胞内に取り込み、葉緑体の中に濃縮する仕組み。
<論文情報>
| タイトル |
“Intelligent Image-Activated Cell Sorting” |
| 著者名 |
Nao Nitta, Takeaki Sugimura, Akihiro Isozaki, Hideharu Mikami, Kei Hiraki, Shinya Sakuma, Takanori Iino, Fumihito Arai, Taichiro Endo, Yasuhiro Fujiwaki, Hideya Fukuzawa, Misa Hase, Takeshi Hayakawa, Kotaro Hiramatsu, Yu Hoshino, Mary Inaba, Takuro Ito, Hiroshi Karakawa, Yusuke Kasai, Kenichi Koizumi, SangWook Lee, Cheng Lei, Ming Li, Takanori Maeno, Satoshi Matsusaka, Daichi Murakami, Atsuhiro Nakagawa, Yusuke Oguchi, Minoru Oikawa, Tadataka Ota, Kiyotaka Shiba, Hirofumi Shintaku, Yoshitaka Shirasaki, Kanako Suga, Yuta Suzuki, Nobutake Suzuki, Yo Tanaka, Hiroshi Tezuka, Chihana Toyokawa, Yaxiaer Yalikun, Makoto Yamada, Mai Yamagishi, Takashi Yamano, Atsushi Yasumoto, Yutaka Yatomi, Masayuki Yazawa, Dino Di Carlo, Yoichiroh Hosokawa, Sotaro Uemura, Yasuyuki Ozeki, and Keisuke Goda*
(*責任著者) |
| DOI |
10.1016/j.cell.2018.08.028 |
| アブストラクトURL |
https://doi.org/10.1016/j.cell.2018.08.028 |
<お問い合わせ先>
<研究に関すること>
合田 圭介(ゴウダ ケイスケ)
東京大学 大学院理学系研究科化学専攻 教授
〒113-0033 東京都文京区本郷7-3-1
Tel:03-5841-4329
E-mail:
<ImPACTの事業に関すること>
内閣府 革新的研究開発推進プログラム担当室
〒100-8914 東京都千代田区永田町1-6-1
Tel:03-6257-1339
<ImPACTプログラム内容およびPMに関すること>
科学技術振興機構 革新的研究開発推進室
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-6380-9012
E-mail:
<報道担当>
武田 加奈子 特任専門職員
大越 慎一 教授・広報室長
東京大学 大学院理学系研究科・理学部
Tel:03-5841-0654
E-mail:
名古屋大学 総務部総務課 広報室
Tel:052-789-2699
E-mail:
理化学研究所 広報室 報道担当
Tel:048-467-9272 Fax:048-462-4715
E-mail:
京都大学 総務部 広報課 国際広報室
Tel:075-753-5729 Fax:075-753-2094
E-mail:
加藤 裕幹
中央大学 研究支援室
Tel:03-3817-1603
E-mail:
九州大学 広報室
Tel:092-802-2130 Fax:092-802-2139
E-mail:
公益財団法人 がん研究会
担当:広報部 本山
Tel:03-3570-0775
E-mail:
東北大学病院 広報室
Tel:022-717-7149
E-mail:
高知大学 総務部 総務課 広報
Tel:088-844-8759・8100・8643 Fax:088-844-8033
E-mail:
奈良先端科学技術大学院大学 企画・教育部 企画総務課 広報渉外係
Tel:0743-72-5026
E-mail:
橋本 絵里香
株式会社エクサウィザーズ 広報担当
Tel:03-5860-1013
E-mail:
科学技術振興機構 広報課
Tel:03-5214-8404
E-mail: