ポイント
- 新規蛍光色素により、生体内のpHをリアルタイムに測定する技術を開発した。
- 蛍光色素が吸収する光や蛍光の波長を調節でき、細胞内の小器官から腫瘍といった生体組織に至るまでpHを測ることに成功した。
- がんや自己免疫疾患など、生体内pHの異常に関わる病気のメカニズムの解明や病態診断への応用が期待される。
細胞は取り込んだたんぱく質や有機物質の代謝、細胞構成成分の合成、輸送など、さまざまな生化学反応を調整して、生命機能を維持しています。これらの生化学反応を効率良く行うために細胞内には多くの異なった小器官注1)が存在し、それぞれ種々の生化学反応に最適な固有のpHを維持しています。臓器レベルでも生体内のpHは維持されている一方、pHの異常はさまざまな疾患につながります。そのため、生体内のpHの観察技術は、疾患メカニズムの解明や疾患の診断といった、基礎生命科学と臨床医療の両面でとても重要です。
東京大学 大学院薬学系研究科の花岡 健二郎 准教授、浦野 泰照 教授の研究グループは、細胞内小器官から生体内の臓器に至るまで、生きたまま蛍光注2)でpHを測定する新たな蛍光色素群を開発しました。細胞内や生体内の特定の部位に集まる物質を蛍光色素に結合させ、生きた細胞に添加したり動物の血液中へ投与することで見たい部位へと蛍光色素を送りpHの測定を行います。今までの蛍光色素は内部が酸性の小器官でのpHの測定は難しく、また光の照射によって徐々に色素が壊れ蛍光が弱まるため、長時間の観察が困難でした。今回開発した蛍光色素は光の照射による色素の崩壊が遅く、長時間の測定が可能になりました。さらに、酸性から中性にかけてオーダーメイドで見たいpHに適した蛍光色素に作り変えられるので、生きた状態でさまざまな細胞や臓器のpHを測ることができます。
本技術は、観察する生体への遺伝子導入を必要とすることなくpHの測定ができるため、多種類の生体での観察が可能です。これまでに、内部が酸性の小器官であるリソソームや、鉄輸送たんぱく質が細胞の外から細胞内に輸送される際の周辺のpHの変化を観察することに成功しました。マウスの観察では、開発した蛍光色素を静脈内へ投与し、腎臓内や皮下腫瘍モデルマウスで腫瘍内のpHを測定することに成功しました。
今回開発した蛍光色素群を用いることで、臓器内のpHや細胞内小器官のpHをこれまでより簡便かつ正確、リアルタイムに測定することができ、がんの画像診断への応用だけでなく、pHの異常が関与する疾患の解明およびそれに基づく薬の開発に貢献することが期待されます。
本研究成果は、2018年4月24日(米国東部夏時間)に米国化学会誌「Journal of the American Chemical Society」のオンライン版に公開されました。
本成果は、JST 研究成果展開事業 先端計測分析技術・機器開発プログラム 開発課題(新規近赤外蛍光団の開発と実用的蛍光プローブの創製(チームリーダー:花岡 健二郎))によって得られました。
<研究の背景と経緯>
細胞内の小器官は固有のpHを持ちさまざまな生化学反応を制御しているため、小器官に固有のpHを観察することは細胞内で起きている生命現象の理解につながります。また、体内のpHも高度に制御されており、骨代謝、がん細胞の浸潤などさまざまな生命現象に関わっていることから、生きた動物の体内でのpHを観察する技術は基礎生命科学や臨床医療の両面で重要です。現在、細胞内小器官のpHを測定する技術は、時間的にも空間的にも高い精度で検出できる蛍光イメージング法注3)が用いられていますが、これまでに使用されている蛍光色素は内部が酸性の小器官では蛍光の変化が小さく、pHの測定に適していませんでした。また、動物体内の臓器のpHの測定では、pH電極注4)やMRI注5)を用いた方法が報告されていますが、三次元的な情報を得ることの難しさや感度の低さに由来する測定時間の長さや造影剤注6)の大量投与を必要とするなどそれぞれ問題がありました。そこで、高い時空間分解能と感度、簡便性によってpHの観察を可能にする蛍光イメージングのための蛍光色素群を開発することを目指して、研究に着手しました。
<研究の内容>
これまでに蛍光色素群を合成し、それらの光学特性を詳しく調べた結果、酸性になることで蛍光性を保ったまま吸収波長が約80nmもの大きな短波長化を示す蛍光色素群を見いだしました(図1)。この蛍光色素群は、大きな吸収波長の変化を示すだけでなく、光の照射にも壊れにくい高い安定性を示しました。さらに、蛍光色素の化学構造を変化させることで、さまざまなpHの変化に対応して、蛍光色も深赤色から近赤外光に変化させることに成功しました。実際に、細胞内に取り込まれることでリソソームに集積することが知られている多糖類の一種であるデキストランに、開発した深赤色の蛍光色素を標識し、リソソーム内のpHの観察や、薬剤添加に伴うリソソーム内部のpHの中性化を観察することに成功しました(図2)。生体内でリソソームの内部のpHを酸性に保つことができなくなるとさまざまな疾患につながることが知られており、リソソームのpHを測定することは疾患のメカニズムの解明につながります。また、鉄輸送たんぱく質であるトランスフェリンに蛍光色素を標識することで、トランスフェリン受容体を介して細胞内に入り、その後、細胞膜へと戻るリサイクリングエンドソーム注7)へと迅速に輸送される過程のpHの変化を観察することにも成功しました(図3)。一方、近赤外光の蛍光を示す蛍光色素を、皮下腫瘍モデルマウスに静脈内投与し全身に分布させてから、周囲の組織に比べて腫瘍部位でのpHがどのくらい低下しているかを観察しました。その結果、正常部位のpHが7.3に対して腫瘍部位の平均pHは6.9と測定されました。さらに、腎臓のpHは6.4と観察されましたが、これは一般的な尿のpHの範囲にありました(図4)。
本研究の成果により、これらの蛍光色素群を用いて蛍光を観察することで、病気の診断や病気とpHの関わりを明らかにできる可能性が示唆されました。
<今後の展開>
開発したpH感受性の蛍光色素群は、生命現象に伴うpHの変化を高い時空間分解能で観察できるため、pHの関わるさまざまな生命現象の解明に貢献することが期待されます。また、体内の臓器レベルでも、例えば、腫瘍の酸性化を引き起こす要因は解糖系の活性化、その他のプロトン(H+)の輸送や代謝に関わる酵素が報告されていますが、これらの生体内での寄与はいまだ明らかではなく、本蛍光色素を用いることでこれらの要因が腫瘍の酸性化にどのように寄与しているかを明らかにできます。
今後、基礎生命科学におけるpHの役割を明らかにするための有用なツールや、臨床医療でも病気の診断の新たな技術となり、基礎研究と臨床医療の両面において、その進展に貢献することが期待されます。
<参考図>
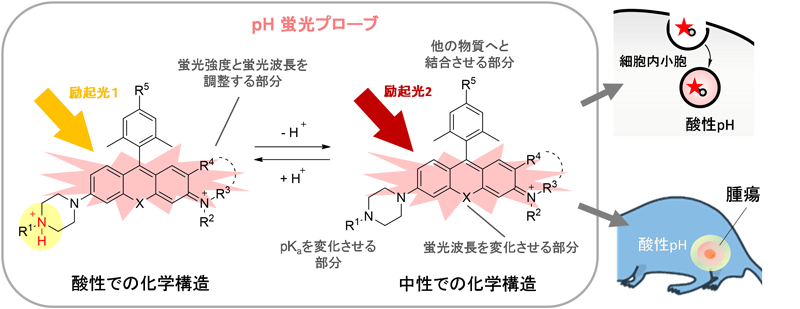
図1 開発したpHを測定できる蛍光プローブ群の化学構造
深赤色から近赤外光に蛍光波長を示す蛍光色素群の化学構造に、pKa(酸性度)の調節部分、蛍光波長の調節部分、他の物質へと結合させる部分があり、観察したい生体サンプルに合わせて、これら化学構造を最適化することができる。酸性条件下では、プロトン(H+)が結合することで、吸収する波長が約80nm短くなる。
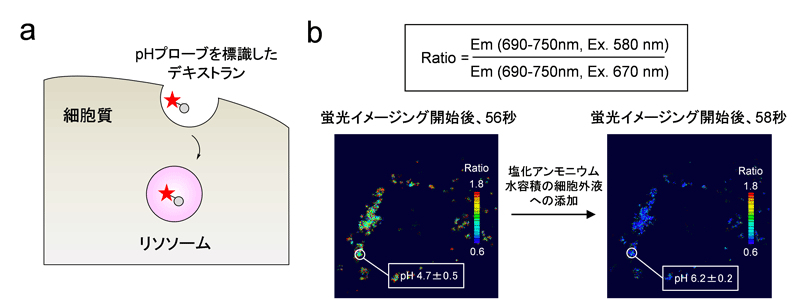
図2 細胞内小器官であるリソソーム内のpHの変化の測定
MEF細胞(マウス胚線維芽細胞)にpHプローブを取り込ませ(a)、リソソームに集積させた後、蛍光イメージングを行った。蛍光イメージングの開始後56秒に、塩化アンモニウム水溶液を細胞外液に添加し、リソソーム内のpHの中性化を観察することに成功した(b)。
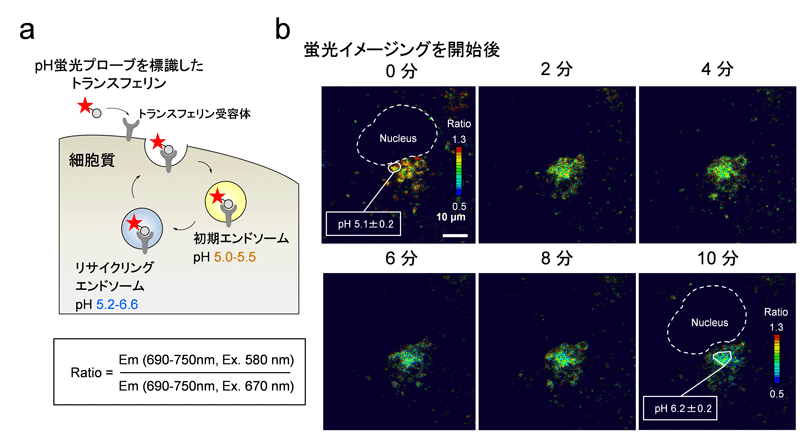
図3 リサイクリングエンドソーム内のpHの変化
COS-1細胞(サル腎線維芽細胞)に、pHプローブを標識した鉄輸送たんぱく質であるトランスフェリンを取り込ませ、初期エンドソームからリサイクリングエンドソームまで蛍光プローブが標識されたたんぱく質を輸送させた(a)。4℃から37℃へと細胞の環境を変化させると共に蛍光イメージングを開始し、10分間、連続的にpHの変化を観察した。初期エンドソームからリサイクリングエンドソームへと輸送されることに伴うpHの変化を観察することに成功した(b)。
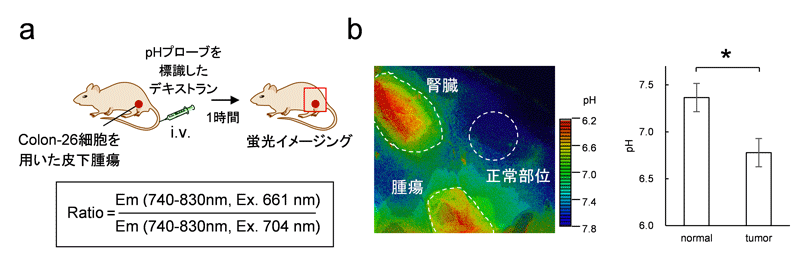
図4 腫瘍内のpHの測定
近赤外光の蛍光を示す蛍光プローブを標識したデキストランをヌードマウスの尾静脈より投与し、その1時間後に腫瘍周辺の蛍光イメージングを行った(a)。その結果、腫瘍部位での弱酸性化を観察することに成功した(b)。また、正常部位では中性を示した一方で、腎臓では弱酸性であることが確認された(b)。
<用語解説>
- 注1)小器官
- 細胞内の構造で、膜で囲まれて一定の機能を持つもので、ミトコンドリアや小胞体、リソソーム、ゴルジ体、核などがあげられる。
- 注2)蛍光
- 紫外線や可視光線といった光が照射されることで、そのエネルギーを吸収し、分子(蛍光色素)が励起状態となり、それが基底状態に戻る際に放出される光のこと。
- 注3)蛍光イメージング法
- 目的とする分子だけを蛍光で光らせて、蛍光顕微鏡を用いて観察するもの。
- 注4)pH電極
- pHを測るセンサー(電極)のこと。
- 注5)MRI
- Magnetic resonance imaging(磁気共鳴画像)の略語で、磁場とラジオ波を利用して、生体のあらゆる断面の画像を得ることができる撮影技術のこと。
- 注6)造影剤
- 画像診断の画像をより明確にするために用いる薬剤のこと。
- 注7)リサイクルエンドソーム
- 細胞膜から取り込まれた物質が再び細胞膜へとリサイクルされる際に通過するオルガネラ(小器官)のこと。
<論文情報>
| タイトル |
“Development of a Series of Practical Fluorescent Chemical Tools to Measure pH Values in Living Samples” |
| 著者名 |
Shodai Takahashi, Yu Kagami, Kenjiro Hanaoka, Takuya Terai, Toru Komatsu, Tasuku Ueno, Masanobu Uchiyama, Ikuko Honda, Noboru Mizushima, Tomohiko Taguchi, Hiroyuki Arai, Tetsuo Nagano, and Yasuteru Urano |
| doi |
10.1021/jacs.8b00277 |
<お問い合わせ先>
<研究に関すること>
花岡 健二郎(ハナオカ ケンジロウ)
東京大学 大学院薬学系研究科 薬品代謝化学教室 准教授
〒113-0033 東京都文京区本郷7-3-1
Tel:03-5841-4852 Fax:03-5841-4855
E-mail:
<JSTに関すること>
科学技術振興機構 産学連携展開部 先端計測グループ
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3529
E-mail:
<報道担当>
東京大学 薬学部・薬学系研究科 庶務チーム
〒113-0033 東京都文京区本郷7-3-1
Tel:03-5841-4719 Fax:03-5841-4711
E-mail:
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: