ポイント
- オリゴ糖とポリプロピレングリコールからなる両親媒性ポリマーが、物質透過性を示す糖鎖高分子ベシクルを形成することを初めて明らかにした。
- 酵素を封入させた糖鎖高分子ベシクルは、血中投与によりがん組織周囲に集まり、その場で酵素反応により抗がん剤を合成、放出する医療用ナノデバイス(ナノファクトリー)として機能し、抗腫瘍効果をもたらすことをマウスで明らかにした。
- 疾患部位で薬を合成する技術は、より優れた治療効果、低い副作用をもたらす医療技術につながることが期待される。
JST 戦略的創造研究推進事業において、京都大学 大学院工学研究科の西村 智貴 特定研究員、秋吉 一成 教授の研究グループは、物質透過性注1)を持つ糖鎖高分子ベシクル注2)を新たに開発し、がん組織周囲でプロドラッグ注3)を抗がん剤へと変換できる酵素封入型ナノデバイス(ナノファクトリー注4))として機能することを見いだしました。
リン脂質からなるリポソーム注5)や両親媒性ポリマー注6)からなるベシクルは、酵素反応場としての応用が進められています。しかし、これらの分子集合体は、極めて物質透過能が低いことが知られており、酵素基質を外部から供給できないため、長期的に酵素反応を進行させることができませんでした。
本研究グループは、糖鎖とポリプロピレングリコールからなる両親媒性ポリマーが形成する糖鎖高分子ベシクルが、分子量の違いによって選択的に物質透過性を示すことを発見し、また、酵素を安定に封入し、内部に安定に保持できることを明らかにしました。この酵素封入ベシクルは、外部から基質を内部の酵素に供給でき、酵素反応生成物を外部に放出できる機能を持つことを見いだしました。さらに、このベシクルは血中投与により生体内のがん組織周囲に集まり、プロドラッグを抗がん剤へと変換し、優れた抗腫瘍効果を示すことをマウスで実証しました。
今回開発した糖鎖高分子ベシクルにより、様々な酵素を用いて長期的に酵素反応を進行させる技術につながると期待されます。また、従来のドラッグデリバリーシステム注7)が抱えていた、がん組織以外への副作用を解決するだけではなく、より優れた治療効果をもたらす新たながん治療に役立つことが期待されます。
本研究成果は、2017年7月17日に独科学誌『Advanced Materials』のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
JST 戦略的創造研究推進事業 総括実施型研究(ERATO)
| 研究プロジェクト |
「秋吉バイオナノトランスポータープロジェクト」 |
| 研究総括 |
秋吉 一成(京都大学 大学院工学研究科 教授) |
| 研究期間 |
平成23年10月~平成29年3月 |
<研究の背景と経緯>
リン脂質からなるリポソームやポリマーからなるポリマーベシクルは、内水相注8)を持つ中空状の集合体として知られています。生体内の細胞やオルガネラのように内水相空間に酵素などの生体高分子を封入することが可能で、酵素反応場やドラッグデリバリーシステム(DDS)における酵素キャリア、さらには人工細胞モデルとして応用研究が進められています。しかし、リポソーム、ポリマーベシクルのいずれも、物質の透過能が著しく低いという欠点があります。そのため、内包された酵素基質やエネルギー源が枯渇すると反応が停止し、長期的に反応を進行させることが困難でした。従って、ポリマーベシクルなどの中空状集合体を酵素反応場として利用する上で、透過能の付与は大きな課題でした。
<研究の内容>
(1)物質透過性高分子ベシクルの開発
本研究グループは、新たにオリゴ糖とポリプロピレングリコールからなる両親媒性ポリマーを設計しました(図1A)。このポリマーは、水溶液中で自発的に分子が集合し、糖鎖高分子ベシクルを形成することを電子顕微鏡観察(図1B)および放射光X線小角散乱測定注9)(図1C)から明らかにしました。また、この糖鎖高分子ベシクルは、分子量の大きなタンパク質・酵素などは内水相に保つことができ、低分子量の化合物は二分子膜を透過する“物質透過性”を持つことを見いだしました。
(2)基質を外部から供給し得る酵素反応場として機能
高分子ベシクルが持つ物質透過性を利用すれば、新たに開発した高分子ベシクルは、外部から基質を供給できる酵素反応場として機能します。実際に、モデル酵素であるβ-ガラクトシダーゼをベシクルに内包させ、加水分解されると蛍光を示す基質を外部から添加すると、基質が二分子膜を透過し、内水相にあるβ-ガラクトシダーゼによって加水分解を受け、蛍光を示すことが分かりました(図2)。この酵素反応場としての機能は、β-ガラクトシダーゼに限らず、生化学実験で汎用的に用いられるα-キモトリプシンやペルオキシダーゼなどの酵素にも適応できるうえ、緩衝液中のみならず、より夾雑な環境下である細胞内でも保たれています。
(3)酵素搭載型新規治療用ナノファクトリーとして機能
従来の抗がん剤治療は、がん組織のみならず正常組織にも作用するため、極めて強い副作用をもたらします。従って、抗がん剤治療において副作用の低減は、喫緊の課題です。そこで、物質透過性高分子ベシクルが持つ酵素反応場としての機能を利用して、がん組織周囲で抗がん剤を合成することに応用しました。がん組織を移植した担がんマウス注10)に、酵素内包高分子ベシクルを投与すると、ベシクルががん組織周囲に集積します。その後、抗がん剤であるドキソルビシンのプロドラッグを投与すると、がん組織周囲に集積していた酵素内包高分子ベシクルが、プロドラッグをドキソルビシンへと変換し、優れた抗腫瘍効果をもたらしました(図3)。また、体重減少や臓器毒性などの副作用も検出されないことも分かっています。このことから、今回開発した高分子ベシクルは、薬物をがん組織周囲で合成、放出し得る酵素搭載型新規治療用ナノファクトリー(Bio-transporting Nanofactory)として機能することを明らかにしました。ナノファクトリーによる治療の概念は、2007年のNature nanotechnology誌で他の研究者グループから提案されていましたが、これまで実際にナノファクトリーとして機能する材料の報告はなく、今回開発した高分子ベシクルが世界で初めてナノファクトリーを実現した材料となります。
<今後の展開>
本研究では、オリゴ糖とポリプロピレングリコール鎖からなる両親媒性ポリマーが、物質透過性を持つ高分子ベシクルを形成することを初めて見いだしました。通常の高分子ベシクルは、物質透過性を全く示さないことから、今回開発した高分子ベシクルは、新たな分子集合体として材料科学の発展に寄与することが期待されます。また、酵素は、食品、洗浄、診断薬、医薬品と幅広い分野で用いられています。本研究で開発した物質透過性を持つ高分子ベシクルを利用すれば、酵素をベシクルで保護することができ、酵素反応を長期・安定的に進行させる技術への応用が期待されます。さらに、内包させる酵素を変えることで、様々な基質に対応でき、がんのみならず様々な疾患に対して有効な治療法の開発にもつながると期待できます。
<参考図>
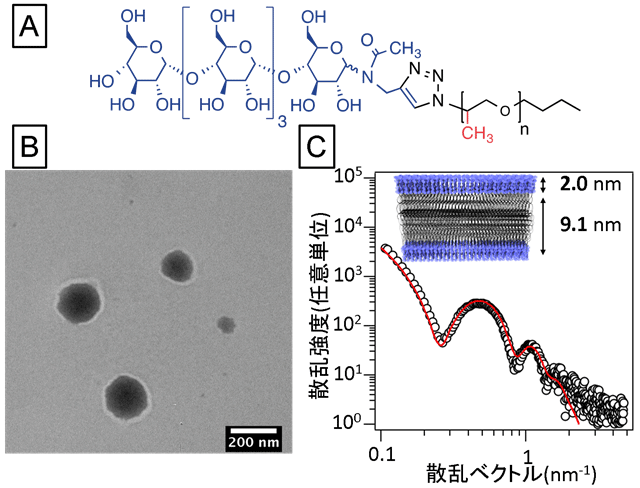
図1
- (A)糖鎖-ポリプロピレングリコールからなる両親媒性ポリマーの化学構造式
- (B)糖鎖高分子ベシクルの電子顕微鏡像
- (C)高分子ベシクルの小角X線散乱プロファイルと二分子膜の模式図
高分子ベシクルの電子顕微鏡観察から、150nm程度の粒子が観察された。小角X線散乱測定で得られたプロファイル(黒丸)は、二分子膜モデル(赤線)で記述でき、二分子膜の厚みが13nm程度であることが分かった。
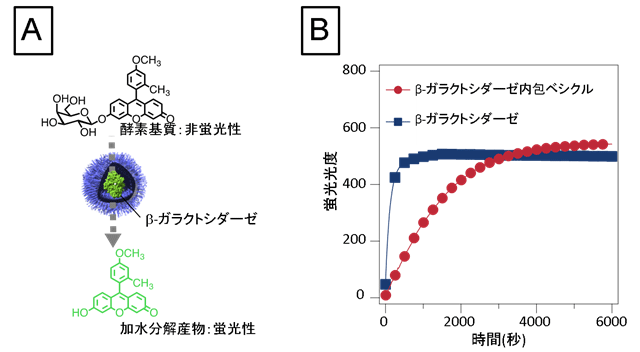
図2
- (A)β-ガラクトシダーゼを内包した糖鎖高分子ベシクルからなる酵素反応場の模式図
- (B)酵素反応場内での蛍光性基質の加水分解挙動
β-ガラクトシダーゼを内包した高分子ベシクルに酵素基質を添加すると、加水分解産物由来の蛍光強度が増大し(赤丸)、基質を外部から供給できる酵素反応場として機能することが判明した。
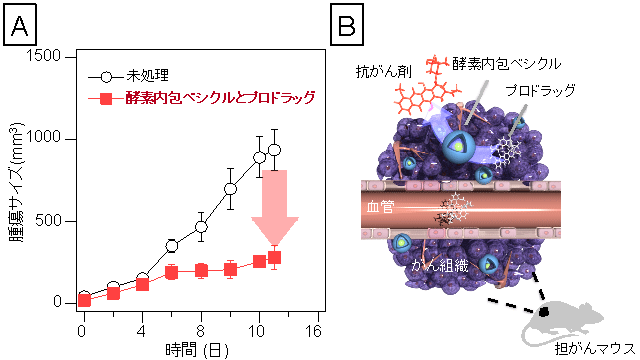
図3
- (A)酵素内包ベシクルとプロドラッグによる抗腫瘍効果
- (B)薬物をがん組織周囲で合成、放出し得る酵素搭載型新規治療用ナノファクトリー
(Bio-transporting Nanofactory)の概念図
酵素内包ベシクルとプロドラッグを組み合わせた治療は、優れた抗腫瘍効果をもたらすことを見いだした。
<用語解説>
- 注1) 物質透過性
- ベシクルの膜が分子を透過させる性質
- 注2) 糖鎖高分子ベシクル
- 糖鎖修飾両親媒性ポリマーが、自発的に集合して球状に閉じた膜構造を持つ中空状集合体
- 注3) プロドラッグ
- 生体内で代謝されることにより薬効を現すような化学構造をした薬剤
- 注4) ナノファクトリー
- 生体内の疾患部位で、薬を産生または、不要な物質を分解・代謝するナノデバイスで、2007年のNature Nanotechnology誌で提案された概念
- 注5) リポソーム
- 脂質人工膜の一種で、リン脂質が、水溶液中で自発的に集合し球状に閉じた中空状集合体
- 注6) 両親媒性ポリマー
- 親水性のセグメントと疎水性のセグメントが1本のポリマー中で結合した化合物
- 注7) ドラッグデリバリーシステム
- 薬剤を患部に選択的に送達することで、副作用を低減しながら治療効果を高める医療技術
- 注8) 内水相
- リポソームやベシクルが持つ、溶媒で満たされた内部空間
- 注9) 放射光X線小角散乱測定
- SPring-8やあいちシンクロトロン光センターなどの放射光施設から生み出される高輝度のX線を用いて、散乱角が数度以下の散乱X線を観察することにより、分子集合体のナノスケールの構造情報を得る手法
- 注10) 担がんマウス
- がん組織を皮下などに移植したマウス
<付記>
放射光X線小角散乱による分子集合体の構造解析には、あいちシンクロトロン光センター BL8S3およびSPring-8 BL40B2の最先端設備が活用されています。
<論文情報>
| タイトル |
“Bio-transporting Self-assembled Nanofactories using Polymer Vesicles with Molecular Permeability for Enzyme Prodrug Cancer Therapy”
(物質透過性高分子ベシクルからなる酵素搭載型自己組織化ナノファクトリーによる酵素プロドラッグ療法) |
| 著者名 |
Tomoki Nishimura, Yoshihiro Sasaki, Kazunari Akiyoshi |
| doi |
10.1002/adma.201702406 |
<お問い合わせ先>
<研究に関すること>
秋吉 一成(アキヨシ カズナリ)
京都大学 大学院工学研究科 高分子化学専攻 教授
〒615-8510 京都府京都市西京区京都大学桂
Tel:075-383-2589 Fax:075-383-2590
E-mail:
<JST事業に関すること>
古川 雅士(フルカワ マサシ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail:
<報道担当>
京都大学 総務部 広報課
〒606-8501 京都府京都市左京区吉田本町
Tel:075-753-2071 Fax:075-753-2094
E-mail:
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: