ポイント
- 人間生活にとって有用であると同時に有害ともなりうるカビが菌糸と呼ばれる細胞を伸ばし続けて成長する仕組みを解明しました。
- 判明した仕組みは、一歩一歩を繰り返して伸び続けるというものでした。
- カビの伸びる仕組みを理解し制御することは、醸造・発酵、抗生物質・有用酵素生産などの産業分野に貢献し、農業・医学分野での農薬・抗菌剤の開発につながることが期待されます。
筑波大学 生命環境系 国際テニュアトラック助教 竹下 典男(研究実施時、ドイツのカールスルーエ工科大学 応用微生物学科 グループリーダー兼任)らの研究グループは、カビが伸び続ける仕組みを解明しました。
カビは食品や医薬品の生成において有用であると同時に、医学、保健、農業分野などで有害な存在でもあります。本研究では、このようなカビの有用性と病原性を特徴付ける菌糸の伸びる仕組みを、超解像顕微鏡注1)を含む蛍光イメージング技術により明らかにしました。
具体的には、菌糸細胞が先端を伸ばす際、菌糸先端でのアクチン注2)の重合化、酵素の分泌、細胞の伸長が周期的に起きること、そして細胞外からのカルシウムイオンの一時的な取り込みも周期的に起き、上記のステップを同調させ制御していることを明らかにしました。すなわち、一見、菌糸細胞が一定のスピードでスムーズに伸びているようですが、そうではなく、いくつかの段階的なステップを周期的に繰り返すことで、細胞を徐々に伸ばし続けていることが明らかとなりました。
カビの伸びる仕組みを理解し制御することは、醸造・発酵、抗生物質・有用酵素生産などの産業分野に貢献し、農業・医学分野における農薬・抗菌剤の開発にもつながる可能性があります。
本研究は、カールスルーエ工科大学 応用微生物学科 Reinhard Fischer 教授、同大学 応用物理学科 Ulrich Nienhaus 教授、筑波大学 生命環境系 高谷 直樹 教授らの協力を得て行いました。
本研究の成果は、米国科学アカデミー紀要(PNAS)オンライン版で2017年5月15日(米国東部時間、日本時間16日)付で公開される予定です。
本研究は、科学技術振興機構(JST) 戦略的創造研究推進事業 総括実施型研究(ERATO)「野村集団微生物制御プロジェクト」の一環で行われました。
<研究の背景>
カビ(糸状菌)は、その名の通り糸状の菌糸からなり、菌糸がその先端を伸長させることで成長します。カビは、環境中に数多く存在する微生物であると同時に、菌糸という細胞を伸ばし続けることで、地球上最大の生き物となる潜在能力をもっています注3)。特に土壌中では、カビは最多種・最大体積の生き物であると考えられています。カビは伸びる際に多くの酵素を出して有機物を分解しており、その分解者としての役割は生態系の物質循環に必要です。我々の身近には、パンに生えるもの、浴室に生えるもの、コウジカビのように伝統的な発酵食品(酒・醤油・味噌など)の生産に関わるもの、有用酵素や抗生物質の生産などバイオ産業で利用されるものなど様々なカビが存在しています。その一方で、免疫不全を来たした人間や農作物の細胞に侵入して病原性を示すことで甚大な被害をもたらすものもあり、医学・農業分野で大きな問題となっています。
細胞は均一な球体ではなく、一般に不均等な形状をしています。これは、広い意味で細胞の極性と呼ばれており、様々な細胞の機能に必須の性質です。極性に従った成長により、機能に適した細胞の形が作られます。カビの菌糸は常に極性をその先端に維持して伸びることから、極性と細胞の形との関わりを解析するのに適したモデルです。また、カビの高い酵素分泌能や病原性は、菌糸の生育と密接に関連しているため、菌糸が伸び続ける仕組みの解明を目指しました。
本研究では、古くから遺伝学の研究対象とされ、分子生物学的手法が整備されたカビ(糸状菌)のモデル生物であるAspergillus nidulans(アスペルギルス ニドゥランス)を用いて、菌糸が伸びる仕組みを解析しました。このカビは、産業上重要なコウジカビAspergillus oryzae(アスペルギルス オリゼー)や日和見感染症のアスペルギルス症の病原菌Aspergillus fumigatus(アスペルギルス フミガタス)などの近縁種です。
<研究の内容と成果>
菌糸細胞が伸びるために必要な膜の成分やタンパク質は、菌糸先端から合成されるアクチンケーブルに沿った分泌小胞の輸送によって、菌糸先端に供給されます。重合化したアクチン、分泌小胞をそれぞれ緑色または赤色蛍光タンパク質で標識し、蛍光顕微鏡で経時的にライブイメージングを行いました。その結果、それぞれの蛍光が菌糸先端で同調して強弱の変化を示しました。また、細胞内のカルシウムイオン(Ca2+)を、バイオマーカーであるR-GECOにより可視化することに成功し、カルシウムチャンネル依存的に、細胞内Ca2+の濃度の一時的な増加が周期的に観察されました。そして、Ca2+の流入と菌糸先端におけるアクチン重合と分泌小胞量の増減が、同調して周期的に起きることを明らかにしました。
以上の結果から、菌糸の伸長速度が一定ではなく、早い遅いを周期的に繰り返すことが示されました。菌糸伸長が遅い期間、つまりエキソサイトーシス注4)の活性が低い時、菌糸先端でアクチンが重合化し、分泌小胞が蓄積します。そこに一時的なCa2+の流入が生じて細胞内のCa2+濃度が上昇すると、菌糸先端のアクチンの脱重合や、分泌小胞と細胞膜の融合が促されます。結果的に、エキソサイトーシス活性が上昇し、菌糸が早く伸長するようになります。この一時的なエキソサイトーシスの活性化で、菌糸が早く伸長した後、分泌小胞量が減少し、再び菌糸の伸長速度が低下します。その後、再びアクチンが重合化し、分泌小胞が蓄積します。そして、一時的なCa2+の流入により、サイクルが進行すると考えられます。
Ca2+チャンネルの活性が、局在する膜の伸張(張力)により活性化されることが知られていることから、菌糸の伸長が遅い時、細胞内の膨圧が徐々に上昇し、その結果、Ca2+チャンネルを活性化し、一時的なCa2+の流入を促すことが予想されます。このような周期的・段階的な細胞伸長は、化学・物理的な細胞内外の刺激により素早く応答し、対応することを可能にするという生物学的な意義が考えられます。
<今後の展開>
カビの伸びる仕組みを理解しその制御が可能となれば、醸造・発酵食品分野での品質向上、抗生物質・有用酵素生産などのバイオ産業分野での生産量の向上、バイオマスを利用したバイオエネルギー分野の発展、農業・医学分野における農薬・抗菌剤の開発など、カビが関わる全ての幅広い分野に貢献することが期待されます。
<参考図>
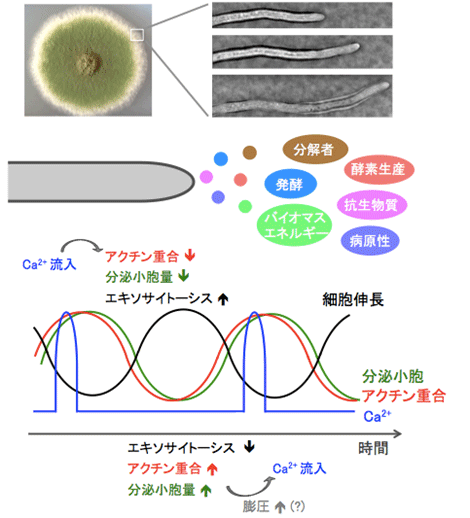
カビ(糸状菌)は大量の酵素を分泌し、菌糸を伸ばし続けることで成長します。カビは、有機物の分解者として、生態系の物質循環に必要であり、バイオマスを分解することでバイオエタノールの生産にも関わります。発酵食品・有用酵素・抗生物質の生産などバイオ産業で利用される一方で、人間や農作物の細胞に侵入して病原性を示すものもあります。本研究では、カビが伸びる仕組み(一歩一歩を繰り返して伸び続ける機構)を解明しました。周期的なCa2+の一時的な流入が、アクチン重合とエキソサイトーシスを同調させることで、周期的・段階的に一歩一歩、細胞を徐々に伸ばし続けています。
<用語解説>
- 注1) 超解像顕微鏡
- 本研究では、蛍光を一つずつ確率的に光らせる技術と、蛍光標識した分子の位置をナノメートルの精度で計測する技術を組み合わせることにより、光の回折限界(200-300ナノメートル)を超えた超解像顕微鏡法の一つであるPLAM (photoactivation localization microscopy、回折限界;20-50ナノメートル)を使用しています。超解像顕微鏡の開発者には、2014年にノーベル化学賞が与えられています。
- 注2) アクチン
- アクチンは多量体を形成してフィラメント状の構造を取る細胞骨格タンパク質です。多量体化した(重合化した)アクチンのフィラメントは、アクチンケーブルを形成し、細胞の形の決定や小胞の輸送に関わります。
- 注3) 世界最大の生き物は菌類
- 1998年にアメリカ、オレゴン州の東部で発見されたキシメジ科のキノコ、オニナラタケ(Armillaria ostoyae)の菌床は、総面積8.9平方キロメートル(890万平方メートル)に及び、推定重量はおよそ600トン、推定年齢は約2400歳といわれています。キノコもカビの仲間で、土や木の中に菌糸を作り成長します。地表に出ている胞子を作る器官(子実体)が、キノコと呼ばれるものです。
- 注4) エキソサイトーシス
- 分泌されるタンパク質などは、細胞内で合成された後、分泌小胞内に貯留されます。分泌小胞は、細胞質内を移動して細胞膜へと接近し、細胞膜と融合します。これにより、分泌小胞の内容物は細胞外へと放出されます。これをエキソサイトーシスと呼び、細胞膜と融合した小胞膜は、そのまま新たな細胞膜となります。
<論文情報>
| タイトル |
“Pulses of Ca2+ coordinate actin assembly and exocytosis for stepwise cell extension”
(Ca2+のパルスがアクチン重合とエキソサイトーシスを同調させることで、段階的に細胞が伸長する) |
| 著者名 |
Norio Takeshita*, Minoas Evangelinos, Lu Zhou, Tomoko Serizawa, Rosa A. Somera-Fajardo, Ling Lu, Naoki Takaya, G. Ulrich Nienhaus, Reinhard Fischer
(*責任著者)
|
| doi |
10.1073/pnas.1700204114 |
<お問い合わせ先>
<研究に関すること>
竹下 典男 (タケシタ ノリオ)
筑波大学 生命環境系 国際テニュアトラック助教
〒305-8572 茨城県つくば市天王台1-1-1 筑波大学総合研究棟A515
Tel:029-853-7191
E-mail:
URL:http://www.microbes.agbi.tsukuba.ac.jp/takeshita
<JST事業に関すること>
大山 健志(オオヤマ タケシ)
科学技術振興機構 研究プロジェクト推進部
Tel:03-3512-3528
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail:
(英文)“Mechanism that Coordinates Growth Spurts in Filamentous Fungi Revealed”