ポイント
- 体内に侵入してきたウイルス由来のRNAを感知して自然免疫応答を引き起こすToll様受容体7(TLR7)と呼ばれるタンパク質の立体構造を明らかにしました。
- TLR7が2か所の部位でウイルス由来のRNAと低分子リガンド注1)を同時に認識し、活性化される詳細な機構を明らかにしました。
- TLR7を標的としたワクチンアジュバント注2)やウイルス感染やアレルギーの治療薬などの設計につながることが期待されます。
東京大学 大学院薬学系研究科の清水 敏之 教授、張 志寛 大学院生、大戸 梅治 准教授、東京大学 医科学研究所の三宅 健介 教授、柴田 琢磨 助教、大阪大学 大学院工学研究科の内山 進 准教授、首都大学東京 理工学研究科の礒辺 俊明 教授、田岡 万悟 准教授らの研究グループは、微生物の侵入を感知して免疫系を活性化するTLR7タンパク質の詳細な立体構造を世界で初めて明らかにしました。
細菌やウイルスなどの病原体に対する感染防御機構として、自然免疫機構が備わっており、TLR受容体が主にその役割を担っています。TLR7はTLR受容体の1つで、ウイルス由来の一本鎖RNAまたは合成低分子リガンドを感知することで、インターフェロン注3)などの産生を促します。そのためTLR7は、抗ウイルス薬、ワクチン、抗がん剤などのターゲットとして注目されていましたが、リガンドを感知する具体的な機構は不明でした。
研究グループは、TLR7が、一本鎖RNA(polyU注4))と2種類の低分子リガンド(グアノシン注5)、loxoribine注6))のいずれか、あるいは低分子リガンドR848注7)に結合した複合体の立体構造を明らかにしました(図1)。その結果、TLR7はそれぞれのリガンドと2:2(または2:2:2)の複合体を形成することで、活性化型の2量体となることが明らかになりました。グアノシン、loxoribineおよびR848などの低分子リガンドは2量体の界面に位置する第1結合部位に、polyU一本鎖RNAはTLR7のリング型構造の凹面の第2結合部位に位置していました(図2)。構造解析と生化学的実験の結果、TLR7はこれらの2種類のリガンドによって協調的に活性化されることが明らかになりました。
これらの知見は、ワクチンアジュバントの開発やウイルス感染やアレルギーなどの治療薬の設計につながることが期待されます。
本研究は、JST 戦略的創造研究推進事業(CREST)、科学研究費補助金、公益財団法人武田科学振興財団助成金、公益財団法人持田記念医学薬学振興財団助成金、公益財団法人第一三共生命科学研究振興財団助成金などの外部資金支援を受けて行われたものです。
<発表内容>
細菌やウイルスなどの病原体に対する防御機構として、自然免疫機構が備わっています。TLR受容体は自然免疫系の受容体であり、病原体の持つ特定の分子の構造を認識しています。TLR受容体が活性化すると、自然免疫が発動して炎症反応や抗ウイルス応答が起こり、病原体を排除します。TLR受容体は膜貫通タンパク質であり、細胞外のロイシンというアミノ酸を多く持つ繰り返し配列部分で分子構造を認識し、細胞内のTIRドメイン注8)を通じてシグナルを伝えています。
TLR7は一本鎖RNAの受容体として同定されており、HIV-1やHCVウイルス感染症に関与しています。また、自身の死細胞などから放出されるRNAへTLR7が過度に応答する現象は、自己免疫疾患に関係するとされています。一方で、TLR7はイミダゾキノリン誘導体注9)やグアノシンなどの低分子化合物によって活性化されることも、報告されています。TLR7が活性化するとインターフェロンなどの産生を促し、免疫反応を引き起こします。このために、TLR7はウイルス感染や自己免疫疾患に対する治療薬やワクチンのアジュバントなどのターゲットとして注目されています。しかし、TLR7がどのようにこれらのリガンドを認識し、免疫を活性化するのかについて具体的な機構は不明でした。
本研究グループは、TLR7による一本鎖RNAおよび低分子リガンドの認識機構を、TLR7-グアノシン-polyU、TLR7-loxoribine-polyU、TLR7-R848、の3つの複合体の立体構造をX線結晶解析注10)で明らかにしました。
大型放射光施設SPring-8および高エネルギー加速器研究機構Photon Factoryの強力なX線を使用して構造解析した結果、TLR7はそれぞれのリガンドと2:2(または2:2:2)の複合体を形成することで活性化型のm字型の2量体構造をとることが明らかになりました(図1)。グアノシンなどの低分子リガンドは2量体界面中の第1結合部位に結合し特徴的な相互作用により認識されていました。また、19のウリジンからなるpolyUの断片のUUU部分はTLR7のN末端側のLRR1-LRR5の凹面およびZ-loop(LRR14とLRR15をつなぐ領域)から構成されている第2結合部位に結合していました。UUUの中央のU部分がその周辺のアミノ酸残基と塩基特異的およびリボース特異的な相互作用を形成していました(図2)。
さらに、TLR7のリガンド特異性および活性化2量体形成機構を調べました。TLR7の第1結合部位は各種ヌクレオシドの中でグアノシンを特異的に認識すること、第2結合部位は非末端部分にウリジン塩基を含む3塩基以上の長さの一本鎖RNAを特異的に認識することを明らかにしました。また、一本鎖RNAによるTLR7の活性化には、第1結合部位と第2結合部位の両方のリガンドが必須であること、さらにTLR7の第1結合部位のリガンドに対する親和性は、TLR7が一本鎖RNAと結合することで強くなることが明らかになりました。
これらの結果から、TLR7の活性化機構を提唱しました(図3)。TLR7はまず第2結合部位を用い、非末端部分にウリジン塩基を含む一本鎖RNAを認識します。次に、第1結合部位にグアノシンが結合することによって、TLR7が活性化します。一方で、R848などの合成低分子リガンドの場合には、第1結合部位への結合だけでTLR7は活性化します。
エンドソーム注11)に局在するTLR7と、TLR7に類似したTLR8とTLR9は一本鎖核酸を認識し、ウイルス感染や自己免疫疾患、さらにはがんまで、さまざまな疾患に関わっていることがわかっています。本研究グループによるこれまでのTLR8およびTLR9の結晶構造解析に加え、今回、さらに世界で初めてTLR7の結晶構造解析に成功しました。
これまでTLR7は一本鎖RNAを認識する受容体だと考えられていましたが、今回の結果から2つのリガンド結合部位を用いて2種類のリガンドを同時に認識し活性化することが明らかになりました。このことから、今後は2つの作用点で制御するという新しい視点で、TLR7をターゲットとした治療薬開発が進むと期待されます。
<参考図>
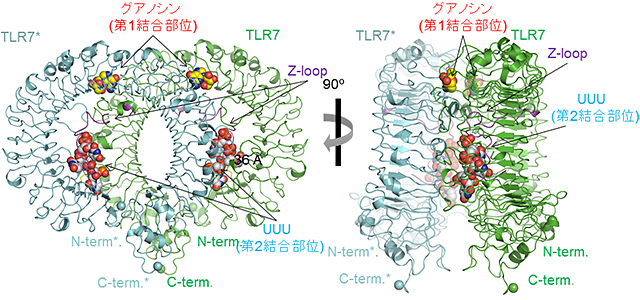
図1 TLR7-グアノシン-polyUの全体構造
2量体を構成している TLR7分子の一方(TLR7)を緑色、他方(TLR7*)を青色で示している。赤文字で示した第1結合部位、および青文字で示した第2結合部位の2箇所のリガンド結合部位が存在し、それぞれグアノシンおよびpolyUの一部のUUUが結合していた。
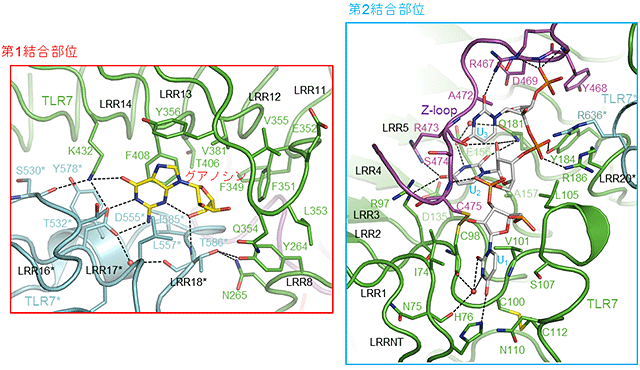
図2 リガンド認識部位の拡大図
- (左図) 第1結合部位の拡大図(グアノシンが結合している)。
- (右図) 第2結合部位の拡大図(PolyUが結合している)。
グアノシン、polyU、TLR7、TLR7*およびZ-loopの炭素原子をそれぞれ黄色、灰色、緑色、シアンおよび紫色で示している。水素結合を破線で示している。
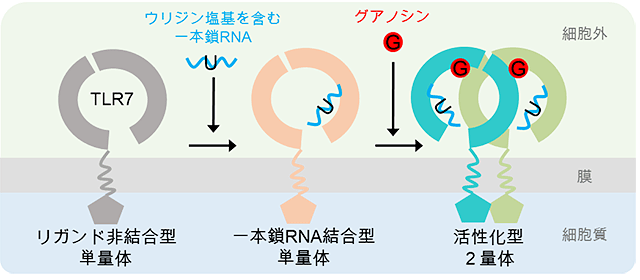
図3 TLR7の活性化機構
グアノシンおよび一本鎖RNAによるTLR7の活性化モデル。まず第2結合部位で非末端ウリジン塩基を含む一本鎖RNAを認識し、次に第1結合部位でグアノシンを認識することで活性化型の2量体が形成される。
<用語解説>
- 注1) リガンド
- 特定の受容体に結合する物質で、それぞれのTLR(ヒトの場合TLR1~TLR10が存在する)は微生物やウイルス由来の異なる物質をリガンドとする。
- 注2) アジュバント
- 抗原と混合して生体に投与することで、投与した抗原に対する免疫応答を増強する物質のことで抗原性補強剤とも呼ばれる。
- 注3) インターフェロン
- 細菌やウイルスなどの病原体の侵入に対して免疫系の細胞が分泌するタンパク質で、ウイルスの増殖を抑制する作用や免疫系を活性化するなどの作用を発揮する。
- 注4) polyU
- 多数のウリジンがホスホジエステル結合で結合した配列を持つRNA。本研究では19のウリジンから構成されるRNAを使用している。
- 注5) グアノシン
- RNAなどの核酸の構成成分として使われている糖と塩基が結合した化合物(ヌクレオシド)の1つ。生体中では他にアデノシン、チミジン、シチジン、ウリジンなどが使われている。
- 注6) loxoribine
- TLR7を活性化する低分子リガンドの1つでグアノシン誘導体である。
- 注7) R848
- TLR7を活性化する低分子リガンドの1つ、Resiquimodとも呼ばれる。TLR8も活性化する。
- 注8) TIRドメイン
- TLRの細胞内の領域で、他のタンパク質と会合することでシグナルを伝達する役割を持っている。
- 注9) イミダゾキノリン誘導体
- 3環系のイミダゾキノリン骨格を有する有機化合物。
- 注10) X線結晶解析
- 物質の構造を解析する手法の1つ。調べたい物質の結晶に対してX線を照射して、そこから散乱されたX線の強度を観測し解析することで最終的に結晶の構造を知ることができる。
- 注11) エンドソーム
- 生体膜からできている小胞で細胞内に存在している。細胞内に取り込まれた物質の選別、分解、再利用などに関係する。
<論文情報>
| タイトル |
“Structural Analysis Reveals that Toll-like Receptor 7 Is a Dual Receptor for Guanosine and Single-Stranded RNA” |
| 著者名 |
張 志寛*、大戸 梅治*、柴田 琢磨、クラユヒナ・エレナ、田岡 万悟、山内 芳雄、丹治 裕美、礒邉 俊明、内山 進、三宅 健介、清水 敏之†(*共同筆頭著者、†責任著者) |
| 掲載誌 |
Immunity |
| doi |
10.1016/j.immuni.2016.09.011 |
<お問い合わせ先>
<研究に関すること>
清水 敏之(シミズ トシユキ)
東京大学 大学院薬学系研究科 教授
Tel:03-5841-4840 Fax:03-5841-4891
E-mail:
URL:http://www.f.u-tokyo.ac.jp/~kouzou/index.html
内山 進(ウチヤマ ススム)
大阪大学 大学院工学研究科 准教授
Tel:06-6879-4216 Fax:06-6879-7442
E-mail:
<JST事業に関すること>
川口 哲(カワグチ テツ)
科学技術振興機構 戦略研究推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: