ポイント
- 骨折治癒過程において、ガンマデルタ(γδ)T細胞という特殊な免疫細胞が重要な役割を果たすことが明らかになりました。
- ガンマデルタT細胞は、主に感染防御に関わるとされていますが、骨折部位ではIL(インターロイキン)-17と呼ばれるサイトカインを産生し、骨を作る骨芽細胞を活性化し、骨折治癒を促進しました。
- 本研究により、今後、IL-17やガンマデルタT細胞を標的とした新たな骨折治療アプローチの開発が期待されます。
骨折治療では、折れた骨を元の位置に戻して固定し、安静に保つことで治癒を図ります。固定期間は数ヶ月に及ぶこともあり、場合によっては日常生活や仕事に大きく支障を来すことがあります。また、高齢患者の場合、長期間ベッド上で安静にすることが原因で筋力が低下し、寝たきりとなることもあります。患者の早期の社会復帰や寝たきり防止のためには、治癒期間の短縮が骨折治療における重要な課題となります。新しい手術法や固定材料の開発といった進歩は見られるものの、今もなお、治癒の遅延例や治癒不良例は少なくありません。
このたび、東京大学 大学院医学系研究科 病因・病理学専攻 免疫学分野の小野 岳人 博士研究員(研究当時)と、岡本 一男 助教、高柳 広 教授らの研究グループは、マウス骨折モデルを用いて、骨折治癒における免疫系の役割を検討しました。その結果、骨折に伴い骨欠損部位でガンマデルタ(γδ)T細胞注1)が増加し、IL(インターロイキン)-17注2)を産生することを見いだしました。IL-17は骨折部位に含まれる間葉系幹細胞注3)を増やし、骨芽細胞に成長させることで、骨の形成を促進しました。IL-17やガンマデルタT細胞を欠損するマウスでは、骨折治癒が遅延していました。以上により、IL-17を産生するガンマデルタT細胞が骨折治癒を促進するという、免疫系による骨折治癒制御の新たなメカニズムが明らかになりました。今後、IL-17やガンマデルタT細胞を治療標的とした骨折治療法の開発が期待されます。
本研究は日本学術振興会 科学研究費補助金、科学技術振興機構(JST) 戦略的創造研究推進事業などの一環で行われました。
本研究成果は、2016年3月11日(米国東部標準時間)に国際科学誌「Nature Communications」にオンライン版で公開されます。
<発表内容>
骨折治癒のプロセスは、炎症反応とそれに続く骨組織の再構築からなります。骨折直後には、血管が断裂して出血し、骨折部位に免疫細胞が集積します。免疫細胞は、損傷時に生じた組織や細胞の細片を除去したり、サイトカイン注4)などを産生して炎症を引き起こしたりします。炎症が消えるのに伴い間葉系幹細胞が集まり、軟骨を作る軟骨細胞や骨を作る骨芽細胞に成長し、これらの細胞が仮骨注5)を形成し、骨の断片同士が固定されます。その後、破骨細胞と骨芽細胞によって骨組織の再構築が進み、骨はほぼ元通りの形態を取り戻します。
骨折治療では、この治癒プロセスが効率的に進むよう、折れた骨の断片を元の位置に戻したうえで固定し、患部を安静に保ちます。固定の際にはプレートなどの人工物を埋入することもあります。固定期間は骨折部位によって異なりますが、長い場合は数ヶ月に及ぶこともあり、さらにリハビリテーションが必要となる場合もあります。これらの行動制限により、骨折治療期間中は患者の日常生活や仕事に大きく支障を来すことがあります。また、高齢患者の場合、長期間ベッド上で安静にすることで筋力が低下し、その結果寝たきりとなることもあります。単に折れた骨を治すためだけでなく、患者の早期の社会復帰や、寝たきりの防止のためにも、治療期間を短縮する新規の骨折治療法を確立する必要があります。
骨折部位には免疫細胞やサイトカインが見いだされることから、これらを制御することによって治癒を促進できる可能性があります。しかし、骨折後どういった免疫細胞がどのような分子を産生し、その分子がどのように治癒を制御しているのかが十分に解明されなければ治療への応用は困難です。骨折部位に集積する免疫細胞にはT細胞が含まれますが、どういったT細胞がどのように治癒を制御するかは分かっていませんでした。
本研究では、マウスの骨折モデルを用いて解析しました。骨折に伴うT細胞に関連するサイトカインの発現変動を検討したところ、IL-17の産生が損傷部局所で増加することが明らかになりました。IL-17遺伝子を欠損するマウスでは、野生型マウスと比べて骨芽細胞の活性が低減し、骨折治癒が遅延しました(図1)。培養細胞系での実験により、IL-17は骨折部位に含まれる間葉系幹細胞の増殖と骨芽細胞分化を促進することが分かりました。IL-17の産生源となる細胞の同定を行ったところ、T細胞の一種であるガンマデルタT細胞が骨折後にIL-17を産生することを見いだしました(図2)。ガンマデルタT細胞を欠損するマウスの骨折治癒を解析したところ、野生型マウスと比べて治癒の遅延が認められました。以上により、IL-17産生ガンマデルタT細胞が骨折治癒過程において、骨芽細胞による骨形成を刺激することにより骨折治癒を促進することが明らかになりました(図3)。
ガンマデルタT細胞は皮膚などの体内と体外の境界部に多く存在し、生体防御に関わるといわれてきました。本研究を通じて、ガンマデルタT細胞には骨折治癒促進という意外な機能があることを見いだし、ガンマデルタT細胞が骨形成を促すという新しい骨制御機構を提示することができました。また、関節リウマチなどの疾患研究を通じて、IL-17の組織破壊への関与がよく知られていましたが、本研究によりIL-17の組織修復作用を生体レベルで明らかにすることができました。
近年、活性化ガンマデルタT細胞を利用した抗腫瘍療法が開発され、注目されています。骨折治療においてもガンマデルタT細胞を活性化し、IL-17産生を促進することができれば治療への応用が期待できます。本研究成果により、IL-17やガンマデルタT細胞を標的とした新たな骨折治療法の開発が期待されます。
<参考図>
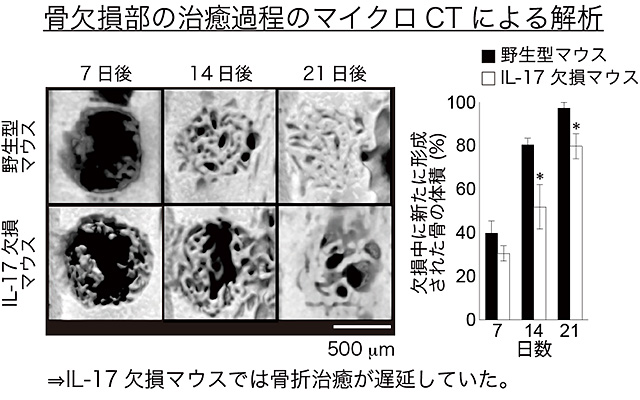
図1 IL-17を欠損するマウスでは骨折治癒が遅延する
野生型マウスおよびIL-17欠損マウスの大腿骨に手術により円形の骨欠損を形成し、治癒過程をマイクロCTにより評価しました。手術後14日以降では、野生型マウスと比較してIL-17欠損マウスに治癒の遅延が認められました。
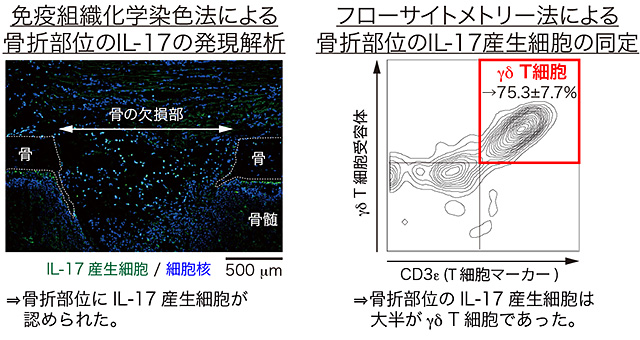
図2 骨折部位ではガンマデルタ(γδ)T細胞がIL-17を発現する
- (左)免疫組織化学染色法によりIL-17産生細胞の局在を調べたところ、骨の欠損部やその周囲にIL-17産生細胞が認められました。
- (右)フローサイトメトリー法注6)により骨折部位のIL-17産生細胞を解析しました。IL-17産生細胞一つ一つについてT細胞マーカー(CD3ε)とガンマデルタT細胞マーカー(γδT細胞受容体)の発現を解析し、発現状態をグラフに示しました。IL-17産生細胞の大半は両方のマーカーを発現する(図中の赤い四角内)、ガンマデルタT細胞でした。
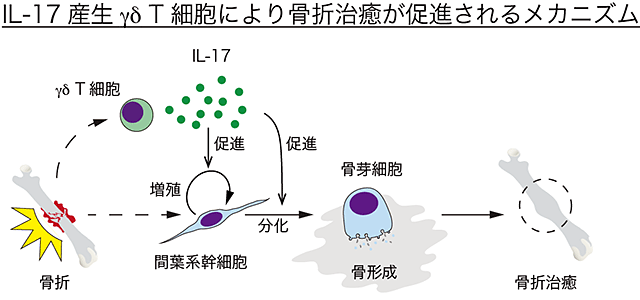
図3 骨折治癒過程ではガンマデルタ(γδ)T細胞がIL-17を産生することにより骨折治癒を促進する
骨折すると、ガンマデルタT細胞が損傷部に速やかに集まり、IL-17を産生します。IL-17は損傷組織中の間葉系幹細胞に作用し、増殖と骨芽細胞分化を誘導します。骨芽細胞により骨折部位に新たに骨組織が形成され、治癒に至ります。
<用語解説>
- 注1) ガンマデルタ(γδ)T細胞
- T細胞は胸腺由来のリンパ球で、生体防御に重要な細胞である。T細胞は病原体などを認識する受容体(TCR)としてαβTCRまたはγδTCRを発現する。αβTCRを発現するαβT細胞は血液中に多量に存在し、免疫応答の中心的役割を担う。一方、γδTCRを発現するγδT細胞は血液中には少なく、皮膚や肺などに多く存在し、病原体の侵入など生体の受けたストレスに迅速に反応する。
- 注2) IL(インターロイキン)-17
- 主に活性化したT細胞が産生するサイトカイン(注4参照)。生体を構成する種々の細胞に作用し、炎症反応を誘導することにより、感染防御や自己免疫疾患における組織の破壊に関与することが知られている。
- 注3) 間葉系幹細胞
- 骨、軟骨、脂肪などの組織は、間葉と呼ばれる胎児期の細胞集塊に由来する。骨芽細胞や軟骨細胞、脂肪細胞などへの分化能を持ち、かつ、自己複製能を持つ細胞を間葉系幹細胞と呼ぶ。
- 注4) サイトカイン
- 細胞から放出され、細胞間の情報伝達に関わるタンパク質の総称。
- 注5) 仮骨
- 骨折治癒の過程で見られる未熟な骨。線維組織や軟骨組織、骨組織からなり、折れた骨の断片同士を固定する。治癒が進むと骨組織の再構築に伴い成熟した骨組織に置き換えられる。
- 注6) フローサイトメトリー法
- 試料に含まれる細胞を一つずつ高速で水流に流しながらレーザーを照射し、各々の細胞が発する蛍光を指標に、細胞一つ一つの大きさや分子の発現を解析する手法。
<論文情報>
| タイトル |
“IL-17-producing γδ T cells enhance bone regeneration” |
| 著者 |
Takehito Ono, Kazuo Okamoto, Tomoki Nakashima, Takeshi Nitta, Shohei Hori, Yoichiro Iwakura and Hiroshi Takayanagi |
| 掲載誌 |
Nature Communications |
| doi |
10.1038/ncomms10928 |
<お問い合わせ先>
<研究に関すること>
高柳 広(タカヤナギ ヒロシ)
東京大学 大学院医学系研究科 病因・病理学専攻 免疫学分野 教授
Tel:03-5841-3373 Fax:03-5841-3450
E-mail:
<JST事業に関すること>
大山 健志(オオヤマ タケシ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: