ポイント
- 細胞性粘菌が細胞間を波のように伝播する誘引物質を合図に集まる性質により、理論上、去りゆく波にも反応して元居た場所へ戻っていってしまう「走化性パラドクス」が生じる。
- 2つの新技術の開発(微小流路内の高精度な層流制御技術、細胞内反応の定量的測定技術の開発)と理論モデルの検証によって、「走化性パラドクス」が起こらない仕組みが分かった。
- 誘引物質によって動く方向が定まる性質は、細胞性粘菌から免疫細胞まで共通してみられるため、体内の目的の組織へ正確に移動する仕組みの理解につながることが期待される。
細胞性粘菌注1)は、単細胞として過ごす時期と、細胞が集合して子実体と呼ばれる多細胞構造を形成する時期とを繰り返します。細胞性粘菌の集合の合図は、細胞間を波のように伝搬する誘引物質が担っており、細胞は誘引物質の濃度がより高い方へ移動します。しかし、それでは、誘引物質の波が進行方向からやってきて去りゆく過程においては細胞が元居た場所へ戻っていってしまう「走化性パラドクス」(図1)が生じます。細胞が去りゆく波に“惑わされず”、一方向に動いていく仕組みの解明が待たれていました。
東京大学 大学院総合文化研究科の澤井 哲 准教授らの研究グループは、細胞性粘菌は誘引物質が経時的に増加する場合のみ、移動するための信号を細胞内に伝達することを明らかにしました。このような細胞応答は、「整流作用注2)」と呼ばれる信号処理特性でコンピュータなどの集積回路に用いられるダイオードが一方向にのみ電気を流す特性と同じです。また、この「整流作用」は、誘因物質の濃度変化に応答する反応機構に、ある範囲での変化に対してのみ鋭敏に反応する性質があるために生じることを示しました。この発見は、微小流路内の高精度な層流制御技術と細胞内反応の定量的測定技術の開発、および理論モデルによる検証から可能となったものです。
今回の結果は、多細胞組織のように外部刺激が時間的にかつ空間的に大きく変化する環境における、細胞の移動方向の決定の動作原理について、大きな手がかりとなるものです。ヒトを含む動物の発生や創傷治癒、免疫反応などにおける細胞移動の機構の理解と、その操作法の開発につながることが期待されます。
<発表内容>
アメーバ細胞や免疫細胞などの這い回る細胞の移動方向が、場の情報からいかにして決定されているかは未解決の問題です。這い回る細胞の多くは誘引物質の濃度を細胞の前と後ろで比べ、濃度の高い側でのみ、アクチンと呼ばれるタンパク質が樹状の線維を形成し、これによって膜を伸張し、濃度の高い方へ移動すると考えられています。これを走化性運動注3)と呼びます。こうした運動の理解は、生化学、分子遺伝学的な実験を実施しやすい細胞性粘菌において進展しています。細胞性粘菌は微生物の一種ですが、単細胞で過ごす時期と細胞が集合して子実体と呼ばれる多細胞構造を形成する時期とを繰り返します。細胞が集合する際の誘引物質は、個々の細胞が分泌するサイクリックAMP(cAMP)という化学物質で、粘菌の細胞は、このcAMPが波のように細胞集団中を伝搬するときの濃度変化を頼りに集合し、多細胞組織を構築します(図1a)。しかし、cAMPの濃度が高い方に移動するというだけでは、「走化性パラドクス」(図1b)と呼ばれる問題が生じます。つまり、cAMP波が細胞へ近づいてくるときはcAMP濃度がより高い方へ動けばよいのですが、cAMP波が細胞から離れていくときに、細胞がcAMP濃度の高い方へ動いてしまっては、細胞は結局元の位置に戻ってしまいます。「走化性パラドクス」が実際の細胞性粘菌に起こらない分子機構として、これまで、細胞が波を積極的に検知しない時期を仮定するものや(不応期説)、細胞の動きが記憶されてそれが持続する(メモリー説)などが提唱されてきましたが、いずれも決定打ではなく、長年、未解決のまま残されてきました。
今回、東京大学 大学院総合文化研究科の澤井 哲 准教授らの研究グループは、細胞性粘菌が、誘引物質cAMPの濃度が経時的に増加する場合のみ、移動するための信号を細胞内に伝達することを明らかにし、この性質によって走化性パラドクスを解決できることを示しました。これは、微小流路内の層流形成によって空間的、時間的に誘引物質の濃度を高精度に制御する技術と、細胞の先端が形成される際の細胞内反応の定量的測定技術、という2つの革新的技術の組み合わせによって初めて可能になったものです。研究グループは、人工的に形成した動的勾配について、さまざまな時定数と、時間変化、空間変化の符合の組み合わせを検討しました(図2a)。また、細胞先端の形成を促す物質の一種であるRasタンパク質(低分子量GTP結合タンパク質)の活性化を、蛍光タンパク質を用いてレーザー共焦点顕微鏡により測定し(図2b)、データを理論モデルと比較、解析しました。その結果、Rasの局所的活性化と大域的抑制化で構成されるフィードフォワード型の反応ネットワーク(図3)に強い抑制がかかっている場合に、cAMP濃度の上昇に反応してスイッチ的な応答(ゼロ次の超感度性注4))を示すこと、この性質によって細胞の適応応答注5)に整流作用が出現すること、整流作用によって観測された細胞の振る舞いのほとんどが矛盾なく説明できることが示されました(図4)。ゼロ次の超感度性は、Rasが活性化された場合の細胞内伝達経路において出現しやすいことが従前予想されており、このことと整流作用がみられることとはよく整合しています。今回の結果は、誘引物質濃度が時間とともに減少する場合に誘引物質が存在するというシグナルを細胞内伝達経路の下流に伝えないこと(整流作用)で、波の背面が無視されていることを示しています(図5)。
細胞の運動に関わる分子群は、細胞性粘菌と免疫細胞において多くの共通性がみられます。今回の発見は、細胞性粘菌の理解に限らず、従来、時間的に変化しない濃度勾配で調べられてきた細胞の移動方向の決定機構について、大きな手がかりとなります。濃度勾配検出の時間変化依存性は、免疫細胞などで示唆されてきており、こうした細胞が場の時空間情報を読み取って体内の目的の組織へ正確に移動する仕組みの理解につながることが期待されます。整流作用は、元来、ダイオードなど一部の電子素子が持つ特性として知られてきたものですが、今後、細胞においていかにこの効果が実装されているかを解明することで、動作原理に基づいた細胞の操作法への応用開発が期待されます(図6)。
本成果は、文部科学省および学術振興会の科学研究費 新学術領域「動く細胞と場のクロストークによる秩序の生成」公募研究、若手研究(A)、(B)、文部科学省の生命動態システム科学推進拠点事業ならびに独立行政法人 科学技術振興機構の戦略的創造研究推進事業の支援のもと、東京大学 大学院総合文化研究科の中島 昭彦(東京大学 特任助教)、石原 秀至(東京大学 助教(現 明治大学 准教授))、修士課程2年の井元 大輔(当時)、澤井 哲(東京大学 准教授、兼 科学技術振興機構 さきがけ研究者)によって得られました。
<参考図>
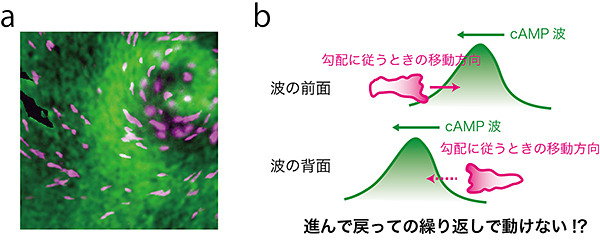
図1 アメーバ細胞の「走化性パラドクス」
a)細胞集団中で自己組織化される誘因物質cAMPのらせん波(緑)と波の中心へむかって移動する細胞(マゼンタ)。b)「走化性パラドクス」の概念図。アメーバ細胞がcAMPの濃度の高い方へ移動する、とすると、波の空間勾配の方向は波の前面と背面で反転するので、進んで戻っての繰り返しで動けないため集合できないことになる。「走化性パラドクス」は、細胞が時空間的に変化する情報をいかに統合して行動を決定するかを考える上で、理想的な例題である。
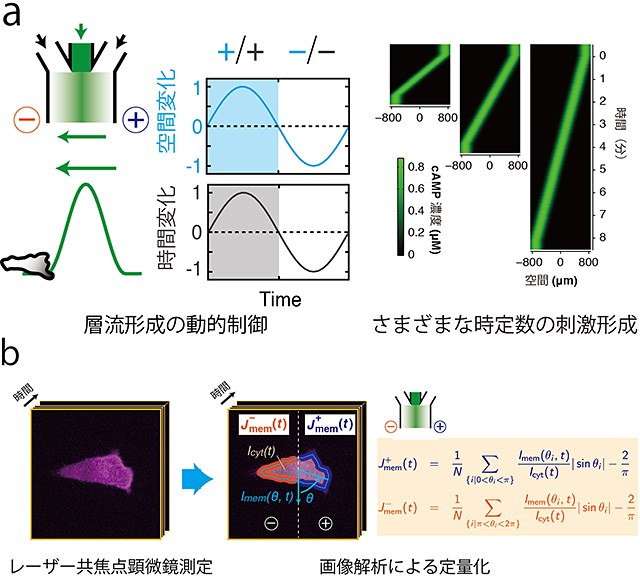
図2 人工的な動的勾配の形成と実験データの精密な定量解析
a)微量流路内に形成した層流によってできた誘因物質cAMPの濃度勾配。層流の流れを動的に制御することで、さまざまな時間空間変化や異なる時定数をもった動的勾配をつくりだす。b)レーザー共焦点顕微鏡測定により取得した細胞応答の様子を画像解析によって定量化し、その結果得られたデータを理論モデルと比較、検証した。
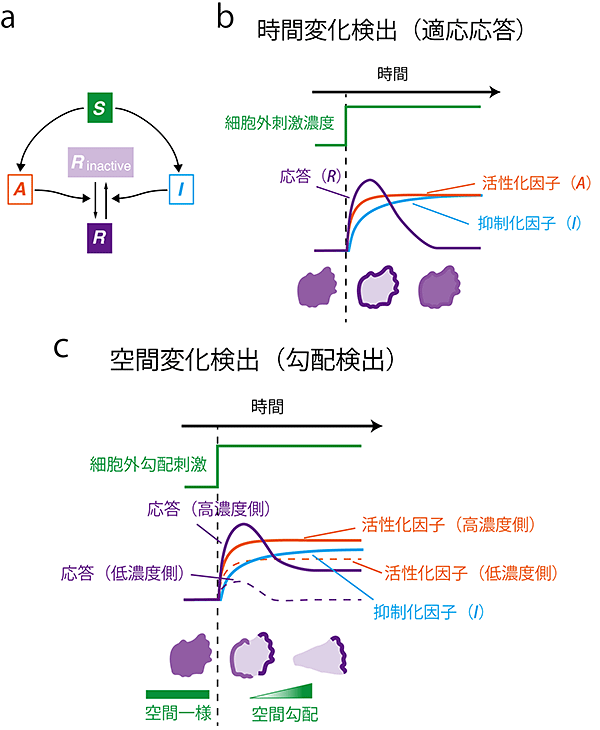
図3 細胞は誘引物質cAMP濃度の時間的、空間的な変化を検出して動く方向を決める
a)時間的変化への応答(適応応答)を生み出すフィードフォワード型の細胞内シグナル伝達経路。細胞外シグナル(S )により活性化された活性化因子(A )と抑制因子(I )が出力(R )をそれぞれ活性化、抑制する。細胞内で活性化因子(A )が局所的に働き、抑制化因子(I )がA より早く拡散することによって細胞全体に伝わるという性質( Local Excitation and Global-Inhibition (LEGI) mechanism)をもてば、適応応答と勾配検出を同時に実現する。b)膜局在を示す走化性シグナル因子の時間変化検出(適応応答)とc)時間変化検出(勾配検出)。
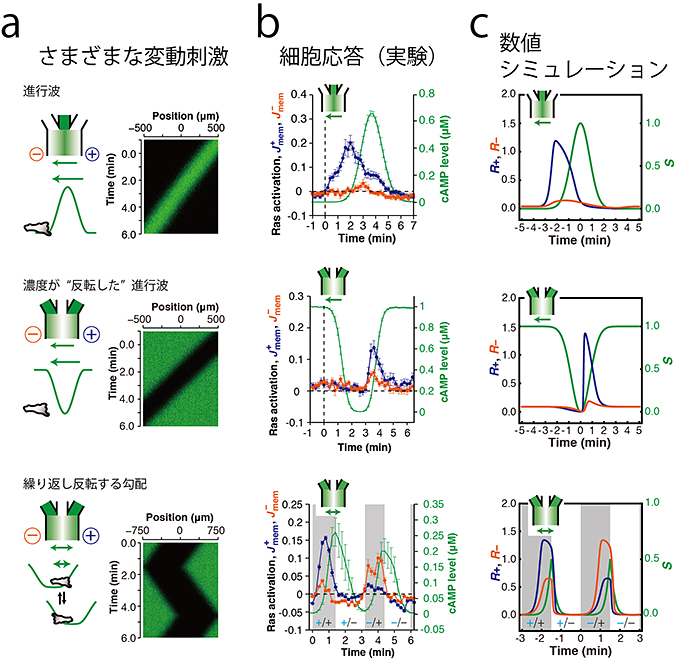
図4 時間空間的に変動する刺激に対する応答はLEGIメカニズムから理解できる
a)微小流路系で形成された誘引刺激の時間空間的な振る舞い。b)細胞先端形成(Rasの活性化)の様子(青、赤はそれぞれ細胞右側、左側のRBD-RFPの輝度値。緑は誘引物質cAMPの濃度)。c)今回提案した超感度性LEGIモデルの振る舞い。誘引物質cAMPの濃度が時間的に上昇している場合にのみ、細胞先端を形成する反応(Rasの活性化)がみられる。
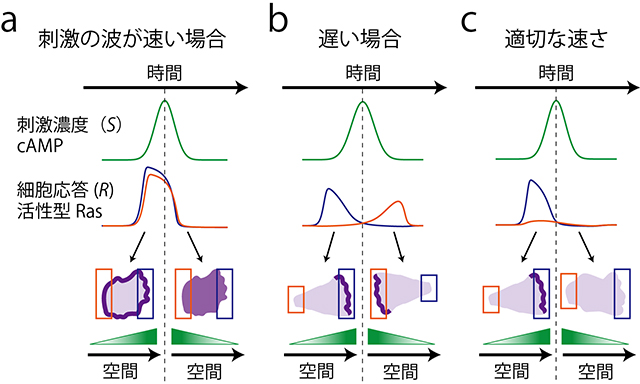
図5 中程度の波の速さでは、細胞の整流作用を介して波の前面でのみ方向検出が生じる
a)、b)、c)さまざまな波の速さに対する細胞実験と理論モデル結果の模式図。a)波が速い場合、b)遅い場合、c)適切な速さの場合。細胞は誘因物質が適切な速さで通過するときにのみ一方向に運動する。このような速さによる細胞の振る舞いの違いは、細胞の整流作用の性質からうまく理解できる。
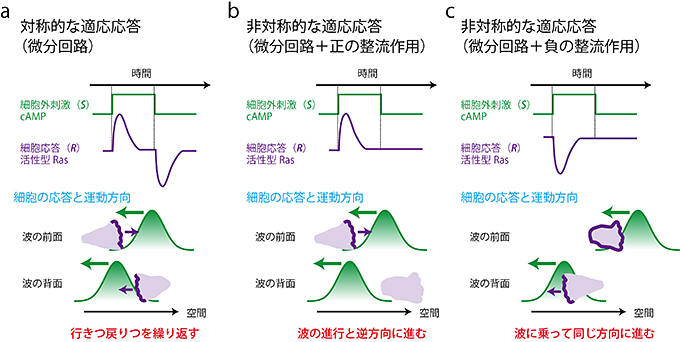
図6 細胞の信号処理特性に応じて細胞移動の方向は変化する
a)刺激の時間変動に対して対称的な適応応答(微分回路)をする場合。b)、c)時間変動に対して非対称な適応応答(微分回路+整流作用)をする場合b)正の整流、c)負の整流。(上段)誘引物質cAMPの空間的に一様な刺激に対するRasの活性化(a、bは測定結果、cは理論からの予想)の模式図。(下段)cAMPの進行波刺激に対するRasの活性化の模式図。
<用語解説>
- 注1) 細胞性粘菌
- 微生物の一種で、単細胞として過ごす時期と、細胞が集合して子実体と呼ばれる多細胞構造を形成する時期とを繰り返す。代表的な種であるキイロタマホコリカビ(学名 Dictyostelium discoideum )は、ゲノムが解読され、酵母にも匹敵する分子遺伝学的操作の自由度と、1細胞と多細胞レベルの可視化と操作性に優れた、細胞移動のモデル生物種。数万個のアメーバ細胞は飢餓を感知すると走化性誘因物質としてサイクリックAMP(cAMP)を自己分泌的に放出し、個々の細胞応答が揃うことでcAMPの進行波が自己組織的に形成される。個々の細胞は空間を伝搬するcAMP波とは逆向きに動き、これによって集合し、多細胞組織を構築する。同じ粘菌でも、多核の巨大アメーバを形成する真性粘菌とは別の系統群に属する。
- 注2) 整流作用
- 工学的に広く知られている性質で、コンピュータなどの集積回路に用いられるダイオードは一方向にのみ電気を流す性質をもち、このような振る舞いが整流作用と呼ばれる。この性質によって交流を直流に変換することや、電気回路の複雑な動作をつくることができる。今回のアメーバ細胞の場合には、誘引物質の濃度が時間的に減少している場合にシグナルを反応経路の下流に伝えない性質を指す。細胞内のシグナル伝達経路(図3a)に超感度性が含まれることによって同等の性質が出現する(図6b)。
- 注3) 走化性
- 化学走性ともいう。真核細胞の多くでは、特定の化学物質を膜上の受容体タンパクで検出し、空間的な濃度勾配を読み取ることで一方向的に移動することが知られている。発生における形態形成運動や、免疫細胞が目的の組織や細胞に辿り着くための基本を担っている。
- 注4) ゼロ次の超感度性(zero-order ultrasensitivity)
- 細胞内の反応における、オンかオフかのスイッチ的な振る舞いを説明する機構の一つ。アルベルト・ゴールドベーターとダニエル・コッシュランドによって80年代初頭に提唱された。ある分子が、リン酸化や脱リン酸化のように互いに逆方向の酵素反応によって2状態を行き来でき、かつ酵素反応の進みやすさが、基質の低濃度領域で決まる場合、順方向か逆方向のいずれかの酵素反応のみが、ある一定の最大速度で基質の量に依存せず(ゼロ次反応)進む。これによって、ある反応パラメータの値を境目にして、順方向、逆方向の生成物のいずれかのみが産生される極端な状況が生じる。細胞先端の形成を担うRasなどの低分子量GTPアーゼは、GTP結合型とGDP結合型の2状態間で遷移し、これらがそれぞれ酵素反応で調節される反応(図3a)を構成しているため、超感度性が生まれやすいことが従来から指摘されている。
- 注5) 適応応答
- 外部刺激を受けた際、一時的に強い応答を示した後に、外部刺激が持続しているにも関わらず、刺激を受ける前の状態へと戻るような一過性の応答のこと。適応応答を示すシステムは外部刺激の強さが変わるときに応答を示すため、外部刺激の時間変化を検出できる。真核細胞の走化性では、フィードフォワード型のシグナル伝達経路(図3a)によって実装されていると考えられている。適応応答は、真核細胞の走化性応答の他にも、バクテリアの走化性、成長因子に対する細胞の応答や酵母の浸透圧調節応答などさまざまな生命現象で普遍的にみられる振る舞いである。また、このような性質は工学的に広く知られる微分回路的な振る舞いでもある。
<発表雑誌>
| 雑誌名 |
Nature Communications(オンライン版11月6日) |
| 論文タイトル |
“Rectified directional sensing in long-range cell migration” |
| 著者 |
中島 昭彦、石原 秀至、井元 大輔、澤井 哲*
(* corresponding author) |
| doi |
10.1038/ncomms6367 |
<お問い合わせ先>
<研究に関すること>
澤井 哲 (サワイ サトシ)
東京大学 大学院総合文化研究科 広域科学専攻 准教授
Tel:03-5454-6737 Fax:03-5454-6737
<JST事業に関すること>
科学技術振興機構 戦略研究推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: