
HOME 研究代表者・研究課題 平成24年度採択 菅裕明

擬天然物の新機能創出分子技術
微生物の産生する天然物が人の疾患発現機構に効用を発揮することがわかり、新薬開発の手がかりとなることがあります。しかし、それは単に「偶然の賜物」に過ぎません。本研究では、天然物に似た化合物、すなわち「擬天然物」群を人工的に合成し、システマティックかつ迅速に活性種を見つけ出す新分子技術を創出することで、偶然から「確実」な発見へとパラダイムシフトを起こしうる「新薬発見の新潮流」を生み出します。それにより、人類の健康に資する技術イノベーションを日本から起こすことを目指します。
- 既存技術ではUndruggableな標的に対する薬剤開発を可能にする基盤技術
- 抗体に匹敵する特異性と薬効をもち、経口剤として処方可能な薬剤の開発
- 次世代創薬の新潮流をつくりうる付加価値の高い分子技術
- 国内外の製薬企業から注目を集め、連携が可能な基盤をもつ体制
- 菅 裕明
- 東京大学
大学院理学系研究科
教授 研究室HP
これまでの研究成果(インパクト)
- 人工擬天然物のワンポット合成法とRaPIDシステムの確立
マイルストーン(1)XX-PatD-FITシステムの完成(XXは特許の関係から非公開)
マイルストーン(2)XX-PatD-FITシステムを応用したAz-RaPIDシステムの構築
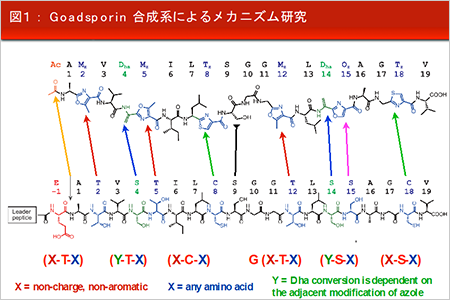
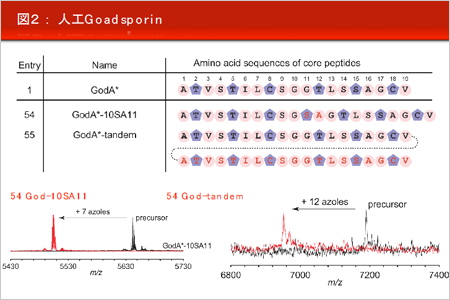
平成28年度に両マイルストーン共に達成。派生的に達成したゴードスポリン合成系の再構成で論文の発表(図1、図2)。 - 膜透過人工擬天然物の超迅速探索法の確立
マイルストーン(3)LiPIDシステムに適した特殊ペプチドライブラリーの構築
マイルストーン(4)細胞内タンパク質に結合する特殊ペプチド・擬天然物のLiPIDセレクション
平成28年度に両マイルストーン共に達成。 - 細胞内薬剤活性を示す人工擬天然物の発見
マイルストーン(5)タンパク質標的Iを阻害する人工天然物の発見
マイルストーン(6)タンパク質標的IIを阻害する人工天然物の発見
平成28年度にマイルストーン(5)については達成し、活性種の機能解析を進めている。
今後の進め方
- マイルストーン(4)で獲得された擬天然物活性種の解析データ収集を進める。
- マイルストーン(5)で獲得された特殊環状ペプチド活性種の解析データ収集を進める。
- マイルストーン(6)の人工擬天然物の発見を目指し、その解析データ収集を進める。
これまでの研究成果(インパクト)
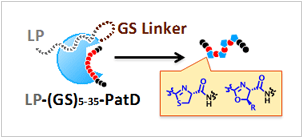
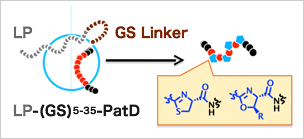
- ヘテロ環合成酵素の人工改変と短鎖ヘテロ環含有ペプチドの迅速合成
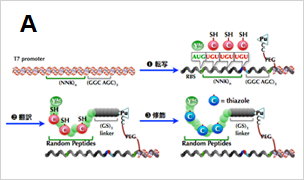
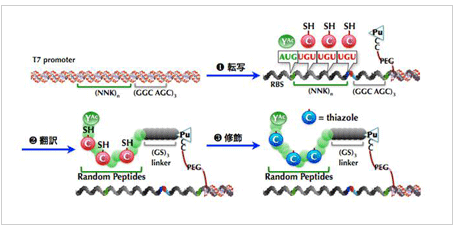
- 短鎖ヘテロ環含有擬天然物活性種探索に向けたRaPID-PatDシステムの確立(図A) 成果:上記図Aと図Bに記載されたシステムについては応用に向けた稼働が始まった。標的タンパク質を2種類選び、結合リガンド・阻害剤のRaPID探索を展開している。
-
Ψ(CH2NH)含有ペプチドの合成
成果:本研究では、Ψ(CH2NH)含有ペプチドの合成を達成した(図C)。システィン残基をPatDの触媒機能でチアゾリンに変換した後、化学的な還元を施すことでΨ(CH2NH)含有ペプチドを合成する技術を達成した。 -
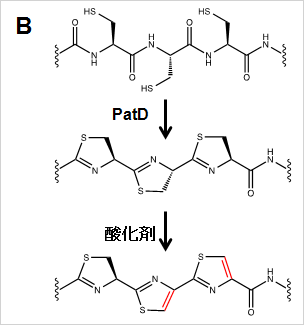
連続チアゾールの合成(図B)
成果:本研究では、システィン残基を連続で入れたペプチドにPatDでチアゾリン基に変換した場合、下流のチアゾリン基は自動酸化を受け、チアゾール基へと変換されることを発見した。条件検討をした結果、適切な酸化試薬を用いることで効率よく連続チアゾール基をもつペプチドへと誘導できる技術を確立した。 -
酸化酵素によるアゾールの合成
成果:本研究では、あるアゾリン酸化酵素をFIT-PatDシステムと組み合わせることで、非常に効率よくアゾール含有ペプチドを合成できることが判明した。この方法論を技術として確立すべく、検討を進めた(詳細は未公開)。
今後の進め方
- RaPID-PatDシステムを用いた標的タンパク質へのヘテロ環含有擬天然物のセレクションを継続的に実証する。
- LiPIDシステムを駆使した標的タンパク質への膜透過性特殊ペプチドのセレクションを継続的に実証する。
- 酸化酵素を組み込んだ新規アゾール含有擬天然物の合成法をライブラリー構築に応用する。
図A
図B
図C
これまでの研究成果(インパクト)
- ヘテロ環合成酵素の人工改変と短鎖ヘテロ環含有ペプチドの迅速合成
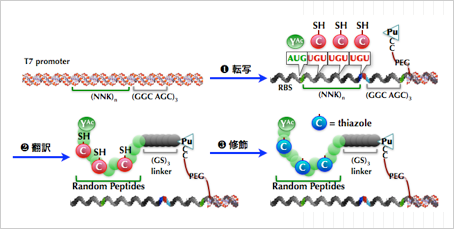
基質に存在するN末端リーダーペプチド配列を移植したLP-PatDを(図A)を作製、これを自在に遺伝暗号をリプログラミングできる翻訳システム(FITシステム)と組み合わせた。このFIT-LP-PatDシステムを用いて、その基質許容性を明らかにし、その知見に基づいて、チアゾリン環含有ペプチドライブラリーの構築まで達成した。 - 短鎖ヘテロ環含有擬天然物活性種探索に向けたRaPID-PatDシステムの確立(図B)
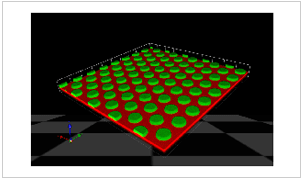
RaPID-PatDシステムの確立を受け、本年度はSIRT2をモデル標的として阻害剤探索を進めた(結果は非公開)。 - 2重脂質膜で分離された極小ウェル作成技術の確立(図C)
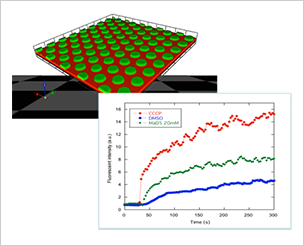
本研究では、膜透過性を有する擬天然物の探索に資する技術を開発するために、MEMS(Micro-Electro-Mechanical Systems)技術を用いて作成した極小ウェル上に、簡便に2重脂質膜を形成させる技術基盤を確立した。これまで、20フェムトリットルの体積をもつ極小ウェルにディフェクト・フリーで2重脂質膜を形成させることに成功し、そのシステムを利用してATP合成酵素の活性を観測できることを実証した。本成果は、東京大学大学院工学系研究科の野地博行研との共同研究としてNature Communications(2014年7月24日号)に論文として発表した。
今後の進め方
- RaPID-PatDシステムを用いた標的タンパク質へのヘテロ環含有擬天然物のセレクションを実証する。
- LiPIDシステムを駆使した標的タンパク質への膜透過性特殊ペプチドのセレクションを実証する。
- 新規Ψ(CH2NH)含有ペプチドの合成法をライブラリー構築に応用する。
図A
図B
図C
これまでの研究成果(インパクト)
- ヘテロ環含有擬天然物合成法の創出―PatD酵素エンジニアリング
基質に存在するN末端リーダーペプチド配列を移植した改変PatDを作成することで、PatDを恒常的に活性化することに成功、ライブラリーの構築に足がかりをつけた(図A)。この酵素を用いて、ヘテロ環含有擬天然物ライブラリーの構築のため、種々の配列を翻訳・ヘテロ環変換合成できることを確認した。 - 擬天然物探索法の開発―RaPID-PatDシステム(図B)
改変PatDを用いて合成される擬天然物のライブラリーをRaPIDディスプレイと組み合わせ、活性種探索技術を確立した。 - 極小ウェル作成技術の確立―fL二重脂質膜アレイ(図C)
脂肪酸二重脂質膜を介して接着する極小アレイ(100,000穴/cm2)の作製法の開発を受け、それを用いて薬剤トランスポーターの活性を確認した。
今後の進め方
- RaPID-PatDシステムを用いた標的タンパク質へのヘテロ環含有擬天然物のセレクションを実施する。
- LiPIDシステムを駆使した標的タンパク質への膜透過性特殊ペプチドのセレクションを実施する。
- 2重脂質膜アレイを用いた膜透過ペプチド探索技術を確立する。
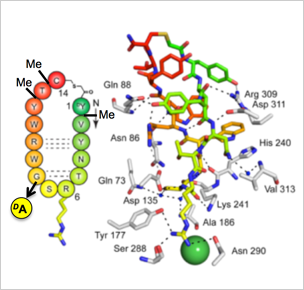
図1:主骨格Nメチルスキャン法
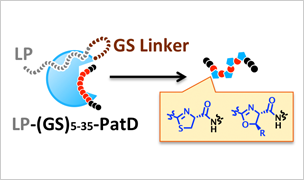
図2:PatD酵素エンジニアリング
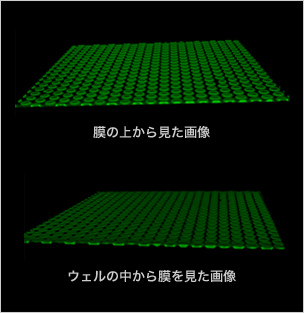
図3:ファムトリットルスケールの
2重脂質膜アレイの作製
これまでの研究成果(インパクト)
- 大環状ペプチドのプロテアーゼ耐性と細胞膜透過性を向上させる分子技術の創出 ─ 主骨格Nメチルスキャン法(図1)
【成果】RaPID法で発見した高活性特殊ペプチドの主骨格にメチル化を各ポジションに入れた特殊ペプチドを化学合成し、その活性を評価し、同時にプロテアーゼ耐性を確認。その後、ヒト細胞膜透過を検討することで、膜透過特殊ペプチドを発見した。 - ヘテロ環含有擬天然物合成法の創出 ─ PatD酵素エンジニアリング
【成果】セリン・スレオニン・システィンの側鎖を主鎖とヘテロ環化する酵素のひとつPatDが標的とする基質特異性を詳細に検討。その結果、基質のN末端リーダーペプチドがPatDに活性化に必要であることが判明。さらにN末端にリーダー配列を融合することでPatDを恒常的に活性化することに成功、ライブラリーの構築に足がかりをつけた(図2)。 - 膜透過指標スクリーニング法の開発 ─ ファムトリットルスケールの2重脂質膜アレイの作製(図3)
【成果】脂肪酸二重脂質膜を介して接着する極小アレイ(100,000穴/cm2)の作製法の開発に成功。
今後の進め方
- 既に菅研で得られている他の生理活性大環状特殊ペプチドについて主骨格Nメチルスキャン法を適応して、細胞内活性を評価する。
- ヘテロ環含有擬天然物のセレクション法を確立する。
- 2重脂質膜アレイを用いた膜蛋白質挿入技術の開発(技術検証)と膜透過ペプチド探索技術を確立する。
