事業成果
医薬品開発の研究にも貢献
iPS細胞でヒト臓器をつくる2017年度更新

- 谷口 英樹(横浜市立大学 大学院医学研究科 教授)
- 戦略的イノベーション創出推進プログラム(S-イノベ)
- 「iPS細胞由来ヒト肝幹細胞ライブラリーの構築によるファーマコセロミクス基盤技術開発」プログラムマネージャー(H21-25)
- 再生医療実現拠点ネットワークプログラム
- 「iPS細胞を用いた代謝性臓器の創出技術開発拠点」拠点長(H25-26)※
※当事業は、2015年度より、国立研究開発法人 日本医療研究開発機構に移管されました
iPS細胞研究は「臨床」と「臓器創出」の段階へ
京都大学の山中伸弥教授らの研究チームが、ひとたび分化した細胞は初期化しないとの従来の医学の常識をくつがえし、どのような細胞にも分化し得る多能性を持つ「iPS細胞」をヒトの皮膚細胞から作り出して、世界を驚かせたのは2007年11月のことだ。
そしてiPS細胞の研究はすでに、どのような細胞に分化し得るかをシラミつぶしに調べる段階は終えつつある。現在の主要課題は、「iPS細胞を応用した臨床研究」と「臓器の創出」である。ともに再生医療(失われた組織・臓器を再生させる医療)への応用だが、2013年には大きな前進があった。すなわち、前者については8月、理化学研究所の髙橋政代プロジェクトリーダーらにより、S–イノベの成果を引き継いだ再生医療実現拠点ネットワークプログラムにおいて世界初の臨床研究が開始された。そして後者については7月、谷口英樹教授らのチームがS-イノベにおいて、世界で初めてヒト臓器を創り出したのである。
「細胞の誘導から臓器の誘導」という発想の転換
特定の臓器が障害を受けて機能しなくなる、末期臓器不全症という疾患がある。これに対しては、損なわれた臓器を健常な臓器へと置換する「臓器移植」が有効な治療法である。しかし、年々増大する臓器移植のニーズにドナー臓器の供給はまったく追いつかないのが現状で、問題解決には臓器移植に代わる治療法の開発が必須かつ急務だ。そこで近年は、多能性幹細胞(iPS細胞、ES細胞)から分化誘導した臓器の細胞を用いて、損なわれた臓器の機能を回復させようという再生医療研究が、さまざまに進められるようになった。
その際、「細胞の分化誘導」という従来の開発概念から脱却して、「臓器の再構成に基づく分化誘導」の実現を目指したのが、谷口英樹教授らの研究グループである。そもそも臓器は、その機能を担う細胞(機能細胞)だけでなく、複数の種類の細胞が立体的配置をとることで構成され、それらが相互作用を行うことで機能している。したがって、十分に機能する細胞を得るためには、機能細胞のみの分化誘導ではなく、立体的な組織の再構成を伴う「臓器」の誘導(臓器の創出)が必要だ、というのがその基本発想である。
こうしてiPS細胞がヒトの肝臓になる
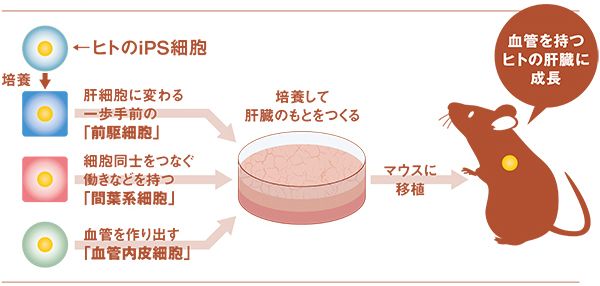
3種類の細胞がボール状に集まり「ミニ肝臓」が形成された!
研究グループはまず、「臓器の原基」(臓器の種)が胎内で形成される過程を試験管内で模倣するため、新しい細胞培養操作技術を開発した。そのうえで、ヒトiPS細胞から作製した「内胚葉細胞」(肝細胞に分化する一歩手前の「前駆細胞」)に、血管を作り出す「血管内皮細胞」と、細胞を結合させる働きなどをする「間葉系細胞」を加えて、試験管内で共培養した。その結果、48時間ほどで、未分化だった3種類の細胞がボール状に集まり、立体的な肝臓の原基(言わば、ヒトの「ミニ肝臓」)が自律的に形成されたのである。
この原基を生体(免疫不全のマウス)に移植したところ、血流を持つ血管網を再構成し、最終的には、タンパク質の合成や薬物の代謝など、人の肝臓に特徴的な機能を持つ組織へと成熟することが判明した。さらに、この原基を移植した肝不全のマウス群は、移植をしなかったマウス群に比べて、有意に生存率が改善した。このことは、生体内で分化誘導されたヒト肝細胞が肝臓としての機能を発揮し、治療効果が現れたことを示している。
こうして研究グループは、iPS細胞由来の細胞から血管網を持つ機能的なヒト肝臓を創り出すことに、世界で初めて成功したのである。
立体的なヒト肝臓原基の形成過程の写真
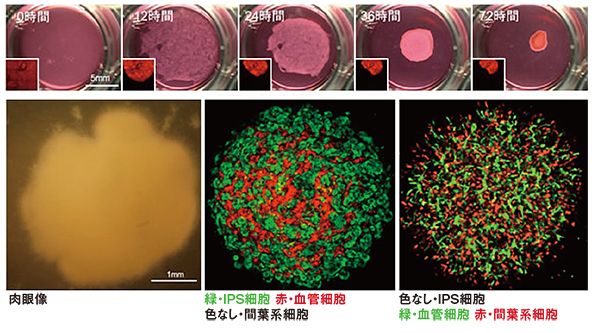
特別な条件下で未分化な3種類の細胞を共培養することにより、立体的な肝臓の原基が自律的に形成された(上段)。iPS細胞由来内胚葉細胞が効率的に肝臓の前駆細胞へと分化誘導されるとともに、血管の細胞はネットワーク様の構造を形成することが明らかになった(下段)。
臓器移植の代替治療に医薬品のスクリーニングに
谷口教授らの研究グループは、ここで開発した技術を「臓器原基移植療法」と名付け、臓器移植の代替治療として提唱している。この技術に基づく治療が実現すれば、肝移植の待機中に死亡する患者を救済することができるのだ。そのため研究グループでは、今後は臓器原基の大量製造技術や最適な移植方法の検討を重ねて、肝臓疾患の患者を対象とする再生医療の実現化を図り、肝臓以外の臓器への応用の可能性についても研究を加速させるという。
一方、本研究の成果は、日本の創薬産業にも大きく貢献する可能性がある。現在の医薬品開発に利用される細胞のうち、最も重要で市場性が高いのはヒト肝細胞で、代謝安定試験・酵素誘導など、医薬品開発でのスクリーニング(新薬候補の選別)に役立っているが、残念ながら、その供給はほぼ100%を欧米に頼っているのが現状だ。そこで、今回開発した技術によりiPS細胞由来のヒト肝細胞・肝組織を大量に製造してスクリーニングに供することができれば、日本の創薬産業の国際競争力向上に寄与すると考えられるのである。