ポイント
- これまでは、光によって誘導される遺伝子発現量は10倍程度で、暗所においても予期せず遺伝子発現が生じてしまうなど、遺伝子の機能解析に利用するには問題がありました。
- 本研究では、光を短時間、または、極めて弱く当てるだけで哺乳類細胞の遺伝子発現量を300倍に増加できる技術の開発・改良に成功しました。
- 本技術は、生体外からの光照射でも狙った場所の遺伝子発現をコントロールできる世界で最も優れた技術であり、将来的には、幹細胞の分化や疾患の発症に関連するなど、幅広い遺伝子の機能解明へと役立つことが期待されます。
内閣府 総合科学技術・イノベーション会議が主導する革新的研究開発推進プログラム(ImPACT)の合田 圭介 プログラム・マネージャーの研究開発プログラムの一環として、コロンビア大学の矢澤 真幸 アシスタントプロフェッサーの研究チーム注1)は、哺乳動物に応用可能な高性能の青色光誘導型注2)の遺伝子発現コントロールシステムを開発しました。 これまで報告されている数々の類似した技術では、青色光によって誘導される遺伝子発現効率が低いことや暗所においても予期していない遺伝子発現が生じてしまうなどの問題が生じていました。 本研究チームは、植物において花を咲かせるのに必須な光受容体を哺乳動物の遺伝子発現コントロールに応用し、様々な分子生物学的手法を駆使し、これまでの課題の解決に取り組んできました。これまでの先行研究では10倍程度の遺伝子発現の上昇が限界であったのに対し、本研究により改良された技術では同等の実験条件の哺乳動物培養細胞で最大300倍程度まで遺伝子発現を上昇させることに成功しています。さらには、培養細胞のみならずマウス個体の組織にも応用可能なことを確認しました。今後は、神経科学や幹細胞を分化する研究、ショウジョウバエ、ゼブラフィッシュなど各種の実験モデルを用いた遺伝子機能の解析、ヒトの疾患メカニズム解明など幅広い分野への貢献が期待できます。 本研究は、2017年10月10日9時(日本時間)に英国の科学雑誌『Nucleic Acids Research』オンライン速報版に掲載されます。
本成果は、以下のプログラム・研究開発課題によって得られました。
内閣府 革新的研究開発推進プログラム(ImPACT)
URL:https://www.jst.go.jp/impact/

矢澤 真幸
| プログラム・マネージャー |
合田 圭介 |
| 研究開発プログラム |
セレンディピティの計画的創出による新価値創造 |
| 研究開発課題 |
細胞検索エンジン(セレンディピター)のための計測プラットフォームおよび細胞分取技術の開発 |
| 研究開発責任者 |
矢澤 真幸
(コロンビア大学 リハビリテーション再生医療学科・薬理学科・幹細胞研究科 アシスタントプロフェッサー) |
| 研究期間 |
平成27年4月~平成29年9月 |
本研究開発プログラムでは、膨大な細胞集団から単一の目的細胞を発見する細胞検索エンジンの開発に取り組んでいます。その中で、矢澤チームは、膨大な細胞集団から目的の細胞を発見するための「細胞内活動のモニタリング技術」の開発および回収した細胞をその後利用するための「細胞内活動の遠隔コントロール技術」の開発に取り組んでいます。
<合田 圭介 プログラム・マネージャーのコメント>
本成果は、ImPACT「セレンディピティの計画的創出による新価値創造」に参画するコロンビア大学の研究チームによるものです。矢澤チームでは、膨大な細胞集団の細胞内活動をコントロールもしくはモニタリングするために必要な技術を開発しています。今回の成果は、光により細胞およびマウス個体の組織内の遺伝子発現をコントロールすることに成功しており、類似した他の技術に比べて非常に優れたもので、今後、本プログラムで開発中の高速イメージング技術を用いた細胞分析装置「セレンディピター」と組み合わせて利用することで、様々な細胞の遺伝子機能解析に大きく貢献できると考えています。
<研究の背景と経緯>
ヒトゲノムの解読によって約3万程度の遺伝子が存在することが明らかになり、それぞれの遺伝子の機能の解明が進んでいます。ゲノム上の遺伝子によって作られたタンパク質の多くは酵素などの機能を有し、様々な細胞内活動に必須であることが明らかになっています。近年、生体での遺伝子の役割を解明するための技術として、化合物や光を使って遺伝子発現量を人為的にコントロールする技術に関心が持たれています。特に、光でのコントロールは、狙った組織や器官、細胞を対象に、任意のタイミングで遺伝子発現を誘導することが極めて簡単にできるようになるため、幅広く基礎研究や医学研究に応用できると期待されています。しかしながら、光を利用した従来の技術はいずれも遺伝子発現効率が著しく低く、生体内の細胞にコントロールに必要な光が届かない、遺伝子発現量の変化が不十分で機能解明に繋がらないなど、マウスなどの実験モデル動物への応用の大きな障害になっています。そのため、弱い光で遺伝子発現量を大きくコントロールできる高性能な技術の開発が強く求められています。本チームは、米国ワシントン大学の今泉貴登准教授らが解明した植物の光受容体FKF1とその結合パートナーであるGIGANTEAの相互作用注3)に着目し、2009年に「Nature Biotechnology」で哺乳細胞内の酵素の局在や遺伝子発現のコントロールに成功したことを報告しています。しかしながら、遺伝子発現量が最大10倍程度であったため、さらなる改良が必要となっていました。
<研究の内容>
本チームでは、哺乳細胞における光誘導型の遺伝子発現技術のさらなる改良のため、光受容体FKF1の様々な突然変異タンパク質を発現させることのできるライブラリーを作成しました。そこからスクリーニングし、FKF1の変異タンパク質H105Lを発見しました(図1)。その一方で、光受容体FKF1、その結合パートナーGIGANTEA、Gal4 DNA結合領域、遺伝子発現活性化領域VP16の4つの必須の部位の組み合わせを可能な限り検証し、最適な組み合わせを発見しました(図2)。その後、他の光受容体を用いた類似した技術との比較検討を重ね、本チームが開発・改良した技術が最も優れていることを明らかにしました。また、比較対象としたCRY2/CIB1を用いた技術にも上記と同様の改良方法を適用し、顕著な改善が認められました(図3)。改良したCRY2/CIB1を用いた技術では暗所においても予期していない遺伝子発現が生じてしまう問題が未だ生じている一方、本チームの改良版の技術ではそういった問題がなく、青色光で遺伝子発現を300倍上昇させることに成功しました(図4)。そして、標的の細胞のみ光を照射することで標的細胞のみで目的の遺伝子が発現することを実証しました(図5A)。さらには、開発した光誘導型遺伝子発現システムをマウスの生体深部における遺伝子の光制御にも応用しました。具体的には、生体外からの非侵襲的な光照射方法を用いて、マウスの生体深部の臓器(本論文では肝臓)において、遺伝子発現を誘導できることを明らかにしました。この結果により、本チームの新技術を用いることでマウス個体内の組織・器官における遺伝子発現を生体外からの光照射でコントロールできることを示しています(図5B)。
<今後の展開>
上述のように本チームは、光を使って自由自在に遺伝子発現をコントロールするための技術を開発しました。他の同様の技術よりはるかに優れた本技術を使うことによって、従来では不可能であった生体(マウスなどの動物個体)の遺伝子発現を、生体外からの非侵襲的な光照射によってコントロールすることができるようになりました。本研究の成果は、神経科学や幹細胞の増殖・分化や、疾患に関わる様々な遺伝子の機能解明にも役立つことが期待できます(図6)。
<参考図>
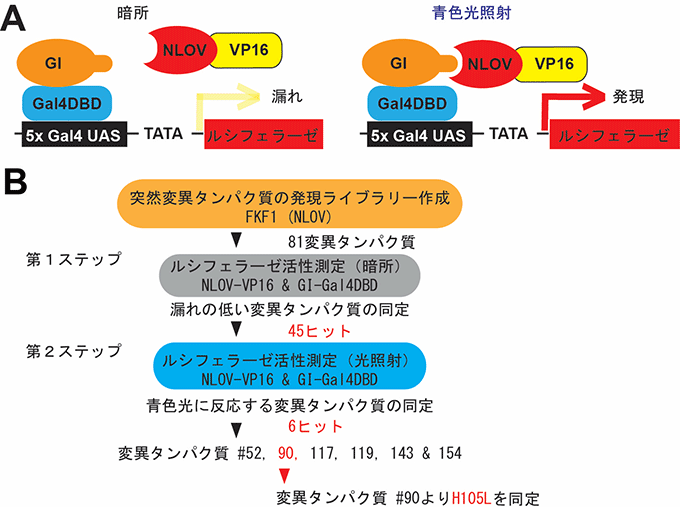
図1
FKF1(NLOV)変異タンパク質スクリーニングの流れ。
- (A)ルシフェラーゼ活性測定を用いたFKF1変異タンパク質のスクリーニングの基本デザイン。FKF1のアミノ基領域とLOV領域(NLOV)には転写活性部位VP16を融合。FKF1の結合パートナーであるGIGANTEA(GI)にGal4 DNA結合領域(Gal4DBD)を融合して、Gal4反応型ルシフェラーゼレポーターとともにHEK293T細胞に発現させスクリーニングを行った。
- (B)戦略的NLOV変異タンパク質のスクリーニングの概要。NLOVを変異タンパク質作成の鋳型として利用し計81変異タンパク質を準備した。第一ステップとして、暗所でルシフェラーゼ発現に漏れがない変異タンパク質をスクリーニングし、45変異タンパク質に発現の漏れがないことが認められた。第2ステップとして、その45変異タンパク質に青色光を照射しルシフェラーゼ活性測定を行い、計6変異タンパク質が光応答を示すことが明らかになった。そのなかの変異タンパク質#90より105番目のアミノ酸がヒスチジンからロイシンに変わっていること(H105L)を同定した。
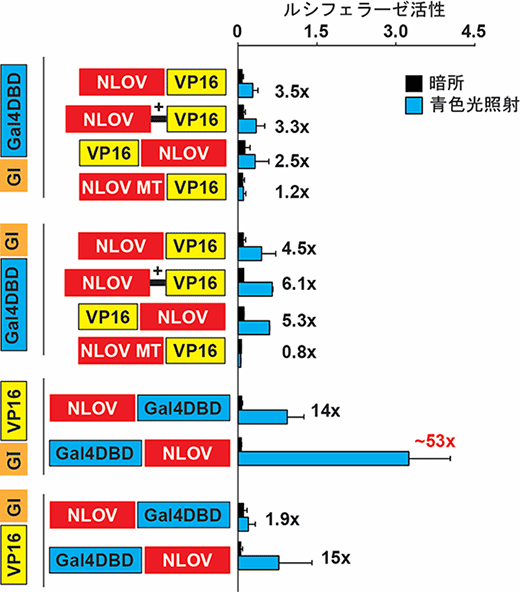
図2
ルシフェラーゼ活性測定を用いたNLOV(G128D変異タンパク質)、NLOV MT(青色光に反応しない変異タンパク質)とGI、Gal4DBD、VP16の融合の組み合わせの最適化。+はグリシン/セリンによる結合リンカーを示す。総当たりの検証により、GI-VP16とGal4DBD-NLOV(G128D)の組み合わせが最も優れていることが明らかになった。G128Dは本チームが先行研究(Yazawa et al. Nat. Biotechnol. 2009)に用いた変異タンパク質である。
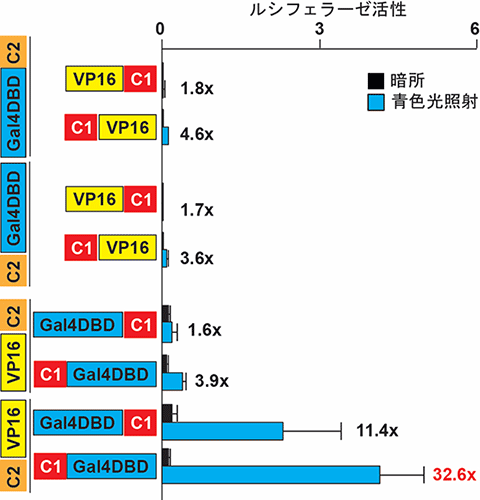
図3
ルシフェラーゼ活性測定を用いたCRY2(C2)と
CIB1(C1)、Gal4DBD、VP16の融合の組み合わせの最適化。総当たりの検証により、CRY2-VP16とCIB1-Gal4DBDの組み合わせが最も優れていることが明らかになった。
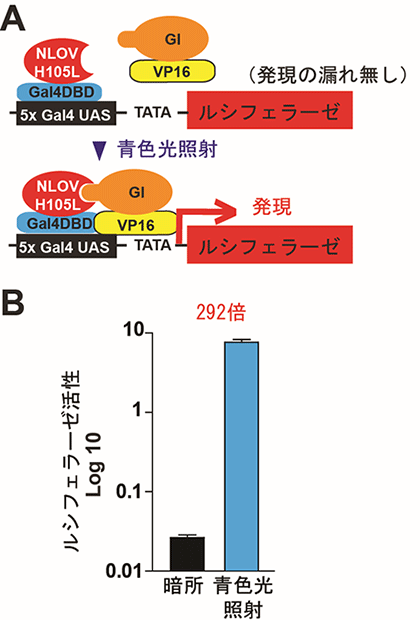
図4
- (A)改良型のGI-VP16とGal4DBD-NLOV(H105L)。
- (B)改良型のGI-VP16とGal4DBD-NLOV(H105L)を用いたルシフェラーゼ活性測定。暗所に比べ青色光を照射することでルシフェラーゼ遺伝子発現を約300倍上昇させることが明らかになった。
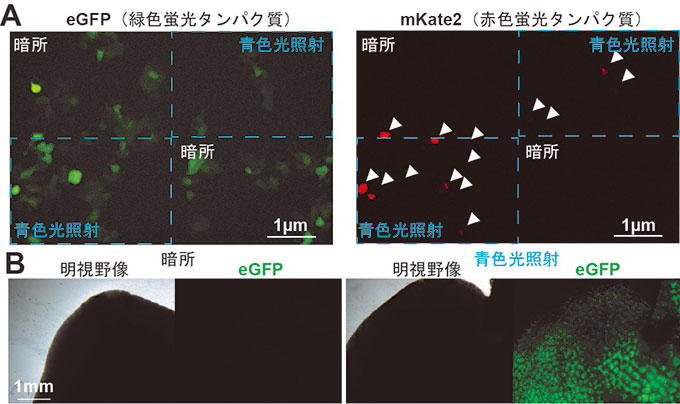
図5
- (A)改良型のGI-VP16とGal4DBD-NLOV(H105L)を用いて標的の生細胞のみに赤色蛍光タンパク質mKate2を発現させた。点線で区切られた右上と左下の区画のHEK293T細胞に青色光照射を行った。矢(白色)はmKate2を発現した細胞を示す。緑色蛍光タンパク質eGFPは改良型のGI-VP16とGal4DBD-NLOV(H105L)を発現しているすべての細胞の指標として利用。暗所の細胞にはmKate2の発現は認められなかった。
- (B)マウス個体の肝臓に改良型のGI-VP64とGal4DBD-NLOV(H105L)を発現させて、生体外から肝臓に向けて青色光を照射し、eGFPを発現させた。これにより、本チームが開発した技術がマウス個体でも応用可能なことが示された。
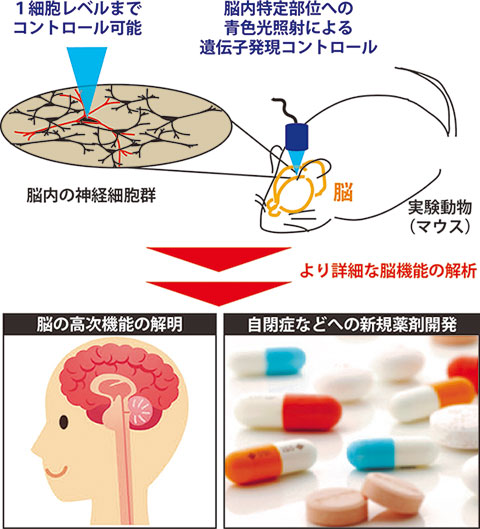
図6
脳機能解明を例とした今後の展望。本研究により、標的とする細胞における目的遺伝子の発現量を光を用いて時空間的な精度で強力に増加させられるようになったことで、これまでよりも詳細な脳機能の解析ができるようになり、将来的には、脳の高次機能の解明や自閉症などへの新規薬剤開発へと進展することが期待される。
<用語解説>
- 注1) 研究チーム
- 本発表の研究チームメンバーは、コロンビア大学 メディカルセンター 矢澤 真幸(アシスタントプロフェッサー)、 Jose Quejada(大学院生)、Seon-hye Emily Park(研究技官)、Fan Shi(研究補助員兼中国からの大学院留学生)、河野 風雲(ポスドク研究員)らで構成され、ImPACTプログラムの一環として、本研究を遂行した。
- 注2) 青色光誘導型
- シロイヌナズナ(Arabidopsis thaliana)が有する青色光受容体(Flavin Kelch-repeat F-box1:FKF1)とその結合タンパク質(GIGANTEA)にプロテインエンジニアリングを施して開発された青色光誘導型タンパク結合スイッチ。青色光を受容すると、互いに結合する。 本研究チームにより開発・報告された(Yazawa et al. Nat. Biotechnol.2009)。これらのツールは光遺伝学分野に使われている。光遺伝学とは光学(optics)と遺伝学(genetics)の方法論を融合させた学問分野であり、オプトジェネティクス(optogenetics)とも呼ばれている。遺伝子として保存された光応答型のタンパク質群を使って、細胞内のイオン濃度やタンパク質の挙動などを光でコントロールすることにより、生命現象を明らかにすることを目的とする。2005年、光駆動型のイオンチャネル(チャネルロドプシン)を使って、神経細胞の活動を光でコントロールする技術が報告されたのをきっかけに、脳神経科学の分野で爆発的に広まった。現在では、チャネルロドプシン以外にもさまざまなツールが開発され、生命科学の新たな研究手法として幅広い分野から注目されている。
- 注3) 光受容体FKF1とその結合パートナーであるGIGANTEAの相互作用
- 2007年に今泉准教授らのグループによって解明された植物の開花に必須な分子機能。「Science誌」に掲載された(Sawa et al. Science 2007)。
<論文情報>
| タイトル |
“Optimized light-inducible transcription in mammalian cells using Flavin Kelch-repeat F-box1/GIGANTEA and CRY2/CIB1”
(Flavin Kelch-repeat F-box1/GIGANTEAおよびCRY2/CIB1を用いた光による哺乳細胞の転写制御技術の改良) |
| 著者名 |
Jose R. Quejada, Seon-Hye E. Park, Daniel W. Awari, Fan Shi, Hannah E. Yamamoto, Fuun Kawano, Juergen C. Jung and Masayuki Yazawa |
| 掲載誌 |
Nucleic Acids Research |
| doi |
10.1093/nar/gkx804 |
<お問い合わせ先>
<研究に関すること>
コロンビア大学 メディカルセンター
リハビリテーション再生医療学科、薬理学科、幹細胞研究科
アシスタントプロフェッサー:矢澤 真幸(ヤザワ マサユキ)
Tel:+1-212-305-1052
E-mail:
<ImPACT事業に関すること>
内閣府 革新的研究開発推進プログラム担当室
〒100-8914 東京都千代田区永田町1-6-1
Tel:03-6257-1339
E-mail:
<ImPACTプログラム内容およびPMに関すること>
科学技術振興機構 革新的研究開発推進室
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-6380-9012 Fax:03-6380-8263
E-mail: 
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: