ポイント
- 安定アミドは化学的に反応しにくく、燃料や医薬品合成の中間体として重要なアミンやアルコールに効率よく変換(水素化)する触媒がなかった。
- 低温で低水素圧の温和な条件で反応が進み、副生成物が少なく、多くの種類のアミドを目的のアミンやアルコールのみに変換する触媒を開発した。
- 天然に豊富な安定アミドを炭素資源として活用することで、炭素循環型社会の実現に貢献できると期待される。
JST 戦略的創造研究推進事業において、名古屋大学 大学院理学研究科の斎藤 進 教授らの研究グループは、多彩な安定アミド注1)をアミンやアルコールに効率よく変換(水素化注2))できる触媒を開発しました。
ナイロンやケブラーに代表される安定アミドは、人工高分子をはじめ、石油化学工業において多種多様に生産され、身の周りに豊富に存在する物質です。この安定アミドを炭素資源として、燃料や医薬品などに多く利用されるアルコールやアミンに変換する水素化は、炭素循環社会の実現に資する有効な反応です。そのため、安定アミドを水素化する触媒の開発に世界中の研究者が挑んできましたが、安定アミドは化学的に反応しにくく、その水素化には大きなエネルギーが必要でした。また、水素化できる安定アミドの種類は、天然資源にはあまり存在しない反応性の高い1~2種類の活性アミド注1)に限られていました。
本研究グループは、新しいルテニウム錯体注3)を開発し、安定な水素分子と安定アミドの両方を反応しやすい状態にする新しい安定アミドの水素化触媒を見いだしました。この触媒によって、水素化できる安定アミドの種類が大幅に増え、その数は25種類以上です。さらに、この触媒を用いて、二酸化炭素由来の安定アミドを水素化し、これまでにない高効率でメタノールが得られることから、本触媒法は簡便なメタノールの合成法として、二酸化炭素の資源利用にも貢献すると期待されます。
本触媒を活用することで、バイオマス資源注4)である安定アミドをアミンやアルコールに変換し、炭素資源として有効利用できることが期待されます。
本研究成果は、2017年5月16日(英国時間)に英国科学誌「Scientific Reports」のオンライン版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 先導的物質変換領域(ACT-C)
| 研究領域 |
「低エネルギー、低環境負荷で持続可能なものづくりのための先導的な物質変換技術の創出」
(研究総括:國武 豊喜 九州大学 高等研究院 特別主幹教授) |
| 研究課題名 |
「分子触媒と固体触媒のクロスオーバー領域の精密化に基づく二酸化炭素の資源化法の開拓」 |
| 研究代表者 |
斎藤 進(名古屋大学 大学院理学研究科 教授) |
| 研究期間 |
平成24年10月~平成30年3月 |
上記研究課題では、光エネルギーもしくは熱エネルギーを用いてCO2を資源化するための新しい触媒化学的方法論の開発を目指しています。
<研究の背景と経緯>
ナイロンやケブラーに代表される安定アミドは、今日の生活を支える石油化学工業で大量に生産されるだけでなく、医薬品として用いられる分子の重要な骨格にも多く見られます。また、ペプチド化合物やたんぱく質などとして天然にも豊富に存在します。
近年、安定アミドをアミンやアルコールに変換し、再生可能な炭素資源として有効利用することが求められています。アミンやアルコールは溶媒や燃料としての利用をはじめ、医薬品や農薬、香料、化粧品、洗剤、繊維の原料になるなど、その用途は多種多様で、生活に必要不可欠な化合物です。
安定アミドをアミンやアルコールに変換する上で、最も理想的な方法の1つが水素化です(図1上段)。水素化は、水素ガス(水素分子)の2つの水素原子を無駄なく反応物質に結合させる方法で、安定アミドからアミンやアルコールに変換する際に、廃棄物を出さないクリーンな変換方法です。安定アミドは非常に反応しにくい化合物(図1中段)で、最も水素化が困難なカルボニル化合物注5)として知られており、これまで安定アミドの水素化には高温と高水素圧といった過酷な条件が必要とされてきました。しかし、高温と高水素圧条件では副反応が生じやすく、目的のアミンやアルコールのみを合成できないという問題点がありました。
<研究の内容>
斎藤教授らの研究グループは、多くの種類の安定アミドを水素化してアミンやアルコールに変換できる触媒の開発に取り組みました。触媒として注目したのは「金属錯体」と呼ばれる金属と有機分子(配位子注6))による複合体です。特に、ルテニウム(Ru)という金属を用いた金属錯体は、水素化によって優れた性能を示すものがたくさんあります(図2上段)。1973年にノーベル化学賞を受賞したジェフリー・ウィルキンソン 教授らによって初めて合成されたルテニウム錯体が、「金属錯体を用いる水素化」の歴史の基礎を築きました。2001年にノーベル化学賞を受賞した野依 良治 教授もルテニウム錯体を水素化触媒として用い、当時不可能といわれた「分子の右手型と左手型のつくり分け」に成功しています。
本研究グループは長年にわたり、さまざまなルテニウム錯体について安定アミドの水素化触媒としての性能を研究してきました(図2中段)。2013年に斎藤教授らはリン(P)原子1つと窒素(N)原子1つからなるPN配位子を2つ持つルテニウム錯体「(PN)2Ru」を用いて安定アミドの水素化を実現しましたが、反応には高温と高水素圧条件が必要でした(Tetrahedron Letters 2013, 54, 2674)。これではルテニウムから配位子が外れやすく、触媒は容易に壊れて、その機能(活性)を失ってしまいます。
改良の結果、PN配位子を2つつなげた新しい配位子「PNNP」(図2下段)を持つルテニウム錯体「(PNNP)Ru錯体」を用いたところ、これまでよりも大幅に効率的に(最も温和な条件では温度60℃、水素圧5気圧)安定アミドを水素化し、アミンやアルコールに変換できることを発見しました。「PNNP」の4つの元素がルテニウムに結合し、「(PNNP)Ru錯体」がつくられますが、特にPNNPのNN(すなわちN-Ru-N部分)が触媒にとって、非常に重要な構造の一部であることを証明しました(図2下段)。同じNNでもビピリジン注7)骨格を持つことが重要で、フェナントロリン注8)骨格にすると水素化がほとんど進行しなくなります。
さらに、水素化触媒としての性能を大幅に向上させるため、ルテニウム錯体につながったリン原子に結合する炭素の鎖の形を詳細に調べました。その結果、リン原子にイソプロピル基注9)やシクロヘキシル基注9)など立体的に大きなサイズの炭素の鎖が結合している場合に、ルテニウム錯体が安定アミドの水素化触媒として非常に優れた性能を示すことを見いだしました(図2下段)。イソプロピル基を持つ新しいルテニウム錯体は、ウィルキンソン教授や野依教授らが用いた錯体では全く機能しない温和な反応条件でもアミドを水素化できる、非常に有効な触媒となることが分かりました。
金属錯体を用いたアミド基の水素化触媒のこれまでの成功例は、より反応しやすい1~2種類の活性アミドにほぼ限られていました。これまでの方法では、炭素-窒素結合を弱める目的でアミド結合の窒素原子にフェニル基などの芳香環を結合させた誘導体を用いたり、または、アミド基の炭素に結合した炭素の鎖に特殊な元素や官能基を導入したりすることで、アミド基が反応しやすいように分子設計がなされていました(図1下段)。しかし、これら活性アミドの構造は、天然に存在する安定アミドとは大きく異なるため、再生可能資源由来の安定アミドの水素化にはほとんど役に立ちません。これに対して、本触媒は、再生可能資源であるたんぱく質の構成成分オリゴペプチド骨格やナイロン系高分子などの大きい安定アミドを含め25種類以上の安定アミドを高効率で水素化できます。二酸化炭素由来の安定アミド(ホルムアミド注1))を水素化することによってメタノールも得られることから、本触媒法は簡便なメタノールの合成法として、二酸化炭素の資源利用にも貢献すると期待されます。さらに、温和な反応条件で反応が進行するため、副生成物が少なく、目的のアミンやアルコールのみを効率よく得られます。本触媒は、ウィルキンソン教授や野依教授らが開発した触媒が得意とするオレフィン化合物注10)よりも安定アミドを優先して水素化することも判明しました。
本触媒がなぜ安定アミドの水素化触媒として優れた機能を発揮するのかについても調べました。水素化に有効な温度や水素圧環境下で、ルテニウム原子と、サイズの大きな炭素の鎖を持つリン原子、およびビピリジンでつくる「大きなサイズの炭素の鎖に覆われたルテニウム-ビピリジン骨格」の構造そのものが、アミド基の水素化の前に水素化されて、触媒として機能する上で重要な最初の構造(図3上段)に変化することを見いだしました。その後、さらなる構造の変化によって多彩な触媒がつくられ、安定な水素分子と安定アミドの両方が反応しやすい状態になっていることが分かりました(図3下段)。実際にはさまざまな構造のルテニウム錯体が温度や水素圧に応じて発生し、各々が水素化に寄与していると考えられます。そして、どの構造の触媒も頑丈な構造を持つため活性を失いにくく、「1つのルテニウムで目的の生成物をいくつつくれるか」を示す「触媒回転数」は最高で8,000程度と極めて高い値を示しました。
<今後の展開>
本触媒は、温和な条件下で安定アミドを高効率でアミンやアルコールに変換する水素化を可能にしました。さらに、優れた触媒活性を示すために鍵となる触媒の形や触媒の設計の仕方を見いだしました。本研究成果は、安定アミドを水素化するための、さらに活性の高い触媒を開発する基盤となると考えられます。そして、天然に豊富に存在する安定アミドを再生可能資源として活用することで持続可能な炭素循環社会に寄与できると期待されます。安定アミドを二酸化炭素から合成する方法は野依 良治 教授の方法注1)などが知られており、その技術と本触媒を組み合わせることにより、二酸化炭素をメタノールとして資源化することにも貢献できると期待されます。
<参考図>
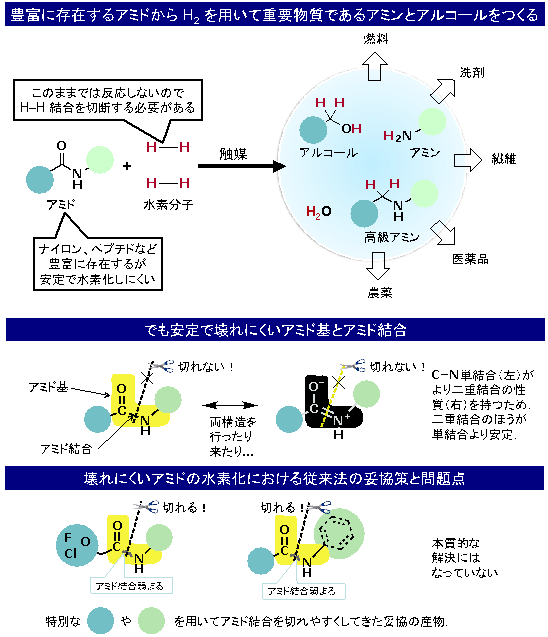
図1 アミドからアミンとアルコールへの水素化反応と従来法の課題
- 上段:アミドに対して2つの水素分子が反応しアルコールとアミン、もしくは高級アミン注11)と水が生成される。アミンとアルコールは多目的に使用できる重要な物質である。アミドの水素化の鍵は、H-H結合を切断することとアミドの反応性を触媒の働きで高めることの2点である。青緑色や黄緑色の丸は、任意の炭素の鎖を指す。
- 中段:アミドの性質。アミド結合は安定で活性が低く、切れにくい。
- 下段:従来法では、アミド結合を弱めるための特別な炭素の鎖をアミド基に故意に結合させて活性アミドとして使ってきた。これでは多彩なアミド(特に安定アミド)の水素化を実現する上で本質的な解決法にはなっていない。
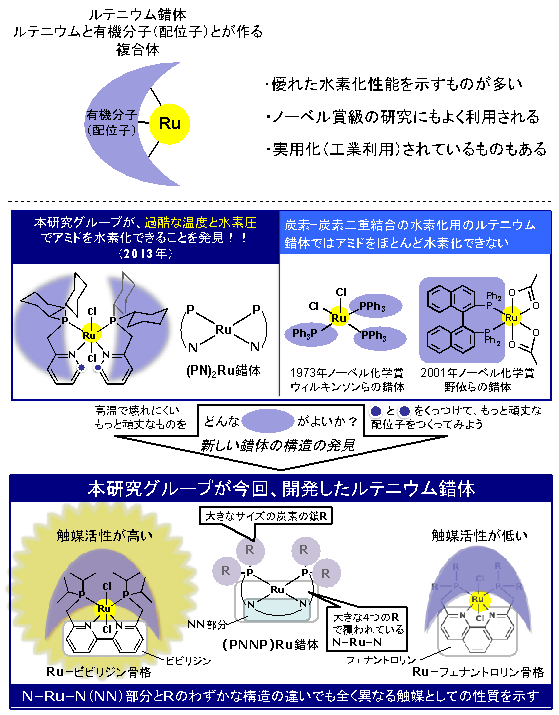
図2 安定アミドの水素化触媒として有能なルテニウム錯体
- 上段:ルテニウム錯体の概念図。
- 中段:本研究グループの初期(2013年)の発見と歴史的マイルストーンであるルテニウム錯体との比較。紫色部分は配位子を表す。
- 下段:本研究グループが今回開発した(PNNP)Ru錯体。金属錯体のわずかな構造の違い(NNにあたるビピリジンとフェナントロリン(すなわちN-Ru-N部分)の違いやリン上の炭素の鎖Rの種類)で全く異なる触媒活性を示す。精密な分子設計の重要性が分かる。
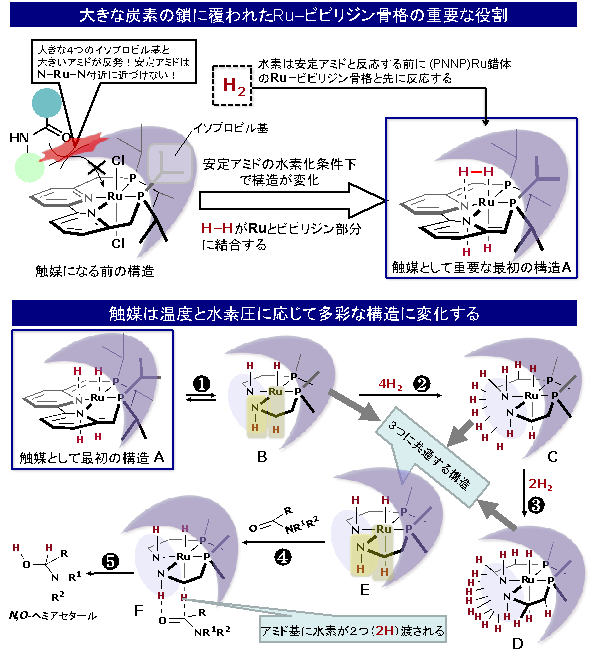
図3 安定アミドの水素化
水素化条件下でのルテニウム錯体の構造の移り変わり
- 上段:開発したルテニウム錯体は水素化反応の条件下で、触媒として機能する上で重要な最初の構造Aへと変化する。このとき、Aの「サイズの大きなイソプロピル基に覆われたRu-ビピリジン骨格」がH-H分子を吸着している。
- 下段左上:構造Aの窒素(N)とルテニウム(Ru)が協力して働き、H-Hと結合をつくり、このH-H結合を切って、H-N-Ru-Hという構造B(黄色)をつくる(過程❶)。
- 下段右・中央あたり:その後、温度や水素圧に応じて複数のH2分子が、もとはRu-ビピリジン骨格であった部分に吸着され構造Cや構造Dをつくる(過程❷および❸)。それら以外にもさまざまな触媒の構造の可能性があるが、少なくともここに挙げた3つの構造B、C、Dに共通するのは「サイズの大きなイソプロピル基に覆われたH-N-Ru-H骨格E(黄色)」であることが分かる。
- 下段左下:アミドRCONR1R2のC=Oと構造EのH-N-Ru-Hとの間で結合が形成され構造Fが生じる(過程❹)。H-N-Ru-HからC=Oへ水素原子Hの受け渡しが円滑に起こり、N,O-ヘミアセタールが生じる(過程❺)。ここから炭素-窒素結合の切断によるアルデヒドとアミンの生成、H2とアルデヒドとの反応を経てアルコールが形成される。一方、脱水反応、イミン生成、H2とイミンとの反応を経れば、高級アミンが形成される。
<用語解説>
- 注1) アミド(安定アミド、活性アミド、ホルムアミド)
- 分子式RCONR1R2で表される化合物の総称。R、R1、R2は炭素鎖もしくは水素原子を表す(図1参照)。アミドは、反応しにくい安定アミドと反応しやすい活性アミドに分類される。中でもホルムアミドとは、HCONR1R2で表される構造の総称。ここではN,N-ジメチルホルムアミド(DMF:(CH3)2NCHO)のことを指す。野依DMF合成法とは、野依 良治 教授(2001年ノーベル化学賞受賞)を中心に開発された方法で、超臨界二酸化炭素(scCO2)とジメチルアミン((CH3)2NH)と水素分子(H2)から、水のみを副生物(廃棄物)としてDMFをつくる方法。反応式では、CO2 +(CH3)2NH + H2 → (CH3)2NCHO + H2Oと表される。野依教授らによって英国科学誌「Nature」に1994年に発表された、scCO2とH2とトリエチルアミン((C2H5)3N)を用いてギ酸アミン塩を合成する方法を改良したもの(J.Am.Chem.Soc.1996,118,344)。
- 注2) 水素化
- 対象となる化合物を、水素分子を用いて還元する(電子を入れる)反応。水素分子H-Hの2つのH(電子を1つ持つ)が両者とも対象となる化合物に結合することで2つの電子が入ることになる。
- 注3) ルテニウム錯体
- 金属と非金属の原子が結合した構造を持つ化合物を金属錯体という。その中で、有機分子が配位子としてルテニウム原子に結合した構造を持つ錯体をルテニウム錯体という。
- 注4) バイオマス資源
- 生物由来の資源。廃棄物系バイオマスや未利用バイオマス、資源作物(エネルギーや製品の製造を目的に栽培される植物)に分類できる。廃棄物系バイオマスとしては、廃棄される紙やバイオディーゼル系廃棄物、家畜排せつ物、食品廃棄物、建設発生木材、製材工場残材、黒液(パルプ工場廃液)、下水汚泥、し尿汚泥などがある。未利用バイオマスとしては、稲わらや麦わら、もみ殻、林地残材(間伐材や被害木)などがある。資源作物としては、さとうきびやとうもろこしなどのでんぷん、糖質系作物やなたねなどの油糧作物が挙げられる。化学原料や工業原料、液体燃料としても利用できるが、石油などの化石燃料と違い枯渇しない。また、大気汚染物質の発生量が少ないという性質も持つ。
- 注5) カルボニル化合物
- 炭素-酸素二重結合(C=O)を持つ有機化合物の総称。
- 注6) 配位子
- 金属に結合する有機分子を配位子という。
- 注7) ビピリジン
- 芳香族化合物であるピリジン(C5H4N)2分子が、その窒素原子のすぐ隣の炭素原子同士で互いに結合したもの。分子式2,2’-(C5H4N)2で表される(図2下段参照)。
- 注8) フェナントロリン
- ビピリジン構造を持つが、そのビピリジンに炭素-炭素二重結合(HC=CH構造)が付け加わったもの(図2下段参照)。
- 注9) イソプロピル基、シクロヘキシル基
- 炭素の鎖の一種。イソプロピル基は分子式(CH3)2CHで、シクロヘキシル基はC6H11で表される。いずれも炭素(C)と水素(H)からなる原子団で、すべての結合がC-C単結合とC-H単結合からなる。
- 注10) オレフィン化合物
- 炭素-炭素二重結合を炭素の鎖に持つ化合物の総称。
- 注11) 高級アミン
- アミンは、炭素の数がより少ない低級アミン(R1NH2で表される1級アミンなど)と、炭素の数がより多い高級アミン(R1R2R3Nで表される3級アミンなど)に分類される。R1、R2、R3、は任意の炭素の鎖を表す。今回は異なる水素化条件で得られるアミンの種類がより高級な場合に本文中では高級アミンと書いている。より低級なアミンとの相対的な違いを明確にする目的で便宜的に使っている。
-
<論文情報>
“Multifaceted catalytic hydrogenation of amides via diverse activation of a sterically confined bipyridine–ruthenium framework”
(立体的な制限下に置かれたルテニウム-ビピリジン骨格の多様な活性化によって実現した多種多彩なアミドの水素化)
doi: 10.1038/s41598-017-01645-z
著者:Takashi Miura, Masayuki Naruto, Katsuaki Toda, Taiki Shimomura and Susumu Saito*(*責任著者)
<お問い合わせ先>
<研究に関すること>
斎藤 進(サイトウ ススム)
名古屋大学 大学院理学研究科 物質理学専攻 教授
〒464-8601 愛知県名古屋市千種区不老町
Tel:052-789-5945 Fax:052-789-5945
E-mail:
<JST事業に関すること>
古川 雅士(フルカワ マサシ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail:
名古屋大学 総務部 広報渉外課
〒464-8601 愛知県名古屋市千種区不老町
Tel:052-789-2699 Fax:052-788-6272
E-mail: