ポイント
- 脳梗塞の再生治療の実現化に向け、梗塞部位に新たな血管を誘引する技術開発が望ま れていた。
- 化学と生物学の分子合成技術を組み合わせて、脳梗塞部位に血管を誘引するスポンジ形状の生体材料を開発した。
- 血管の誘引は、損傷した脳を修復・再生させる再生医療への展開が期待される。
JST 戦略的創造研究推進事業において、東京医科歯科大学 脳統合機能研究センターの味岡 逸樹 准教授らは、脳梗塞領域に血管を誘引するスポンジ形状の人工細胞足場を開発しました。
脳梗塞は、脳の血管が詰まり、酸素や血液の供給が遮断され、脳のニューロン注1)が壊れる疾患で、運動障害や言語障害などを引き起こします。これら失われた機能を回復させる治療である、脳梗塞の再生治療の実現化には、ニューロンの死を最小限に抑え、損傷した脳を修復し、再生させるために新たな血管を誘引する必要があります。しかし、脳梗塞部位で局所的に新たな血管を誘引する方法はなく、それを可能にする技術開発が望まれていました。
味岡准教授らは、化学と生物学の分子合成技術注2)を用いて、血管を誘引する機能を持つたんぱく質を結合させた、スポンジ形状の人工細胞足場を開発しました。さらに、マウス脳梗塞モデルに移植し、脳梗塞領域に血管が誘引されることを明らかにしました。
本手法を用いることで、損傷した脳を修復し、再生させる再生医療への展開が期待されます。
本研究は、東京医科歯科大学 脳統合機能研究センターの押川 未央 特任助教と岡田 桂 研究支援者、名古屋市立大学 大学院医学研究科の澤本 和延 教授と金子 奈穂子 講師と共同で行ったものです。
本研究成果は、2017年5月10日(ドイツ時間)にドイツ科学誌「Advanced Healthcare Materials」のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業
| 研究領域 |
「分子技術と新機能創出」
(研究総括:加藤 隆史 東京大学 大学院工学系研究科 教授) |
| 研究課題名 |
「低酸素状態で構造変換するタンパク質を用いる脳再生デバイスの創製」 |
| 研究者 |
味岡 逸樹(東京医科歯科大学 脳統合機能研究センター 准教授) |
| 研究実施場所 |
東京医科歯科大学 脳統合機能研究センター |
| 研究期間 |
平成26年10月~平成30年3月 |
<研究の背景と経緯>
脳は一度損傷を受けると再生しない組織だと考えられていました。例えば、脳の病気の1つである脳梗塞は、脳の血管が詰まり、酸素や血液の供給が遮断され、脳のニューロンが死ぬ疾患です。障害されたニューロンが手足の運動を制御するニューロンであれば、手足の麻痺が起こり、自然治癒力ではほとんど回復しません。しかし、私たち哺乳類の脳にも潜在的な再生能力が秘められていることが、近年の研究で明らかになってきました。現在の治療法には薬物療法などがありますが、発症から数時間以内に投与しなければ治療効果が得られないという問題点があり、脳梗塞領域に新たな血管を導き、脳の潜在的な再生能力を引き出す治療法の開発が期待されていました。
<研究の内容>
研究グループは、血管内皮細胞の足場として機能するラミニン注3)たんぱく質を利用して、スポンジ形状の人工細胞足場を作製しました。血管を誘引する機能を持つ血管内皮細胞増殖因子(VEGF)注4)を人工足場に結合させ、VEGF結合ラミニンスポンジを開発しました。この人工足場をマウス脳梗塞モデルの脳梗塞領域に移植し、VEGF結合ラミニンスポンジが血管新生能を持つことを明らかにしました。
VEGFの生物活性を損なわずにVEGFをラミニンスポンジに結合させるために、コバルトイオンとアミノ酸の1つであるヒスチジンのアフィニティー結合注5)を利用しました。試験管の中で分子をつなぐ化学合成の手法でラミニンスポンジの表面にコバルトイオンを結合させ、細胞に分子を作らせる遺伝子工学の手法でVEGFたんぱく質のC末端にヒスチジンを付加しました。これらのアフィニティー結合能を利用して、VEGF結合ラミニンスポンジを作製しました(図1)。
マウス脳梗塞モデルによる実験では、脳梗塞処理3日後に、脳梗塞領域へVEGF結合ラミニンスポンジを移植し、7日後に血管誘引能を評価しました。VEGFを結合していないラミニンスポンジ(コントロール)を移植した場合(図2右)、新生血管がほとんど検出されなかったのに対し、VEGF結合スポンジを移植した場合は(図2左)、脳梗塞領域で顕著な新生血管が認められました。
<今後の展開>
新たな血管形成は損傷組織の修復・再生に必須のステップであり、今後は、開頭手術を必要としない非侵襲的な人工細胞足場を開発することや、再生しないと考えられている損傷脳を、修復し再生させる再生医療へと展開させることを目指します。
<参考図>
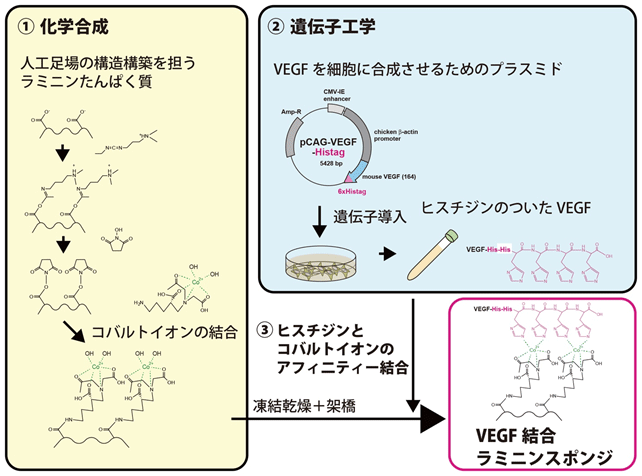
図1 化学合成(化学)と遺伝子工学(生物学)の手法を組み合わせて作製したVEGF結合ラミニンスポンジ
- ① 化学合成の手法でラミニンスポンジの表面にコバルトイオンを結合(左)
- ② 遺伝子工学の手法でVEGFタンパク質のC末端にヒスチジンタグを付加(右上)
- ③ アフィニティー結合能を利用して、VEGF結合ラミニンスポンジの作製(右下)。
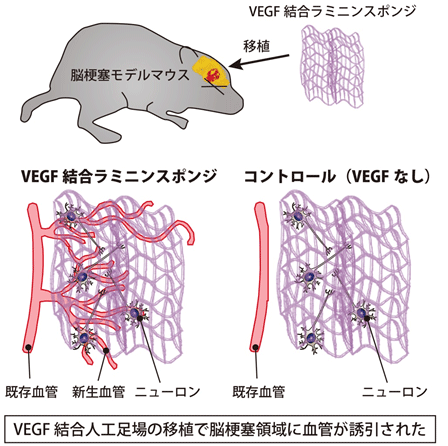
図2 脳梗塞領域におけるVEGF結合ラミニンスポンジの血管新生能
<用語解説>
- 注1) ニューロン
- 脳を構成する最も重要な細胞の1つで神経細胞と呼ばれる。入力刺激を受け取り、活動電位を発生させ、接続するニューロンに情報を伝達する細胞である。単一の細胞として機能するのではなく、他のニューロンと接続し、神経回路を形成して機能を発揮する。例えば、手足の運動を制御する神経回路を構成するニューロンが死ぬと、その回路が破綻し、手足の運動障害が起こる。
- 注2) 分子合成技術
- 機能的な分子を合成する技術で、試験管の中で分子を合成する化学合成がよく知られている。一方で、生物は生存に必要な分子を自分自身で合成する能力を持っており、この能力を利用して人為的に分子を合成させる遺伝子工学も知られている。たんぱく質医薬品の多くは遺伝子工学の手法で作られており、研究者がたんぱく質の設計図を化学合成が容易なDNAで設計・合成し、細胞がその設計図に従ってたんぱく質を合成する。
- 注3) ラミニン
- 細胞接着活性を持つたんぱく質で、血管内皮細胞などの増殖や遊走に必要な細胞足場として機能する。
- 注4) 血管内皮細胞増殖因子(VEGF)
- 血管内皮細胞の表面にある受容体に結合し、増殖や遊走などの生物活性を持つ。既存の血管から新たに血管を誘引するのに最も重要なたんぱく質だと考えられている。
- 注5) アフィニティー結合
- 分子間の特異的な結合相互作用。ヒスチジンとコバルトイオンの結合では、ヒスチジンのイミダゾール環がコバルトイオンを強く結合する性質を利用している。
<論文情報>
“Affinity-Immobilization of VEGF on Laminin Porous Sponge Enhances Angiogenesis in the Ischemic Brain”
(VEGFをアフィニティー結合させたラミニンスポンジが虚血脳の血管新生を促進する)
doi: 10.1002/adhm.201700183
<お問い合わせ先>
<研究に関すること>
味岡 逸樹(アジオカ イツキ)
東京医科歯科大学 脳統合機能研究センター 准教授
〒113-8510 東京都文京区湯島1-5-45
Tel:03-5803-4972 Fax:03-5803-4716
E-mail:
<JST事業に関すること>
中村 幹(ナカムラ ツヨシ)
科学技術振興機構 戦略研究推進部 グリーンイノベーショングループ
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3525 Fax:03-3222-2066
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail:
東京医科歯科大学 総務部 総務秘書課 広報係
〒113-8510 東京都文京区湯島1-5-45
Tel:03-5803-5833 Fax:03-5803-0272
E-mail: