ポイント
- 細胞内には、コレステロールが集まる脂質ラフト注1)と呼ばれる構造があり、病気による生体内の酸性環境との関係が注目されています。そのため、細胞の環境に応じた脂質ラフトの動きを詳しく調べる手法が求められています。
- 本研究では、コレステロールに小さな目印を結合させた分子を開発し、この分子を細胞に取り込ませた状態で、化学反応によって特定の分子振動を起こす化学構造へと変化させ、その分子振動を検出することに成功しました。また、この反応が酸性環境下でより生じやすいことを見出しました。
- 今回開発した分子は、特定のタイミングにおいて酸性環境下にある脂質ラフトを検出する新しいプローブ注2)であり、この分子を用いて脂質ラフトと病気の関係を細胞レベルで調べることで、新しい診断法や治療法、医薬品などの開発につながると期待されます。
東京大学 先端科学技術研究センターの岡本 晃充 教授、山口 哲志 講師らの研究グループは、内閣府 総合科学技術・イノベーション会議が主導する革新的研究開発推進プログラム(ImPACT)「セレンディピティの計画的創出による新価値創造」(合田 圭介 プログラム・マネージャー)の一環として、望みのタイミングで分子振動が起こらない化学構造から分子振動を起こす化学構造へ変化させる『スイッチオン』が可能な新しい生体分子検出法を開発しました。
細胞膜上のコレステロール密度が高い『脂質ラフト』と呼ばれる場所には、さまざまな病気に関わるタンパク質が存在していることが知られており、その動きを詳しく調べる手法が求められています。また、近年、病気による生体内の酸性環境との関係も注目されています。通常は、脂質ラフトのような細胞内構造を検出するために蛍光分子を目印としますが、コレステロールのような比較的小さな生体分子に大きな蛍光分子を結合させると、生体分子としての性質が大きく変わってしまいます。そこで、非常に小さなアルキン(炭素-炭素3重結合)を目印とし、アルキンが発するラマン散乱光注3)を用いて検出する方法が注目されています。しかし、これまでは目印となるアルキンが常に検出されてしまい、特定部位、あるいは特定環境を区別して観察することはできませんでした。
本研究グループは、アルキンを目印とする新しいコレステロール類似体注4)を開発し、望みのタイミングでスイッチオンできることを実証しました。開発した分子を細胞内に取り込ませ、変換反応でスイッチオンにし、高感度なラマン散乱顕微鏡で観察したところ、弱酸性環境下にあるコレステロール類似体のみを可視化することに成功しました。
今後、本手法を用いて酸性環境下の脂質ラフトの動きを明らかにすることにより、全く新しい仕組みによる創薬や診断、治療への可能性が開かれると期待されます。
本研究成果は、2017年1月24日10時(英国時間)にネイチャー・パブリッシング・グループ(NPG)の電子ジャーナル「Scientific Reports」で公開されます。
本成果は、以下のプログラム・研究開発課題によって得られました。

岡本 晃充

山口 哲志
内閣府 革新的研究開発推進プログラム(ImPACT) https://www.jst.go.jp/impact/
| プログラム・マネージャー |
合田 圭介 |
| 研究開発プログラム |
セレンディピティの計画的創出による新価値創造 |
| 研究開発課題 |
化学的1細胞遺伝子解析技術の開発 |
| 研究開発責任者 |
岡本 晃充(東京大学 先端科学技術研究センター 教授) |
| チームメンバー |
山口 哲志(東京大学 先端科学技術研究センター 講師) |
| 研究期間 |
平成27年4月~平成29年3月 |
本研究開発課題では、膨大な細胞集団から単一の目的細胞を発見する細胞検索エンジンの開発に取り組んでいます。その中で、岡本チームは、新規の機能を有している細胞を、化学的なアプローチでエピゲノム・トランスクリプトームレベルで視覚的に効率よく拾い上げる方法の開発に取り組んでいます。
<合田 圭介 プログラム・マネージャーのコメント>
本成果は、ImPACT「セレンディピティの計画的創出による新価値創造」にて細胞刺激技術を開発する岡本チームが中心となって開発し、細胞計測技術を開発する鈴木チームとの共同で実証したものです。今回岡本チームが開発したプローブは、多くの病気との関連性が指摘されている脂質ラフトの働きを調べる新しい手法として期待されます。本研究成果は、膨大な数の細胞集団から希少な細胞を見つけ出す細胞検索エンジン「セレンディピター」の用途を広げる重要な成果であると考えています。
<研究の内容>
細胞膜上にはコレステロールを豊富に含む部分があり、『脂質ラフト』と呼ばれています。脂質ラフトには、さまざまな病気に関わるシグナル分子を感受するタンパク質があり、細胞の寿命や動き、栄養の取り込みや分泌など多岐に渡る現象を仲介しています。また、これらのタンパク質と周りの脂質ラフトの大きさや配置には相関があることが報告されており、脂質ラフトが細胞内にどのように分布して存在しているかに応じて、タンパク質の働きが変化していると考えられています。さらに、近年、がんや炎症部位において細胞は酸性環境にあることが報告されており、酸性環境下での脂質ラフトの分布や、その動きを詳しく調べ、正常な細胞とは異なる特徴を見つけることができれば、これまで治療が難しかった病気のための新しい薬や副作用の少ない薬を作る手がかりになると考えられます。また、将来的には、その特徴を目印にして、病気の診断を行うこともできると期待されています。
このような背景から、脂質ラフトを観察するための目印であるプローブ分子が世界中で開発されてきました。生体分子を可視化する上で、蛍光分子を生体分子に結合させ、その発光によって検出を可能とするプローブ分子が使われます。しかし、コレステロールは比較的小さな生体分子であり、大きな蛍光分子を結合させると、生体分子としての性質が大きく変わってしまいます。そこで、わずか2つの炭素骨格からなり化学的に安定なアルキン(炭素-炭素3重結合)を生体分子に修飾し、その分子振動から発せられるラマン散乱光を用いて生体分子を光学的に検出するアルキンプローブ分子が注目されています。アルキンはそのサイズが小さいため、アルキン修飾が生体分子の働きを大きく変えないことが特長です。また、アルキンが発するラマン散乱光は、一般的な生体分子とは異なる特徴的な光周波数に発生するため、一般的な生体分子が発するラマン散乱光との重複がなく、高感度に検出できます。しかし、このような分子では、すべてのプローブ分子が常に検出されてしまい、特定部位の分子、あるいは特定環境の分子を区別して検出することはできませんでした。
そこで、本研究グループでは、望みのタイミングでアルキン修飾を『スイッチオン』することが可能な新しいコレステロール類似体を開発しました。このコレステロール類似体にはエポキシケトン基注5)が組み込まれており、トルエンスルホニルヒドラジド(TsNHNH2)と反応することでエッシェンモーザー・タナベ開裂反応注6)(図1)が生じ、アルキン基を有する類似体に変換(アルキン化)することができます(図2)。このアルキン由来のラマン散乱光を目印にすることで、生体内でアルキン化されたコレステロール類似体だけを検出できます。また、このアルキン化反応は、弱酸性条件(pH6程度)で反応速度が格段に上がることもわかりました。この性質を利用してTsNHNH2を短時間だけ作用させることにより、弱酸性条件においてのみアルキン化をスイッチオンさせることが可能となりました。今回開発したプローブを細胞の細胞膜に導入し、弱酸性条件と中性条件でそれぞれTsNHNH2と作用させ、誘導ラマン散乱顕微鏡という高感度なラマン顕微鏡で観察を行った結果、弱酸性条件でスイッチオンさせた細胞のみから選択的にラマン散乱光が観察され(図3)、時間とともに細胞内での分布が変化する様子が確認できました。
このようなスイッチオン型のプローブは、特定の場所や条件における脂質ラフトの動きを選択的に追跡でき、腫瘍や炎症部位においてがん細胞や免疫細胞がどのように脂質ラフトを介してシグナル伝達や小胞輸送を制御しているかなど、病態の分子メカニズムを理解するための助けになると期待されます。
<参考図>
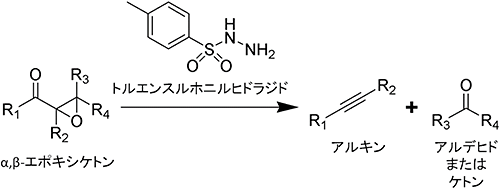
図1 エッシェンモーザー・タナベ開裂反応
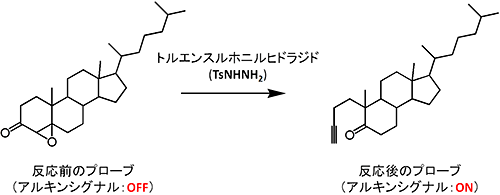
図2 コレステロールアナログプローブのアルキン化反応
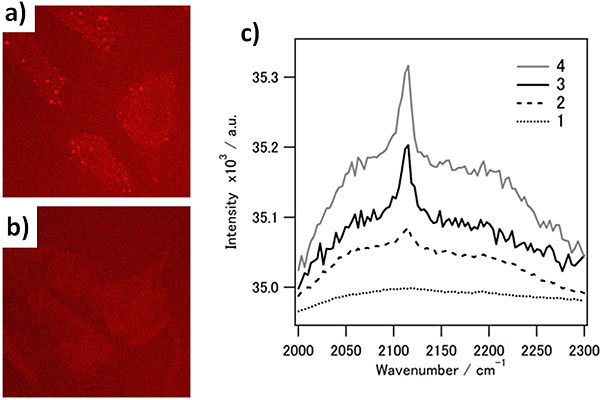
図3 細胞上での誘導ラマン顕微鏡像
(a)弱酸性条件下で反応した細胞、(b)中性条件下で反応した細胞、(c)弱酸性条件下で反応した細胞中の輝点のラマンスペクトル、2115cm-1にアルキンのピークを確認(点線1: 細胞外領域のスペクトル、破線2:細胞内の粒子状の輝点以外の領域のスペクトル、実線3・4: 細胞内の粒子状の輝点のスペクトル)。
<用語解説>
- 注1) 脂質ラフト
- 生体膜の微小な部分構造の一種で、コレステロールとコレステロールに親和性の高い脂質(スフィンゴ脂質)に富む。この部分構造は、膜タンパク質を集積し、細胞膜を介したシグナル伝達、細菌やウイルスの感染、細胞接着や細胞運動、細胞内の小胞輸送などに深く関わることが明らかとなり、幅広い研究分野で注目されている。
- 注2) プローブ
- 本来は探針の意味であるが、バイオイメージングの分野では、観察したい対象を標識するための分子、物質を指す。
- 注3) ラマン散乱光
- ラマン散乱光物質に光を入射した時、散乱された光のうち、入射された光の波長と異なる波長の光のこと。このラマン散乱は入射光と物質との間にエネルギーの授受によって起こり、散乱光と入射光とのエネルギー差は物質を構成する分子構造に由来するエネルギーに対応している。そこで、ラマン散乱光の波数に対するスペクトルを測定し、固有の振動エネルギーを持つ分子構造の存在を同定することに用いられる。近年では、ラマン散乱光の強度やスペクトルを指標にして、特定の物質や分子の局在を二次元平面上で拡大して画像化するラマン顕微鏡が開発され、染色をせずに非侵襲的に生体試料を観察する手段として盛んに研究されている。
- 注4) コレステロール類似体(アナログ)
- 化学や薬学において、アナログとは、化学的な構造や分子生物学的な性質は類似しているが、構成している原子や官能基は違う分子のこと。コレステロールアナログとは、コレステロールと構造や性質は似ている別の分子であることを意味する。
- 注5) エポキシケトン基
- エポキシドとカルボニルを有する化学構造であり、この構造を介した位置選択的な化学反応は利用価値が高く、この構造を含む化合物(エポキシケトン類)は香料配合剤、医農薬中間体として広く用いられている。
- 注6) エッシェンモーザー・タナベ開裂反応
- α,β-エポキシケトンにトルエンスルホニルヒドラジド(TsNHNH2)を作用させ、アルキンとアルデヒドまたはケトンとに分解させる有機化学反応である。この反応はアルバート・エッシェンモーザーらと、マサト・タナベらの研究グループから同時期にそれぞれ別々に報告された。
<論文情報>
| タイトル |
“Chemically-activatable alkyne-tagged probe for imaging microdomains in lipid bilayer membranes” |
| 著者名 |
Satoshi Yamaguchi、Taku Matsushita、Shin Izuta、Sumika Katada、
Manami Ura、Taro Ikeda、Gosuke Hayashi、Yuta Suzuki、Koya Kobayashi、Kyoya Tokunaga、Yasuyuki Ozeki and Akimitsu Okamoto* (*責任著者)
|
| 掲載誌 |
Scientific Reports |
| doi |
10.1038/srep41007 |
<お問い合わせ先>
<研究に関すること>
岡本 晃充(オカモト アキミツ)
東京大学 先端科学技術研究センター 生命反応化学分野 教授
Tel:03-5452-5200
E-mail:
<ImPACTの事業に関すること>
内閣府 革新的研究開発推進プログラム担当室
〒100-8914 東京都千代田区永田町1-6-1
Tel:03-6257-1339
<ImPACTプログラム内容およびPMに関すること>
科学技術振興機構 革新的研究開発推進室
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-6380-9012 Fax:03-6380-8263
E-mail:
<報道担当>
東京大学 先端科学技術研究センター 広報・情報室
〒153-8904 東京都目黒区駒場4-6-1
Tel:03-5452-5424
E-mail:
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: