ポイント
- 細胞の核と小胞体がオートファジーで分解されることを発見
- それぞれの分解の目印となるタンパク質を特定し、メカニズムを解明
- 小胞体分解の目印タンパク質は感覚神経障害の原因遺伝子と関連
東京工業大学 大学院生命理工学研究科の中戸川 仁 准教授と持田 啓佑 大学院生らの研究グループは、モデル生物「出芽酵母注1)」を用いて、細胞内の大規模分解システム「オートファジー(自食作用)」が核や小胞体をも分解の対象とすることを発見した。さらに核と小胞体に結合して「目印」となる2つのタンパク質を特定し、それらを分解するメカニズムを解明した。
細胞内の核の分解は栄養飢餓時の細胞の生存に重要であり、小胞体の分解の目印タンパク質は、ヒトの遺伝性感覚自律神経性ニューロパチーII型注2)の原因遺伝子から作られるタンパク質に相当することが示唆された。
研究成果は、英国科学誌「ネイチャー」のオンライン版で6月3日(米国東部標準時)に公開される。
<研究の背景>
私たちの体を形作る細胞の中では、様々なものが作られ、機能しているが、生命活動の維持には、それらを適宜分解することも重要である。オートファジーは、このような役割を担う、細胞内の大規模な分解システムである。タンパク質や核酸などの生体高分子から細胞小器官注3)まで、大小問わず様々な細胞内成分をオートファゴソームと呼ばれる脂質膜の袋で包み込み、種々の分解酵素を含むリソソームや液胞といった分解専門の細胞小器官に運び入れて分解する(図1)。
近年、パーキンソン病などの神経変性疾患の原因ともなり得る機能不全となったミトコンドリアなど、いくつかの細胞小器官がオートファジーで選択的に(狙いを定めて)分解されることが明らかとなり、そのメカニズムの解明や制御方法の開発を巡って世界中で激しい研究競争が繰り広げられている。しかし、細胞小器官の恒常性維持や機能制御にオートファジーがどの程度広く関与しているのかについては不明であった。
<研究成果>
オートファジーで選択的に分解されるためには、分解の対象上に「目印タンパク質」が提示されることが必要となる(図1)。目印タンパク質はそれぞれ決まった分解対象を正確に認識して結合する。既知の目印タンパク質はすべて、オートファゴソーム膜上の「Atg8」というタンパク質にも結合することが明らかとなっていた。この結合により分解対象がオートファゴソームに効率良く包み込まれる(図1)。
持田大学院生と中戸川准教授らは、Atg8と結合するタンパク質を網羅的に決定すれば、その中に未知の目印タンパク質が含まれているに違いないと考えて研究を進め、これまでまったく解析されていなかった2つのタンパク質を見いだし、「Atg39」、「Atg40」と名付けた。解析の結果、Atg39は核の分解の目印であり、Atg40は小胞体の分解の目印となることを明らかにした。
核は遺伝情報の格納・発現・伝承を担い、小胞体は多くのタンパク質や脂質の合成の場である、共に極めて重要な細胞小器官である。Atg39は核に集まり(局在し)、核の一部をちぎりとったようなものをオートファゴソームに包み込ませる(図2)。Atg40は小胞体に集まり、その一部を折り畳まれたチューブあるいはシートのような状態でオートファゴソームに取り込ませる。
これら目印タンパク質はどちらも細胞が栄養飢餓状態に陥ると発現し、それぞれの細胞小器官の分解を誘導する。Atg39を持たない酵母細胞は栄養飢餓時に核の形態に異常を来たし、通常の細胞よりも早期に死に至ることが明らかとなった。飢餓時に必須の分子を核の一部を分解することで供給している可能性がある。あるいは、異常となった核成分を分解除去することが細胞の生存に重要である可能性も考えられる。
一方、本成果と同時に「ネイチャー」に報告される論文では、ゲーテ大学(ドイツ)のグループが、ヒトの遺伝性感覚自律神経性ニューロパチーII型の原因遺伝子であるFAM134Bの遺伝子産物(タンパク質)が、哺乳類でのオートファジーによる小胞体分解のための目印タンパク質であることを明らかにした。
構造上の特徴の類似性などから、本研究で発見した酵母のAtg40は、このFAM134Bに相当すると考えられ、小胞体のオートファジーによる分解が、生物の進化の上でも極めて重要であったと推察される。
<今後の展開>
本成果は、高等動植物を含む他の生物種における研究の発展の引き金となり、オートファジーによる核および小胞体の分解の生理的意義、疾患との関連、分子メカニズムの解明のための足掛かりになると期待される。Atg40を介した小胞体の分解は、その破綻が特定の遺伝性神経障害と関連があることが示唆されたが、Atg39が誘導する核の分解については、Atg39に相当するタンパク質の哺乳類での存在を含め、未だ多くの謎が残されており、さらなる研究の発展が期待される。
<参考図>
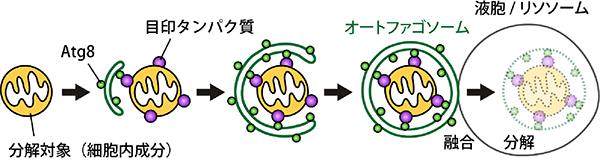
図1 オートファジーのプロセス
オートファジーで選択的に分解すべき対象が細胞内に生じると、それらには特定のタンパク質で目印が付けられる。目印タンパク質は、オートファゴソームを作る装置を分解対象上に呼び寄せ、オートファゴソームの形成を開始させる。目印タンパク質はさらに、オートファゴソーム膜上のAtg8というタンパク質と結合することで、分解対象を効率良くオートファゴソームに包み込ませる。完成したオートファゴソームは、液胞(酵母や植物などの場合)やリソソーム(哺乳類などの場合)と融合し、対象物の分解が達成される。
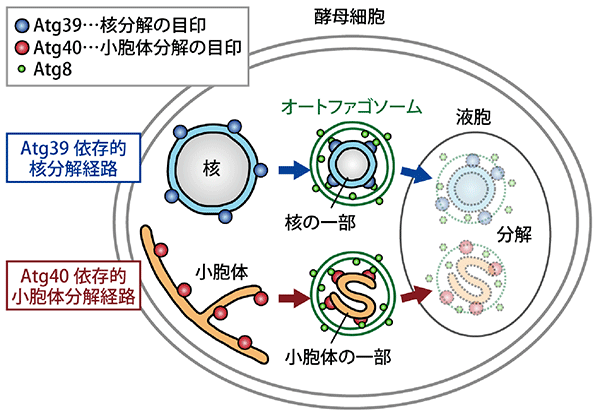
図2 本研究で明らかになった核と小胞体のオートファジーによる分解経路
酵母が栄養飢餓に晒されると、Atg39、Atg40という目印タンパク質が作られる。Atg39は核へ、Atg40は小胞体に局在し、これら細胞小器官のオートファゴソームによる取り込みを誘導する。
<用語解説>
- 注1) 出芽酵母
- 単細胞の真核生物。パンやワインなどの発酵食品の製造にも利用される有用微生物であるが、基本的な生命現象についてはヒトを含めた高等動植物と共通の原理が成立するため、生命科学の研究においても優れたモデル生物として酵母を用いた研究が先導的な役割を果たしている。
- 注2) 遺伝性感覚自律神経性ニューロパチーII型
- 主に末梢の感覚神経および自律神経が傷害される進行性の疾患。痛覚の喪失を特徴の1つとする。最近になっていくつかの原因遺伝子が特定されたが、発症機構など不明な点が多く残されており、根本的な治療法は確立されていない。
- 注3) 細胞小器官
- 細胞は脂質膜(細胞膜)で外環境と自己とを隔てているが、その内部にも膜で仕切っていくつかの空間、すなわち細胞小器官を作りだし、それぞれに独自の役割を担わせている。
<論文情報>
| 掲載誌 |
Nature |
| 論文タイトル |
“Receptor-mediated selective autophagy degrades the endoplasmic reticulum and the nucleus” |
| 著者 |
Keisuke Mochida, Yu Oikawa, Yayoi Kimura, Hiromi Kirisako, Hisashi Hirano,Yoshinori Ohsumi & Hitoshi Nakatogawa |
| doi |
10.1038/nature14506 |
<研究グループ>
東京工業大学、横浜市立大学
<研究サポート>
本成果は、主に、科学技術振興機構 CREST「ライフサイエンスの革新を目指した構造生命科学と先端的基盤技術」および、文部科学省科学研究費補助金 新学術領域研究(研究領域提案型)「オートファジーの集学的研究:分子基盤から疾患まで」のサポートを受けて得られた。
<お問い合わせ先>
<研究に関すること>
東京工業大学 大学院生命理工学研究科 生体システム専攻 准教授
中戸川 仁
Tel:045-924-5879 Fax:045-924-5113
E-mail:
<JST事業に関すること>
科学技術振興機構 戦略研究推進部 ライフイノベーショングループ
川口 哲
Tel:03-3512-3524 Fax:03-3222-2064
E-mail:
<報道担当>
東京工業大学 広報センター
Tel:03-5734-2975 Fax:03-5734-3661
E-mail:
科学技術振興機構 広報課
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: