ポイント
- 「記憶や学習の場」と考えられているシナプスの形成・維持・除去の仕組みは十分に解明されていなかった。
- C1ql1というたんぱく質が記憶・学習機能に重要な神経回路の強化・維持に必須であることが分かった。
- 記憶障害や精神疾患の原因解明と治療法開発に役立つことが期待できる。
JST 戦略的創造研究推進事業において、慶應義塾大学 医学部 生理学教室の柚﨑 通介 教授と掛川 渉 専任講師らは、神経回路が選択的に形成・維持されるのに必須なたんぱく質を発見しました。
私たちの脳の中では、無数の神経細胞が「シナプス注1)」を介して互いに結合し、記憶・学習注2)に必要な神経回路を形成しています。近年、発達障害や精神疾患の原因の1つとしてシナプスを基盤とした神経回路の障害が疑われています。しかしシナプスがどのようにして形成、維持、あるいは除去されるのかについては、未解明な点が数多く残されています。
本研究グループは、マウスを用いた実験により、神経細胞が分泌するC1ql1(シーワンキューエル1)注3)と呼ばれるたんぱく質が、生後発達時の小脳において正しいシナプスを選択的に強化することを発見しました。また、成熟後にC1ql1を除去すると、いったん形成されたシナプスが失われ、小脳神経回路による運動学習が著しく障害されることが分かりました。
C1ql1に類似したたんぱく質は小脳以外のさまざまな脳部位にも存在し、それぞれの神経回路において機能すると考えられます。このため、本研究の成果は、記憶障害や精神疾患の原因解明と治療法開発に役立つことが期待されます。
本研究は、JSTの課題達成型基礎研究の一環として、新潟大学の崎村 健司 教授、北海道大学の渡辺 雅彦 教授、英国オックスフォード大学のラドゥ アリセスク 博士と共同で行ったものです。
本研究成果は、2015年1月21日(米国東部時間)に米国科学誌「Neuron」のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域 |
「脳神経回路の形成・動作原理の解明と制御技術の創出」
(研究総括:小澤 瀞司 高崎健康福祉大学 健康福祉学部 教授) |
| 研究課題名 |
「成熟脳におけるシナプス形成機構の解明と制御」 |
| 研究代表者 |
柚﨑 通介(慶應義塾大学 医学部 生理学教室 教授) |
| 研究期間 |
平成21年10月~平成27年3月 |
JSTはこの領域で、脳神経回路の発生・発達・再生の分子・細胞メカニズムを解明し、さらに個々の脳領域で多様な構成要素により組み立てられた神経回路がどのように動作してそれぞれに特有な機能を発現するのか、それらの局所神経回路の活動の統合により、脳が極めて全体性の高いシステムをどのようにして実現するのかを追求します。またこれらの研究を基盤として、脳神経回路の形成過程と動作を制御する技術の創出を目指します。
上記研究課題では、C1qファミリー分子によるシナプス形成・維持機構を解明し、C1qファミリー分子を介したシグナル伝達経路を操作することによって、神経回路の形成と個体行動を制御する方法を探ります。
<研究の背景と経緯>
私たちの脳内には、1,000億を超える数の神経細胞が存在し、神経細胞同士が互いに「シナプス」と呼ばれる結び目を形成することによって神経回路ネットワークを構築します(図1)。生後間もない時期に、神経細胞同士はいったん過剰にシナプスを形成して未熟な神経回路を形成し、成長とともに必要な神経回路が強化される一方で、不必要なシナプスはしだいに除去されていきます。この過程を「シナプス刈り込み」と呼びます。これまでの研究により、シナプス刈り込みは脳内のあらゆる部位で起こる普遍的な事象であることが分かってきました。シナプス刈り込みによって完成された神経回路は、その後長期にわたって維持され、記憶や学習といった高次神経機能を担うと考えられています。
スポーツや楽器演奏などの繰り返しの練習によって身に付く「運動記憶・学習」は、私たちの後頭部に位置する小脳によって担われます。小脳の下部に位置する延髄にある「下オリーブ核」の神経細胞が伸ばす突起(登上線維)は、小脳のプルキンエ細胞とシナプス(登上線維シナプス注4))を形成します(図2)。登上線維は、小脳において運動学習を引き起こすための教師信号注5)として働くことが知られています。生後間もない時期のプルキンエ細胞は複数本の登上線維とシナプスを形成していますが、発達にともなって、登上線維の間に強弱が生じます。最終的に弱い登上線維とそのシナプスは刈り込まれ、1本の強い登上線維が形成するシナプスが勝ち残ります(図3)。このような登上線維シナプスの刈り込み過程が障害された遺伝子改変マウスでは、運動記憶・学習が著しく低下することが分かっています。しかし、登上線維の刈り込みがどのようにして起きるのかについては未解明な点が数多く残されていました。
<研究の内容>
本研究グループは、小脳における登上線維シナプス刈り込み現象をモデルとして、正しい神経回路が形成されるメカニズムの解明を目指しました。近年、本研究グループや他のグループによって、免疫系で働く分子である補体C1qに似たたんぱく質(C1qファミリー分子)が神経細胞においてシナプス形成や除去に関与することが分かっています。そこで登上線維のもとである下オリーブ核神経細胞が、C1qファミリーに属するC1ql1(シーワンキューエル1)を作っていることに着目し実験を行いました。
まず、C1ql1遺伝子を欠くC1ql1欠損マウスを作製し、登上線維シナプスのシナプス刈り込み過程を観察しました。野生型マウスでは1本の強い登上線維が強化されるとともに、弱い登上線維の刈り込みが進みます。一方、C1ql1欠損マウスでは、強い登上線維が強化されず、その結果として、他の弱い登上線維シナプスの刈り込みが障害されることが分かりました。また登上線維から分泌されたC1ql1は、プルキンエ細胞に存在するBAI3(バイ3)注6)と呼ばれる受容体に結合することを発見しました(図4)。
BAI3遺伝子欠損マウス(BAI3欠損マウス)や、C1ql1-BAI3間の結合を阻害したマウスにおいても、登上線維シナプスの刈り込みが障害されました。C1ql1やBAI3を欠損したマウスでは小脳神経回路に依存した運動記憶・学習機能が著しく低下することも分かりました(図5)。
さらに、成熟した野生型マウスにおいてC1ql1やBAI3を除去すると、登上線維シナプスが失われることから、C1ql1-BAI3シグナリングは登上線維シナプスを大人になってからも維持していくためにも必要なことが分かりました。
以上のことから、C1ql1-BAI3シグナリングは、小脳において発達時に特定の登上線維を選択的に強化・刈り込みするために必須であるのみならず、成熟後においても神経回路を維持し、運動学習を制御するために重要な役割を果たすことが明らかになりました。
<今後の展開>
C1ql1の関連分子であるC1ql2-4は小脳以外のさまざまな脳部位にも存在します。また他のC1qファミリーたんぱく質もさまざまな神経回路に存在していることが分かっています。従って、本研究グループによる小脳におけるC1ql1シグナリングメカニズムの解明は、他の神経回路におけるC1qファミリーたんぱく質を介したシナプス刈り込みや記憶・学習機構の理解につながることが期待されます。
また、近年、発達障害や精神疾患の原因の1つとして、シナプスを基盤とした神経回路障害が疑われています。興味深いことに、C1ql1と結合するBAI3は、統合失調症や双極性障害の関連遺伝子として報告されています。C1ql1-BAI3シグナリングによる新しい神経回路形成・維持機構を追究した本研究の成果が、今後、種々の精神疾患の病態解明や治療法開発に新たな可能性をもたらすものと期待されます。
<参考図>
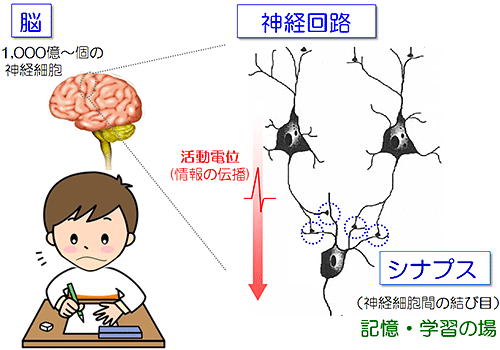
図1 神経細胞はシナプスによって結合し、神経回路を形成
私たちの脳には、1,000億を超える数の神経細胞が存在し、神経細胞同士がシナプスを介して互いに結合することにより、記憶や学習の形成に必要な神経回路を構築する。そのため、シナプスこそが私たちの脳における「記憶・学習」の場と考えられている。
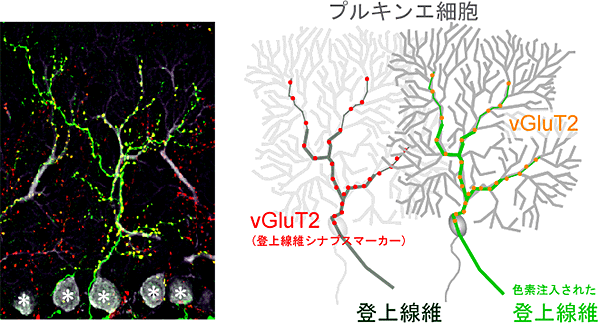
図2 小脳プルキンエ細胞に結合する登上線維と登上線維シナプス
- (左図)成熟マウスの延髄下オリーブ核に蛍光色素を注入し、登上線維を標識化した小脳切片。カルビンジン(プルキンエ細胞のマーカー;灰色)と小胞性グルタミン酸トランスポーター2(vGluT2;登上線維シナプスマーカー;赤色)の特異的抗体を用いて、切片を免疫染色した。色素注入により標識化された登上線維(緑色)上のvGluT2(赤色)は黄色に見える。枝分かれが特徴的な神経細胞であるプルキンエ細胞と登上線維が登上線維シナプスを形成していることが知られていた。根元にある球状のもの(*部分)はプルキンエ細胞の細胞体を表している。
- (右図)登上線維シナプスの模式図。
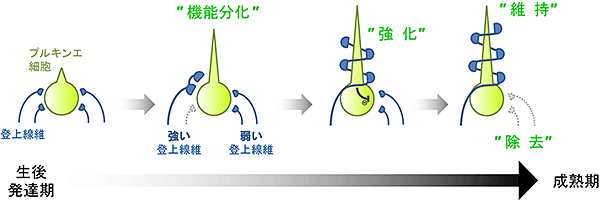
図3 登上線維シナプス回路の生後発達変化
生後間もないプルキンエ細胞は複数本の弱い登上線維によって結合されているが、その後、登上線維間で入力の強弱が生じ(機能分化)、強い線維のみがプルキンエ細胞の細胞体から樹状突起(上方)に移動し、強化されていく(強化)。一方、弱い登上線維はしだいに刈り込まれ(除去)、最終的に、成熟期のプルキンエ細胞には1本の強力な登上線維のみが支配するようになる(維持)。
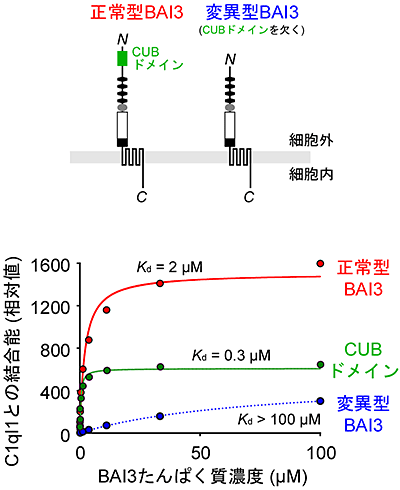
図4 C1ql1はプルキンエ細胞の膜表面に発現するBAI3と結合する
BAI3は、細胞接着型Gたんぱく質共役受容体であり、細胞外領域にCUBドメイン(緑ラベル)と呼ばれる機能部位を持つ。今回、正常型BAI3(赤ラベル)とCUBドメインを欠く変異型BAI3(青ラベル)の細胞外領域を用いて、C1ql1との結合強度を表面プロズモン共鳴法により計測した。その結果、変異型BAI3は正常型に比べ、C1ql1への結合能が著しく低下した(Kd(解離定数)の値が大きいほど結合能が低い)。一方、CUBドメインとC1ql1との結合能を計測すると、極めて強固な結合を示すKd値が得られた。従って、C1ql1はBAI3の細胞外領域に位置するCUBドメインに選択的に結合することが分かった。
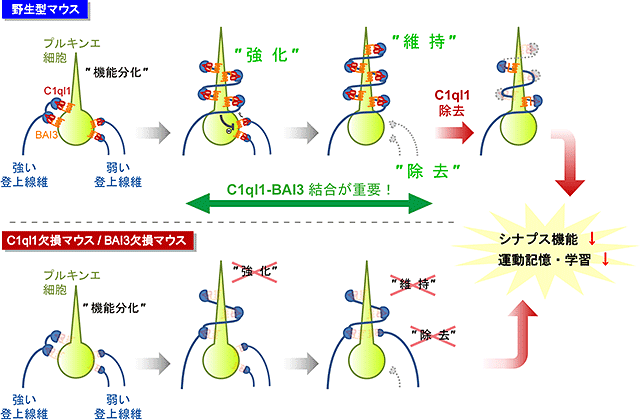
図5 C1ql1-BAI3結合は登上線維シナプス回路を調節し、運動記憶・学習を制御する
野生型マウス(上段)とC1ql1あるいはBAI3欠損マウス(下段)における登上線維シナプス回路の生後発達変化。欠損マウスの場合、プルキンエ細胞に結合する複数本の登上線維間で正常に機能分化するものの、その後、強い線維はそれ以上、強化されない。そのため、他の弱い登上線維の刈り込みが損なわれ、結果として、シナプス機能および運動記憶・学習に障害を生じてしまう。また、成熟期の野生型マウスにおいて、C1ql1を急性除去すると、いったん形成された登上線維シナプスが外れ、欠損マウスと同様に、シナプス機能が障害された。従って、C1ql1-BAI3結合は、正しい神経回路の強化に働くばかりでなく、維持にも重要であることが分かった。
<用語解説>
- 注1) シナプス
- 神経細胞と神経細胞のつなぎ目。シナプスの前側にある神経細胞からグルタミン酸などの神経伝達物質が放出され、後ろ側の神経細胞がこれを受け取ることによって情報が伝達される。記憶・学習の形成過程において、シナプスの数が変化したり、あるいはシナプス伝達効率が変化したりすることから、シナプスは「記憶・学習の場」であると考えられている。
- 注2) 記憶・学習
- 記憶は言語で表せるような記憶(陳述記憶)と言語では表せない記憶(手続き記憶)に大きく分類される。運動に関する記憶は後者に含まれる。例えば、初めはピアノを弾けなくても練習をするにつれて上手になっていくことや、しばらく弾かなくて腕が落ちても、また少し練習するとすぐにもとのように弾けるようになることが運動記憶・学習に相当する。運動記憶には脳のさまざまな部位が動員されるが、特に小脳は、この獲得と保持に大きな役割を果たしている。
- 注3) C1ql1(シーワンキューエル1)
-
免疫系補体C1qの機能部位である球状C1qドメインを持つたんぱく質群はC1qファミリーと呼ばれている。C1qファミリーの中には、補体C1qに加え、脂質代謝にかかわるアディポネクチンや冬眠時に脳内で濃度上昇する冬眠特異的たんぱく質などが含まれる。また、本研究グループが以前に報告した中枢シナプス形成を促すCbln1もこのファミリーに属す。
- C1ql1はC1qファミリーたんぱく質の1つであり、C1ql1-4の同族分子が存在する。C1ql1は、C末端の球状C1qドメインやN末端のコラーゲン様ドメインおよびジスルフィド結合を介して多量体を形成し、細胞から分泌される。脳内では、登上線維の起始核である延髄下オリーブ核にほぼ選択的に発現する。
- 注4) 登上線維シナプス
- 延髄下オリーブ核より投射する登上線維が小脳のプルキンエ細胞と結合することで形成される興奮性シナプス。運動記憶・学習の獲得の際、教師信号としてプルキンエ細胞に情報を伝えると考えられており、このシナプスの形成あるいは機能の異常が運動記憶・学習障害をもたらす。
- 注5) 教師信号
- 記憶や学習を担う神経回路の機能や構造を最適化させるのに必要な外部信号。小脳が担う運動記憶・学習の場合、登上線維シナプスは、運動のエラーシグナルを教師信号としてプルキンエ細胞に伝えている。
- 注6) BAI3(バイ3)
- 脳特異的血管新生抑制因子3(Brain-specific Angiogenesis Inhibitor 3)。細胞接着型Gたんぱく質共役受容体の一種であり、同族分子としてBAI1-3が存在する。BAI3は、統合失調症や双極性障害の関連遺伝子として、近年注目されている。
<論文タイトル>
“Anterograde C1ql1 Signaling Is Required in Order to Determine and Maintain a Single-Winner Climbing Fiber in the Mouse Cerebellum”
(順行性C1ql1シグナリングはマウス小脳において単独勝者となる登上線維の決定および維持に必要である)
doi: 10.1016/j.neuron.2014.12.020
<お問い合わせ先>
<研究に関すること>
柚﨑 通介(ユザキ ミチスケ)
慶應義塾大学 医学部 生理学教室 教授
〒160-8582 東京都新宿区信濃町35
Tel:03-5363-3749 Fax:03-3359-0437
E-mail:
<JST事業に関すること>
川口 貴史(カワグチ タカフミ)
科学技術振興機構 戦略研究推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail:
<報道担当>
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail:
慶應義塾大学 信濃町キャンパス 総務課
〒160-8582 東京都新宿区信濃町35
Tel:03-5363-3611 Fax:03-5363-3612
E-mail: