ポイント
- 手綱核の神経活動がこれからの体験がどのくらい危険であるかの予測値を表現
- 「手綱核-縫線核神経回路」は危険を回避する適切な対応行動の学習に必須
- パニック障害などの疾患の治療法につながる可能性
理化学研究所(理研、野依 良治 理事長)は、遺伝子改変魚注1)を用いて、動物が危険を察知したときに、パニック反応を抑えて、冷静かつ適切に危険回避策をとれるようになるために不可欠な脳神経回路を発見しました。これは、理研 脳科学総合研究センター(利根川 進 センター長)発生遺伝子制御研究チームの岡本 仁 チームリーダー(脳科学総合研究センター 副センター長)、天羽 龍之介 基礎科学特別研究員らの研究チームの成果です。
経験の浅いネズミは、天敵であるネコが現れる予感がする場面(猫の首輪の鈴の音が聞こえるなど)に遭遇すると、浅いながらの経験から危険を察知してパニック行動の一種であるすくみ行動を起こしてしまいますが、そのままでは捕まってしまうこともあります。一方、経験を積んだネズミは、パニック反応を起こさないで、最も安全なルートを探して逃げ出すことができます。このような行動の変化は、これから体験することがどのくらい危険かという予測値「危険予測値注2)」に反して、それほど危険でないような結果に終わり、「ほっと安心する」ことによって、危険を回避する特定の行動様式が強化され、適切な危険回避行動が修得された結果といえます。ところが、このような危険予測値が脳のどこでどのように表現され、情報として学習に利用されているのかは明らかではありませんでした。
研究チームは、小型淡水魚ゼブラフィッシュ注3)の脳で、腹側手綱核(ふくそくたづなかく)注4)という領域の神経細胞が、危険予測値に対応して活動することを見いだしました。実際に腹側手綱核からの情報を遮断すると、危険を回避する学習である「能動的回避学習注5)」ができなくなりました。一方、ゼブラフィッシュの腹側手綱核を、「光遺伝学注6)」という手法を用いて人為的に活性化させると、危険を予測しているかのような回避行動が誘導され、危険予測値を植え付けることに成功しました。また、魚類からほ乳類まで進化的に保存されている手綱核は、気分などに関わる脳内神経伝達物質のセロトニン注7)を分泌する脳幹にある縫線核(ほうせんかく)という領域の活動を調節しており、本結果から、危険予測値の情報がセロトニンによって伝わることも明らかとなりました。
危険予測値を利用した適切な対応行動が学習できないと、本能的なパニック反応から抜け出せず、パニック障害などの疾患を引き起こすと考えられます。手綱核を介した危険予測値の情報がどのように伝わり学習に使われるのか、その仕組みを解明することは、このような疾患の治療法の改善につながると期待できます。
本研究成果は、米国の科学雑誌『Neuron 』(12月3日号)に掲載されるに先立ち、オンライン版(11月20日付け:日本時間11月21日)に掲載されます。
<背景>
動物は恐怖を感じる事象に遭遇すると、本能的にパニック反応を起こしてすくんでしまうことがあります。この反応は、危険回避の救急処置としては有効ですが、いつも最適とは限りません。実際に自分の安全を確保するためには、このパニック反応を抑え、与えられた状況ごとに冷静に適切な対処法を探して、それを学習する必要があります。たとえば経験の浅いネズミは、天敵であるネコが現れる予感がする場面(猫の首輪の鈴の音が聞こえるなど)に遭遇すると、浅いながらの経験から危険を察知してパニック行動の一種であるすくみ行動を起こしてしまいますが、そのままでは捕まってしまうこともあります。一方、経験を積んだネズミは、パニック反応を起こさないで、最も安全なルートを探して逃げ出すことができます。
この例は、「これから体験することがどのくらい危険とされるか」という「危険予測値」に反して、たまたまうまく逃げて「実際の体験がそれほど危険でなかった」場合に起こる学習の結果といえます。こうした場合には、危険が回避できて「ほっと安心する」ことによって、危険を回避できた特定の行動様式が強化され、最も適切な危険回避行動が修得されていきます。このように、経験によって危険予測値自体も減少していき、パニック反応から抜け出して、冷静で適切な対処法を取ることができるようになります。このような、積極的かつ適切な行動を起こすことによって危険を回避する行動を、能動的回避行動といいます。
「ほっと安心する」ときには、脳内のドーパミン神経細胞注8)の活動が上昇します。これまでの研究から、ドーパミン神経細胞は、行動する前に動物が持っている危険予測値と、現実の結果の差(予測誤差)に応じて反応することが明らかになっています。実際に、行動の結果、動物がたとえ偶然でもうまく危険を回避できた場合、予測誤差はポジティブとなり、これに応じてドーパミンが分泌されます。これが、安心に導く行動の強化学習注9)に使われていることが分かってきています。
ところが、このような強化学習で、予測誤差が正しく計算されるためには、危険予測値が脳のどこかで表現されていなければならないはずですが、それが脳のどこで、どのように表現されているのかは、明らかではありませんでした。
研究チームは、進化的に非常によく保存されている脳の手綱核という領域に着目し、小型淡水魚であるゼブラフィッシュを用いて、危険予測値が脳内でどのように表現されているのかを調べました。
<研究手法と成果>
手綱核は、脳内の重要な神経伝達物質であるドーパミンとセロトニンの分泌を制御しています。手綱核を介した神経ネットワークは、魚類からヒトを含む霊長類まで、進化的に非常によく保存されています。今回、研究チームは、気分などに関わるといわれるセロトニンの分泌を促進する、ゼブラフィッシュの腹側手綱核の働きに注目しました。
まず、魚が危険を予測しているときの腹側手綱核の神経細胞の活動を調べたところ、これらの神経細胞は危険予測値に対応して活動することが分かりました。
この学習は、行き来が可能な2つの部屋に分かれた水槽で行いました。魚がいる部屋で危険を予告する赤ランプを点灯し、それに続いて一定時間後に軽い電気ショックを与えます。赤ランプが点灯中に反対側の部屋に逃げ込めば、電気ショックは回避できます。魚は初め、ルールが分からずに軽い電気ショックを受け、やがて赤ランプの提示に対してパニック反応を示すようになりますが、そのうちに、赤ランプがついている間に偶然反対側の部屋に移れば電気ショックを受けない、ということを知り、次第に能動的回避行動を学習していきます(図1)。
つまり、与えられた状況(赤ランプの点灯)で将来に起こりうる危険(電気ショック)を回避するための学習では、はじめに電気ショックを受け続けている段階で、まずその状況(赤ランプの点灯)が危険であることを学習します。このような状況では、赤ランプの点灯に対して、魚は次第に大きな危険予測値を抱くようになると予想されます。
その後、学習の過程で危険回避の方法を修得するにつれて、同じ危険の到来を知らせるサイン(赤ランプの点灯)に対しても、実際にそれを回避できると確信するようになります。このような状況では、魚が抱く、将来起こりうる危険の予測値は、次第に減少していくと予想されます。
実際に、学習の初期の段階で学習を中断し、魚の動きを止める薬剤で処理した後、顕微鏡下で、赤ランプの点灯に対する腹側手綱核の神経細胞の活動を計測したところ(図2A、B)、学習前の魚の計測値と比べて、活動の有意な上昇が見られました。一方、学習を完了した魚の腹側手綱核の反応を調べると、学習前の魚と反応レベルが変わりませんでした(図2C)。
つまり、腹側手綱核の神経細胞は、危険を予感させるサインの提示に対して、学習の初期過程では活動頻度を上昇させるように反応し、学習が進むにつれて、活動頻度の上昇が小さくなり、やがて学習が完成すると、活動頻度が平常レベルに戻ることが示されました。このような結果は、先に述べたような予想と大変良く一致することが分かりました。
この結果は、腹側手綱核の神経細胞が、この神経細胞が活動を促進する縫線核のセロトニン神経細胞群へ、脳内で危険予測値の情報を正確に伝えていることを示唆しています。
さらに、この情報が単に危険予測値の変化と並行して変動するだけでなく、危険回避行動の学習にも欠くことができない働きをしていることが明らかになりました。実際に、腹側手綱核から縫線核のセロトニン神経細胞群への経路を、遺伝子操作技術を使って遮断すると、危険が到来する前に逃避するという、能動的回避行動を学習できなくなりました(図3)。このような、腹側手綱核が働かないゼブラフィッシュは、能動的回避行動を学習できなくても、赤ランプが点灯するとパニック反応を示すという学習の初期段階の反応を示すことができ、むしろこの反応を示し続けました(図3)。この結果は、腹側手綱核が働かないと、パニック反応から抜け出せなくなることを示しています。
また逆に、光感受性のタンパク質を神経細胞に発現させ、光を当てることで神経活動を亢進・抑制する「光遺伝学」という手法を用いて、腹側手綱核を人為的に活性化させたところ、大きな危険予測値を植え付けることができました。この実験では、水槽の半分は底が赤に、もう半分は緑に光るようにします(図4)。ゼブラフィッシュが赤のエリアにいる時だけ、腹側手綱核を光刺激によって活性化させると、赤のエリアを避けるようになりました。逆に緑のエリアだけで腹側手綱核を活性化させた場合は、緑のエリアを避けるようになりました。これらの結果は、脳の腹側手綱核から縫線核のセロトニン神経細胞群へと危険予測値の情報が伝わることで、ゼブラフィッシュが回避行動を学習することを示唆しています。
これらの結果から、腹側手綱核-縫線核神経回路が危険予測値を正しく伝えることで、動物はパニック反応から抜け出して、適切な回避行動を学習することができる、という仕組みが明らかになりました。
<今後の期待>
手綱核-縫線核神経回路は、ゼブラフィッシュから人間を含むほ乳類まで保存されており、その機能も保存されていることが期待できます。パニック障害は、状況に釣り合わない過剰な不安とそれに伴う身体症状(どうき、胸苦しさ、息苦しさ、めまいなど)が発作的に起こるもので、約100人に1~2人程度で発症するといわれています注)。そのメカニズムの全貌は明らかになっていませんが、本能的なパニック反応を抑えることができなくなっていることから、この疾患では手綱核-縫線核神経回路が正常に機能していない可能性があると考えられます。パニック障害の治療法として、セロトニンの作用を高めると考えられるセロトニン再取り込み阻害剤(SSRI)が比較的有効であることが知られ、この仮説を裏付けています。今後、手綱核-縫線核神経回路から伝えられた危険予測値の情報が、行動様式の学習に使われる仕組みを研究することにより、パニック障害などの疾患に対する、より有効な治療法の開発につながると期待できます。
なお、本研究は文部科学省 脳科学研究戦略推進プログラム「神経情報基盤(課題G)の一環として実施され、文部科学省 科学技術研究費の新学術領域研究「予測と意思決定の脳内計算機構の解明による人間理解と応用」、科学技術振興機構(JST)戦略的創造研究推進事業(CREST)「脳神経回路の形成・動作原理の解明と制御技術の創出」研究領域(研究総括:小澤 瀞司 高崎健康福祉大学 健康福祉学部 教授)における研究課題「手綱核による行動・学習の選択機構の解明」(研究者:岡本 仁)の支援を得て行われました。
注) 厚生労働省ホームページ: http://www.mhlw.go.jp/kokoro/know/disease_panic.html
<参考図>
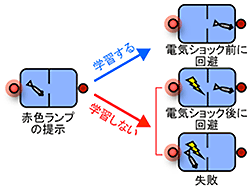
図1 危険を知らせるシグナルに対して、回避行動を学習する能動的回避行動の学習実験
赤色ランプが点灯後しばらくすると電気ショックが与えられるが、赤色ランプ点灯中に反対の部屋に移動することができれば電気ショックを回避できる。
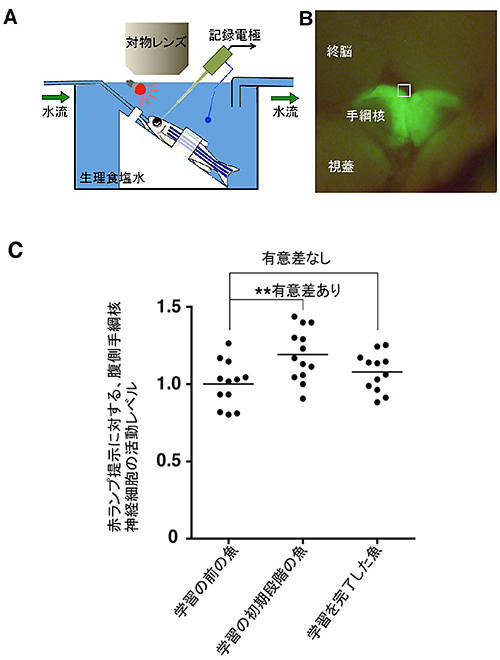
図2 能動的回避学習での危険予測値の増減に一致した腹側手綱核の神経活動の変化
- A :赤色ランプの点灯に対する、腹側手綱核の神経活動の応答を記録する実験の模式図。
- B :緑色の蛍光を発するタンパク質GFPで標識した腹側手綱核を生きたゼブラフィッシュで観察し、この蛍光シグナルを頼りに電極を挿入して、神経活動を記録する。
- C :能動的危険回避学習過程での腹側手綱核の神経活動の増減。
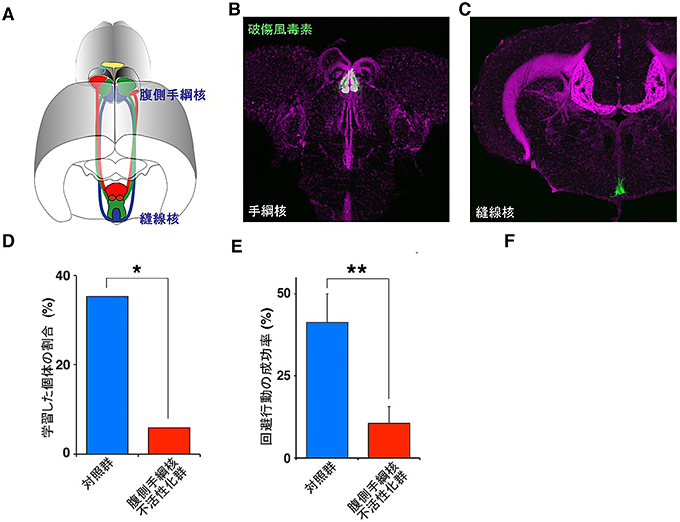
図3 腹側手綱核は危険を予測した際の回避行動の学習に必須である
| A |
:ゼブラフィッシュの脳での腹側手綱核-縫線核経路の模式図。 |
| B、C |
:腹側手綱核-縫線核経路に神経伝達を遮断する破傷風毒素(緑色)を発現するように操作した遺伝子改変ゼブラフィッシュの脳切片。赤紫色は細胞の核を示す。 |
| D、E |
:腹側手綱核-縫線核経路の神経伝達を遮断したゼブラフィッシュでは、回避行動の学習に異常が認められる。 |
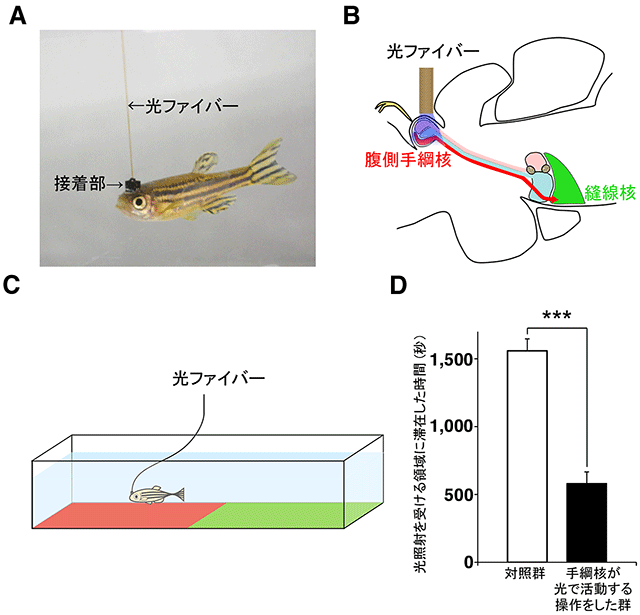
図4 人為的に腹側手綱核の神経活動を上昇させることで、危険予測値を植え付ける
| A |
:光ファイバーを接続した自由遊泳中のゼブラフィッシュ。 |
| B、C |
:光遺伝学を利用して腹側手綱核を人為的に活性化させる実験の模式図。赤または緑のどちらか一方の領域に滞在している間、光ファイバーを介した光の照射によって光感受性タンパク質を発現させた手綱核を人為的に活動させる。 |
| D |
:腹側手綱核に光感受性タンパク質を発現させた魚では、光照射による腹側手綱核の活動の上昇に伴って回避行動が観察され、光の照射を受ける領域に滞在する時間が短くなる。 |
<用語解説>
- 注1) 遺伝子改変魚
- 遺伝子組み換え技術により、人為的に外部から任意の遺伝子をゲノムDNAに導入した魚。ゼブラフィッシュでは比較的簡便に遺伝子改変を行える。また、導入する遺伝子が働く時期や領域の操作も可能。
- 注2) 危険予測値
- 現在の状況から予測される将来の危険の程度。実際に経験する危険の程度と比較することで、直前の行動を強化または弱化し、次の危険予測値を更新するのに利用される。
- 注3) ゼブラフィッシュ
- インド原産の淡水性熱帯魚。飼育が比較的容易で多産であるため実験動物として利用されている。受精卵にDNA断片や特定遺伝子を微量注入することで、遺伝子組み換えが容易に行える。魚類と人は同じ脊椎動物であり脳の基本構造が一致しているため、脳研究の新しいモデル動物として注目されている。
- 注4) 腹側手綱核(ふくそくたづなかく)
- 間脳に位置する手綱核の腹側の領域。手綱核は進化的によく保存されており、ゼブラフィッシュにおいては腹側、背側手綱核に分かれる。ゼブラフィッシュの腹側手綱核がうつ状態の制御に重要な哺乳類の外側手綱核の相同領域であることを同研究チームが突き止めている。
- 注5) 能動的回避学習
- 電気ショックなどの刺激やそれを予期させる合図に対して、能動的な回避法を試行錯誤により学習する行動課題。本研究では部屋を移動することで電気ショックを回避する。
- 注6) 光遺伝学
- 光感受性のタンパク質を神経細胞に発現させ、光を当てることで人為的に神経活動を亢進または抑制する技術。
- 注7) セロトニン
- 脳内では神経伝達物質として利用され、縫線核のセロトニン神経細胞から脳内に広く分泌される。睡眠、食欲、うつ状態、不安、闘争行動など、さまざまな行動を制御する。抗うつ薬の多くはこのセロトニンの作用を上昇させる。
- 注8) ドーパミン神経細胞
- 神経伝達物質として利用されるドーパミンを分泌する神経細胞。腹側被蓋野(ふくそくひがいや)や黒質といった領域に固まって存在する。ドーパミン神経細胞はさまざまな報酬に対して反応し、運動の制御や学習に関与する。
- 注9) 強化学習
- 報酬を獲得することや、罰(危険)から逃れることを目的として、試行錯誤を繰り返すうちに、うまくいって報酬がもらえたり、危険が回避できたりするような行動をした場合、たまたま取ったその行動を、将来選択しやすくするということを繰り返していくうちに、結果として最大の報酬や最小の罰を得るような行動プログラムを獲得できるという学習の様式。
<原論文情報>
Ryunosuke Amo, Felipe Fredes, Masae Kinoshita, Ryo Aoki, Hidenori Aizawa, Masakazu Agetsuma, Tazu Aoki, Toshiyuki Shiraki, Hisaya Kakinuma, Masaru Matsuda, Masako Yamazaki, Mikako Takahoko, Takashi Tsuboi, Shin-ichi Higashijima, Nobuhiko Miyasaka, Tetsuya Koide, Yoichi Yabuki, Yoshihiro Yoshihara Tomoki Fukai and Hitoshi Okamoto. “The habenulo-raphe serotonergic circuit encodes an aversive expectation value essential for adaptive active avoidance of danger.” Neuron, 2014,
doi: 10.1016/j.neuron.2014.10.035
<報道担当・問い合わせ先>
<問い合わせ先>
理化学研究所 脳科学総合研究センター 発生遺伝子制御研究チーム
チームリーダー 岡本 仁(おかもと ひとし)
E-mail:
理化学研究所 脳科学研究推進室
Tel:048-467-9757 Fax:048-467-4914
<文部科学省 脳科学研究戦略推進プログラム>
脳科学研究戦略推進プログラム事務局
丸山 めぐみ(まるやま めぐみ)
Tel:0564-55-7804 Fax:0564-55-7805
E-mail:
<JST事業に関すること>
科学技術振興機構 戦略研究推進部
川口 貴史(かわぐち たかふみ)
Tel:03-3512-3524 Fax:03-3222-2064
<報道担当>
理化学研究所 広報室 報道担当
Tel:048-467-9272 Fax:048-462-4715
科学技術振興機構 広報課
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: