九州大学 大学院薬学研究院 薬理学分野の井上 和秀 主幹教授と津田 誠 准教授を中心とする研究グループは、神経のダメージで発症する慢性的な痛み(神経障害性疼痛)の原因タンパク質として「IRF5注1)」を突き止めました。IRF5は、神経の損傷後に脳・脊髄の免疫細胞と呼ばれる「ミクログリア注2)」の中だけで増え、IRF5を作り出せない遺伝子操作マウスでは痛みが弱くなっていました。さらに、研究グループは、2003年にP2X4受容体注3)というタンパク質のミクログリアでの増加が神経障害性疼痛に重要であることを英国科学誌Natureで発表していますが、実は今回見つかったIRF5がP2X4受容体を増やす実行役であることも明らかにしました。この研究成果は、慢性疼痛メカニズムの解明へ向けた大きな前進となり、痛みを緩和する治療薬の開発に応用できることが期待されます。
本研究は、最先端・次世代研究開発支援プログラム、および独立行政法人 科学技術振興機構(JST) 戦略的創造研究推進事業 チーム型研究(CREST)の成果で、英国科学誌『Nature Communications』オンライン版に2014年5月13日付け(英国時間)で発表されます。
本研究は、最先端・次世代研究開発支援プログラム(NEXT)における研究課題「ミクログリア転写因子IRF8を切り口にした慢性疼痛メカニズムの解明」(研究代表者:津田 誠 九州大学 大学院薬学研究院 准教授、研究期間:2010~2013年度)、および独立行政法人 科学技術振興機構(JST) 戦略的創造研究推進事業 チーム型研究(CREST)「炎症の慢性化機構の解明と制御に向けた基盤技術の創出」(研究総括:宮坂 昌之 大阪大学 未来戦略機構 特任教授、フィンランドアカデミー FiDiPro 教授)における研究課題「脳内免疫担当細胞ミクログリアを主軸とする慢性難治性疼痛発症メカニズムの解明」(研究代表者:井上 和秀 九州大学 大学院薬学研究院 教授、研究期間:2010~2015年度)の研究成果です。
<背 景>
がん、糖尿病、帯状疱疹あるいは脳卒中などで神経に障害が起きると、抗炎症薬やモルヒネなどの鎮痛薬が効きにくい「神経障害性疼痛」という慢性痛が発症し、服が肌に触れただけでも非常に痛みを感じることがあります。しかし、これまでそのメカニズムは明らかになっておらず、効果的な治療法もありません。研究グループでは、脳や脊髄の免疫細胞と呼ばれる「ミクログリア」が、神経損傷後の脊髄で活性化した状態になり、それが慢性的な痛みを引き起こしていることを明らかにしてきました(Nature 2003;Nature 2005;PNAS 2009;EMBO J 2011;Cell Rep 2012)。ミクログリアは、細胞の働きを調節するタンパク質が増えることで活性化状態となりますが、その中でも、私たちが2003年にNature誌に発表したP2X4受容体は神経障害性疼痛の発症に非常に重要な役割を果たしていると考えられています。しかし、どのようなメカニズムでP2X4受容体がミクログリアの中だけで増えるのかは長らく不明でした。
<内 容>
今回研究グループは、神経を損傷させたマウスの脊髄で、様々な遺伝子の発現をコントロールするタンパク質「IRF5」がミクログリアの中だけで増えることを発見しました。この増加は、2012年に米国科学誌Cell Reportsで報告したIRF8によって調節されていることもわかりました。また、IRF5を作り出せないように遺伝子を操作したマウス(IRF5遺伝子欠損マウス)では、神経損傷後の痛みが弱くなっていました。さらに、IRF5がP2X4受容体の調節に必要な遺伝子領域に作用し、P2X4受容体を増やすように働いていることを明らかにしました。
したがって、神経損傷後、IRF8によってミクログリアで増えるIRF5がP2X4受容体を増やすという一連の流れが、神経障害性疼痛を引き起こす原因であることを明らかにしました(図1)。
<効 果>
今回研究グループが特定したIRF5は、神経障害性疼痛に重要なP2X4受容体を増やし、ミクログリアを「痛みモード」にかえる実行役のような働きをしています。したがって、IRF5の働きを抑える薬が開発されれば、ミクログリアを正常化し、神経障害性疼痛を緩和できる可能性があります。
<今後の展開>
現在、九州大学 大学院薬学研究院では、既承認医薬品から新しい作用を見つけ、より早く臨床で使用できるようにするための研究「エコファーマ注4)」を同研究院附属 産学官連携創薬育薬センター(センター長:井上 和秀)において推進しており、現在建設中の「グリーンファルマ研究所(仮称)」(平成26年度末竣工予定)において、さらに推進していく予定です。今回の研究で、神経の損傷後にミクログリア細胞でIRF5が増えることが慢性疼痛の原因であることを明らかにしましたので、今後、IRF5が増えるのを抑制する、あるいはIRF5がP2X4受容体遺伝子に作用するのを抑制する薬などを既承認医薬品から探索する計画を検討しています。
<参考図>
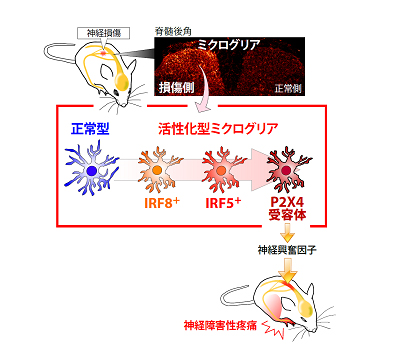
図1
<論 文>
Takahiro Masuda, Shosuke Iwamoto, Ryohei Yoshinaga, Hidetoshi Tozaki-Saitoh, Akira Nishiyama, Tak W. Mak, Tomohiko Tamura, Makoto Tsuda*, Kazuhide Inoue* (*Corresponding Authors)
Transcription factor IRF5 drives P2X4R+ reactive microglia gating neuropathic pain
Nature Communications doi: 10.1038/ncomms4771
<共同研究グループ>
九州大学 大学院薬学研究院 薬理学分野:井上 和秀(主幹教授)、津田 誠(准教授)、増田 隆博(特任助教)、岩本 祥佑(大学院生)、吉永 遼平(大学院生)、齊藤 秀俊(助教)
横浜市立大学 医学部 免疫学:田村 智彦(教授)、西山 晃(准教授)
トロント大学:Tak W. Mak(教授)
<用語解説>
- 注1) IRF5
- インターフェロン調節因子5(interferon regulatory factor 5)。インターフェロン調節因子ファミリーに属する。細胞の核内にあるDNAに結合して、様々な分子の発現を調節し、免疫制御に関わっている。しかし、脳や脊髄における役割はわかっていなかった。
- 注2) ミクログリア細胞
- 脳や脊髄に存在する免疫細胞と呼ばれ、中枢神経系を構成する細胞の約5~20%を占める。正常状態では細長い突起を動かしながら周囲の環境を監視している。しかし、神経細胞の障害などにより、過度に活性化すると、炎症性物質(炎症性サイトカインなど)を産生し、神経細胞の機能異常などを引き起こすことが知られている。
- 注3) P2X4受容体
- 細胞の外にあるATPで刺激されるタンパク質。細胞膜上にあるイオンチャネル型受容体で、ATPで刺激されると細胞の中に陽イオンを入れ、細胞を興奮させる。神経の障害後にミクログリアだけで増え、この受容体を遮断する薬物で痛みが緩和される(2003年にNature誌で発表)。新規P2X4受容体遮断薬の開発が産学官の連携で現在進行中。
- 注4) エコファーマ
- 九州大学 大学院薬学研究院では、これまで、既承認医薬品から新しい薬理作用を見出し、それを基に新しい創薬シーズを探索する「エコファーマ」を独自に推進してきた。エコファーマは、既承認薬の膨大な基礎資料とヒトへの安全性から、短期間・低コストで安全な薬を創ることを可能にし、患者さんに短期間で治療薬を提供できる有効なストラテジーとして注目されている。
<お問い合わせ先>
<研究に関すること>
井上 和秀
九州大学 大学院薬学研究院 教授
Tel:092-642-4729 Fax:092-642-4729
E-mail:
津田 誠
九州大学 大学院薬学研究院 准教授
Tel:092-642-6628 Fax:092-642-4729
E-mail:
<JST事業に関すること>
川口 貴史
科学技術振興機構 戦略研究推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail:
<報道担当>
九州大学 広報室
〒819-0395 福岡県福岡市西区元岡744
Tel:092-802-2130 Fax:092-802-2139
E-mail:
URL: http://www.kyushu-u.ac.jp
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432
E-mail: