<ポイント>
- 合成ラミニンを用いた分化誘導法により、ドパミン神経細胞の大量培養が可能になった。
- 抗コリン抗体を用いたセルソーティング(細胞選別)によってドパミン神経前駆細胞を選別することで、より安全かつ効率的な細胞移植が可能になった。
- iPS細胞を用いたパーキンソン病治療の臨床応用に向けたプロトコールを確立した。
土井 大輔 研究員、髙橋 淳 教授(京都大学 CiRA 臨床応用研究部門)らの研究グループは、大阪大学および株式会社カン研究所と共同研究を行い、臨床応用に向けたヒトiPS細胞由来ドパミン神経前駆細胞の製造方法を開発しました。これまでヒトiPS細胞から誘導したドパミン神経細胞の移植でパーキンソン病モデルラットの運動機能の改善は報告されていますが、臨床応用を行うには大量培養法の開発と腫瘍化の危険性がある細胞の排除が必要と考えられてきました。今回開発された方法では、合成ラミニン注1)(大阪大学 蛋白質研究所が開発した組換えラミニン511E8フラグメント)を用いた接着培養をすることで従来の20倍以上の濃度で細胞を培養することが可能になり、さらに株式会社カン研究所で開発された抗コリン抗体注2)を用いたセルソーティングを行うことで、ドパミン神経前駆細胞の選別・濃縮が可能となりました。この方法で作製した細胞をパーキンソン病モデルラットの脳内に移植したところ、腫瘍を形成せず運動機能の改善をもたらし、より安全かつ効率的なドパミン神経細胞移植が可能になることが明らかになりました。
本成果は2014年3月6日(米国東部時間)に米国科学誌「Stem Cell Reports」で公開されます。
本研究は、下記機関より資金的支援を受けて実施されました。
- 文部科学省 再生医療の実現化ハイウェイ
- 科学技術振興機構(JST) 再生医療実現拠点ネットワークプログラム
- 文部科学省 橋渡し研究加速ネットワークプログラム<大阪大学>
<研究の背景>
パーキンソン病は、中脳黒質から線条体に投射するドパミン神経細胞注3)が減ることで脳内のドパミン量が減り、手足の震えや体のこわばり、運動減少などの症状が出る進行性の神経難病です。従来の薬物や電極を用いた治療法では症状の改善はできてもドパミン神経細胞の減少を食い止めることはできず、病状の悪化に伴い症状の改善が困難になります。そこで、細胞移植によってドパミン神経細胞を補い、新たな神経回路の形成を促して脳の機能を再生させるという、より積極的な治療法に期待が寄せられています。ヒトiPS細胞はその移植細胞の供給源の1つと考えられています。
iPS細胞は、高い増殖性を持つことが特徴の1つですが、その反面、移植片として患者さんに投与する際には、増殖能力を持った細胞が残り腫瘍化するリスクを常に考慮する必要があります。髙橋教授らのグループでは、以前にヒトES細胞由来の神経細胞を霊長類に移植した実験で、ES細胞由来のドパミン神経細胞が多数脳内に生着し神経症状を改善させることを明らかにしました(Doi et al., Stem Cells 2012)。この実験ではヒトES細胞の残存は見られなかったものの未熟な神経細胞がわずかに増殖していることが観察されました。また、以前の方法では移植片の中でもさまざまな細胞が混在しており、パーキンソン病治療に必要とされるドパミン神経細胞が含まれる割合は比較的低いものでした。したがって臨床応用に際しては、増殖の可能性のある細胞を排除し、ドパミン神経細胞の割合を高めることが必要でした。また臨床応用を行うには1000万~1億個台と大量の細胞が必要で、さらに動物由来成分を含まない条件で培養する必要があり、新たな培養法の開発が必要でした。これらの課題を解決するために、分化誘導方法を改良し、セルソーティング(FACS)注4)によるドパミン神経前駆細胞の選別を試みました。
<研究結果>
1)ヒトiPS細胞から合成ラミニン上でドパミン神経細胞を作製し、ソーティングを行った
これまで神経誘導のための接着培養ではマトリゲルというマウス細胞由来の基質が用いられていましたが、動物由来であるため臨床に用いることはできません。そこで我々は大阪大学 蛋白質研究所と共同研究を行い、ヒトiPS細胞をマトリゲルの代わりに組換えラミニン511E8フラグメント上で培養し、ドパミン神経前駆細胞を誘導しました。高密度培養を行うことにより従来の浮遊培養法(Serum-Free Embryonic Body quick:SFEBq法)注5)と比較して20倍以上の神経前駆細胞を得ることができました。さらに株式会社カン研究所と共同研究を行い、胎生期の神経管の腹側で発現しているコリンという表面抗原注6)を用いてソーティングを行ったところ、ドパミン神経前駆細胞のマーカーであるFOXA2とLMX1Aを発現する細胞が約80%まで濃縮されました。選別された細胞は高効率にドパミン神経細胞へと分化し、脱分極注7)してドパミン分泌を行っていることも確認されました。
2)ソーティングした移植片は脳内で増大せず、ドパミン神経細胞として機能
パーキンソン病モデルラットの脳内へ移植することにより、作製したドパミン神経前駆細胞の安全性と有効性について検討しました。移植後4ヵ月の時点では、ソーティングした細胞由来の移植片はソーティングしないものよりも移植片が均一で有意に小さく、移植片内の増殖細胞はごくわずか(0.1%未満)でした。ラットの運動機能は改善し、脳切片の免疫染色では、ソーティングした細胞の移植片で有意に多くのドパミン神経細胞が生着していました。また、ソーティングのタイミングや移植のタイミングについて検討を行ったところ、分化誘導開始後12日目にソーティングを行い28日目に移植を行った場合に最良の結果が得られることが明らかになりました。
<本研究の意義と今後の展望>
iPS細胞を用いた細胞移植治療では、増殖性細胞の残存による移植片の腫瘍化が問題とされてきました。本研究では、抗コリン抗体を用いたセルソーティングを行うことで腫瘍化の危険性がある細胞を除去し、さらに移植片内の中脳ドパミン神経細胞の割合を高めることで、より安全かつ効率的な移植が可能となりました。また、iPS細胞の培養や神経誘導にはマウス由来のフィーダー細胞が必要でしたが、そのままでは臨床応用はできません。神経誘導の際には浮遊培養が可能でしたが、大量培養には不向きでした。今回、組換えラミニン511E8フラグメントを使用することで、臨床に使用できる細胞を大量に培養することが可能になりました。このような改良を加えることで臨床応用に向けたプロトコールを確立できたことに意義があります。
今回の実験ではモデルラットへの移植で4ヵ月間の経過観察を行い、プロトコールを確立しました。臨床応用を開始する前に、このプロトコールで作製された細胞を霊長類モデルにも移植し、より長期の経過観察を行うことによって、安全性や有効性をより詳細に確認する予定です。また、iPS細胞は自家移植が可能ですが、パーキンソン病患者さん由来のiPS細胞から作製したドパミン神経が脳内で機能するかについても検討が必要です。これらの課題をクリアした上で、臨床応用に進みたいと考えています。
<参考図>
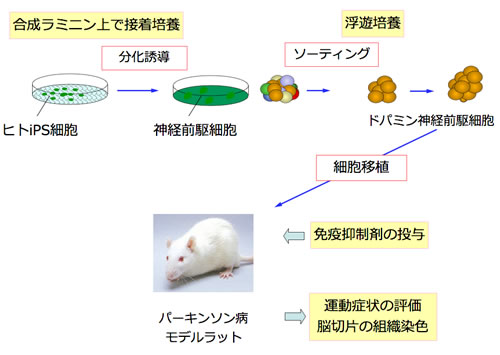
図1 実験の概要
iPS細胞を分化誘導し、ドパミン神経前駆細胞を選別する。得られた細胞をさらに浮遊培養し、パーキンソン病モデルラットの脳内に移植し、運動症状の評価、脳切片の組織染色を行う。
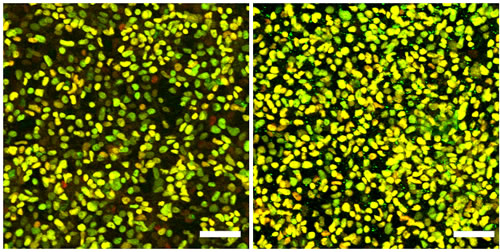
図2 ヒトiPS細胞から作製したドパミン神経前駆細胞の免疫染色
抗コリン抗体を用いて選別することで、ドパミン神経前駆細胞に特徴的なマーカー(緑:FOXA2、赤:LMX1A)で染色される細胞(黄色)が濃縮できた。左はソーティングなし、右はソーティングあり。
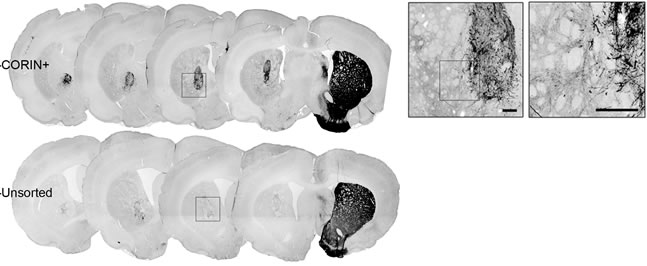
図3 脳切片のドパミン神経マーカー(TH)による免疫染色
ソーティングした細胞由来の移植片では多数のドパミン産生神経細胞が生着し、周辺の脳組織へ神経突起を伸ばしている。CORIN+:ソーティングあり、Unsorted:ソーティングなし。右図はCORIN+の拡大。
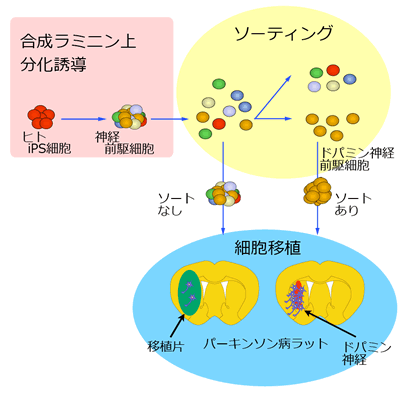
図4 本研究の成果
iPS細胞から組換えラミニン511E8フラグメント上で分化誘導した細胞のセルソーティングを行い、ドパミン神経前駆細胞を選別した。これらの細胞をモデルラットの線条体に移植したところ、腫瘍性増殖性はみられず多くの中脳ドパミン神経細胞が生着した。
<用語解説>
- 注1)ラミニン
- 細胞を接着させるために重要なタンパク質。上皮細胞や筋細胞、血管内皮細胞などさまざまな細胞で分泌合成されている。さまざまなタイプのラミニンがあり、細胞の種類によって作られているラミニンは異なる。なお本研究では、大阪大学 蛋白質研究所で開発した組換えラミニン511E8フラグメントが使用された。
- 注2)抗コリン抗体
- コリン(CORIN)という物質だけを特異的に認識する抗体。この抗体に蛍光物質を結合させておくことで、表面にコリンを持っている細胞だけに蛍光標識することができ、セルソーティング(後述)が可能となる。なお、本研究で用いた抗コリン抗体は株式会社カン研究所、尾野 雄一 研究員のグループにて作製された。
- 注3)ドパミン神経細胞
- 神経細胞の1種で、神経伝達物質としてドパミンを放出する。多くのパーキンソン病では、中脳黒質にあるドパミン神経細胞の変性が見られる。
- 注4)セルソーティング(FACS:Flurorescence-activated cell sorting)
- 目的の細胞だけを分取する技術。FACSは、蛍光抗体で染色した細胞を液流に乗せて流し、レーザー光の焦点を通過させ、個々の細胞が発する蛍光を測定することによって細胞表面にある抗原量を定量的に測定し、その情報をもとに特定の細胞だけを生きたまま無菌的に分取できる。
- 注5)浮遊培養法(Serum-Free Embryonic Body quick:SFEBq法)
- 細胞をバラバラに分散させて、数千個程度の固まりにした状態で培養する方法。細胞が浮遊しているので培養皿に貼り付けるための物質(マトリゲルやラミニン)が不要。
- 注6)表面抗原
- 抗体が認識する細胞表面にある物質のこと。この論文ではコリンのこと。
- 注7)脱分極
- 神経細胞の活動の1つ。細胞膜内にはマイナスの静止膜電位が存在しているが、刺激を受けるとマイナスの電位が減少する。これを脱分極という。脱分極により膜電位がある程度まで減少すると、能動的な活動電位が生じる。
<論文名と著者>
○論文名
“Isolation of Human Induced Pluripotent Stem Cell-derived Dopaminergic Progenitors by Cell Sorting for Successful Transplantation”
○ジャーナル名
Stem Cell Reports
○著者
Daisuke Doi1, Bumpei Samata1, Mitsuko Katsukawa1, Tetsuhiro Kikuchi1, Asuka Morizane1, Yuichi Ono2, Kiyotoshi Sekiguchi3, Masato Nakagawa1, Malin Parmar4, and Jun Takahashi1, 5, 6
○著者の所属機関
1. 京都大学 iPS細胞研究所(CiRA)
2. 株式会社カン研究所
3. 大阪大学 蛋白質研究所
4. ルンド大学 ワレンベルグ 神経科学センター
5. 京都大学 再生医科学研究所
6. 京都大学 大学院医学研究科
○DOI
doi: 10.1016/j.stemcr.2014.01.013
<お問い合わせ先>
<研究内容に関すること>
京都大学 iPS細胞研究所(CiRA)
研究支援部門 国際広報室 和田濵
Tel:075-366-7005 Fax:075-366-7023
E-mail:
<JSTの事業に関すること>
科学技術振興機構 再生医療研究推進部
Tel:03-5214-8427 Fax:03-5214-7810
<報道担当>
科学技術振興機構 広報課
Tel:03-5214-8404 Fax:03-5214-8432