ポイント
- 医薬品開発などで、薬物の標的たんぱく質を探し出す手法が求められています。
- 標的たんぱく質と結合すると同時に蛍光体に変化する小さな分子を開発しました。
- 医薬品開発やたんぱく質を対象にした生命現象の理解に有力な手段を提供します。
JST 課題達成型基礎研究の一環として、理化学研究所の袖岡 幹子 主任研究員らは、生きた細胞の中で薬物の標的たんぱく質注1)を選択的に光らせて探し出すラベル化法を開発しました。
医薬品開発などでは、薬物と結合する標的たんぱく質を探し出すことは、副作用の軽減やさらなる効果を発揮する薬剤開発につながるため極めて重要です。細胞内に存在する数多くの生体物質の中から、標的たんぱく質を見つけ出すことは容易ではありません。有効な手段の1つとして、標的たんぱく質に目印をつけることができる「アフィニティーラベル化法注2)」があります。しかし、この方法ではその目印となる分子(反応基注3)と蛍光基注4))が大きいため、標的たんぱく質との相互作用を損なうことがしばしばあり、狙った通りに探し出すことが困難でした。このため、新しいラベル化法の開発が望まれていました。
今回研究グループは、標的たんぱく質との相互作用を損なわないように反応基と蛍光基をできるだけ小さくすることを目指し、分子サイズの小さなニトロベンゾオキサジアゾール(NBD)という物質に着目しました。この物質は通常無蛍光ですが、たんぱく質中に存在するアミノ基と反応して蛍光を発します。そこで、このNBDを反応基と蛍光基の2つの機能を併せ持つ目印分子として利用することを考案しました。この分子の特徴は、そのもの自体が小さいだけではなく、標的たんぱく質と結合すると同時に蛍光体に変化することです。結合しない場合は蛍光を発しないため、背景ノイズを抑え高感度に検出することができます。このラベル化法を、ミトコンドリア外膜の膜たんぱく質であるトランスロケーターたんぱく質(TSPO)に適用したところ、その実用性を生きた細胞で確認することに成功しました。
今回開発したラベル化法では、標的たんぱく質との相互作用を損なわないため、いまだ作用メカニズムが分からない薬物の標的たんぱく質の発見に貢献できます。また、生きた細胞内でたんぱく質の動きの追跡などが可能となり、医薬品開発の推進やたんぱく質の機能解明に有力な手段となることが期待されます。
本研究成果は、英国王立科学会誌「Chemical Science」のオンライン速報版で近日中に公開されます。
本成果は、以下の事業・研究プロジェクトによって得られました。
戦略的創造研究推進事業
| 研究プロジェクト |
「袖岡生細胞分子化学プロジェクト」 |
| 研究総括 |
袖岡 幹子(理化学研究所 袖岡有機合成化学研究室 主任研究員) |
| 研究期間 |
平成20年10月~平成26年3月 |
上記研究課題では、生命の根幹を担う現象である「細胞死」の仕組みを明らかにすべく、細胞死を制御する低分子化合物「細胞死制御分子」と新しい化学的解析手法の開発を行い、これらを組み合わせることで分子レベルでの解明を目指します。
<研究の背景と経緯>
医薬品開発の基礎研究の段階においては、新薬候補である物質(リガンド注5))の探索に引き続き、リガンドに結合する標的たんぱく質を探し出し、その機能を理解することが重要となっています。数万種類以上の生体分子が存在する極めて複雑な細胞内で、リガンドと相互作用する特定のたんぱく質を探し出すことは容易ではありません。
これまで、標的たんぱく質を探し出す方法がいくつか提案されています。それらの中で、生きた細胞内でも利用できる有力な手法として、「アフィニティーラベル化法」が挙げられます。この手法では、一般的にリガンド部位、反応基および蛍光基から構成されるプローブ(探索)分子が用いられます。その原理は以下の通りです(図1a)。まず、プローブ分子のリガンド部位(鍵)が細胞内で標的たんぱく質(鍵穴)を認識します。次に、反応基が標的たんぱく質と結合(捕捉)します。蛍光基は、捕捉された標的たんぱく質の細胞内での位置確認や分離・精製するための目印で、分離・精製されたたんぱく質は最後に質量分析などを用いて同定が行われます。そのため、本手法にとって反応基と蛍光基の両者は欠かせないものです。
しかし、これら複数の官能基注6)を導入したプローブ分子は、本来のリガンドの能力である「認識機能(標的たんぱく質に対する親和性や選択性)」を損なうことが少なからずあり、標的たんぱく質の発見を困難にしていました。この問題を解決するには、反応基と蛍光基をできるだけ小さく、すなわちリガンドと標的たんぱく質の相互作用を損なわない形にする必要がありますが、汎用性の高い優れた方法はこれまでありませんでした。
<研究の内容>
本研究グループでは、アフィニティーラベル化法のプローブ分子設計を根本的に変えることにしました。着目したのは、分子サイズの小さなNBD(分子量180)というユニットです。1980年代の論文で、NBDに酸素原子が結合したO-NBDがアミン類と反応して蛍光性のN-NBDを与えるという報告がありました。そこで、リガンドにO-NBDユニットだけを導入したシンプルなプローブ分子を考案しました(図1b)。
このプローブ分子の優れた点は、反応基(O-NBD)が蛍光基(N-NBD)へと変化する点で、リガンドの化学修飾を最小限に抑えることが可能になります。従来法との違いはこれだけではありません。ラベル化反応と同時に、蛍光を発するという点も大きな特徴です。プローブ分子自体は無蛍光であるものの、標的たんぱく質と反応すると蛍光を示すため、結合していないプローブ分子に邪魔されることなく高感度なイメージングが可能になります。
以上の概念が実際に機能することを証明するために、まず入手容易なビオチン・アビジン注7)を用いたモデル実験を行いました。ビオチンとアビジンは、リガンドと標的たんぱく質の関係にあります。はじめに、ビオチンにO-NBDユニットを導入し、プローブ分子を作成しました。次に、プローブ分子をアビジン含有のたんぱく質混合物へと添加し、どのたんぱく質が蛍光ラベル化されたか解析を行いました。その結果、アビジンが99.9%以上の高い選択性で蛍光ラベル化されたことが分かりました。また、予想通りラベル化が蛍光の発光(turn-ON)を伴って進行することも確認できました。さらに、質量分析によりラベル化部位が、ビオチン結合サイト近くのリジン残基であることを突き止め、本手法がリガンドの結合サイト解析に利用できることも明らかにしました。
次に、TSPOというたんぱく質に焦点を当て、本ラベル化法の実用性を確認することにしました。TSPOは、ミトコンドリア外膜に発現する膜たんぱく質で、電位依存性アニオンチャンネル(VDAC)やアデニンヌクレオチド転位酵素(ANT)など、ほかのたんぱく質と複合体を形成することが分かっています(図2)。近年、TSPOのリガンドは神経変性障害、炎症または不安神経症などの治療薬のリード化合物(新薬の候補となる化合物)として注目を集めていますが、その中で比較的最近開発されたTSPOリガンドとしてN,N-ジ-n-ブチル-2-フェニルインドール-3-イルグリオキシルアミド(PIGA)があります。そこで、PIGAにO-NBDユニットを導入し、マウス腎臓から単離したミトコンドリアのラベル化を試みました。質量分析で詳細に解析を行ったところ、興味深いことに蛍光ラベル化されたのは標的たんぱく質のTSPOではなく、TSPOと複合体を形成している相手のたんぱく質であるVDACだということが分かりました。この結果は、TSPOリガンドがTSPOとVDACの接触部位に結合することを示唆するもので、作用機構を理解する上で重要な知見です。続いて、腎臓由来の培養細胞でもラベル化を試みたところ、ラベル化はTSPO-VDAC-ANT複合体が存在するミトコンドリアで選択的に進行し、本手法が生細胞内でも機能することが証明できました(図3)。
<今後の展開>
今回、O-NBDユニットを用いた新しいアフィニティーラベル化法を考案し、生きた細胞内で標的たんぱく質複合体を選択的に蛍光ラベル化することに成功しました。本手法は、元の化合物の特性を損なうことなく利用できることから、広くさまざまな化合物に適用できると期待されます。従って、いまだ作用メカニズムが不明の薬物の標的たんぱく質の発見に貢献する可能性があります。特に、既存の手法では解析が難しい膜たんぱく質複合体などを標的とする化合物にも適応できる可能性があります。イオンチャネル、受容体や膜輸送体などの膜たんぱく質は、医薬品開発の主要な標的であり、今後、新しく開発したラベル化法は、生命現象の理解のみならず医薬品開発の推進に有力な手段となることが期待されます。
<参考図>
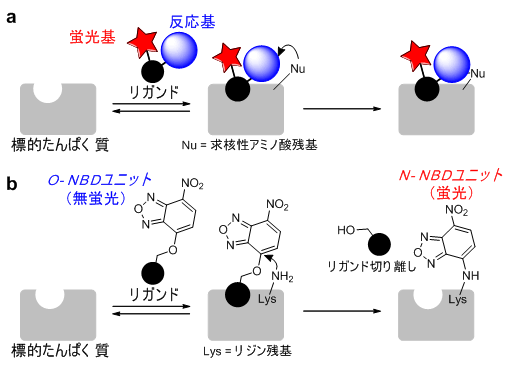
図1 標的たんぱく質のラベル化
- (a)リガンド、反応基および蛍光基からなるプローブ分子による一般的なアフィニティーラベル化(従来法)
蛍光基、反応基とリガンドの3ユニットからなる大きなプローブ分子では、標的たんぱく質に対する親和性や選択性がしばしば損なわれる。
- (b)リガンドおよびO-NBDからなるプローブ分子によるアフィニティーラベル化(新規開発法)
リガンドおよびO-NBDの2ユニットからなるプローブ分子のO-NBDが標的たんぱく質と結合しN-NBDに変化することにより蛍光を発する。
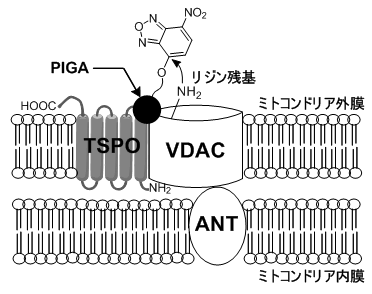
図2 ミトコンドリア膜のTSPOたんぱく質複合体モデル
PIGAがミトコンドリア外膜に存在するVDACとTSPOとの接触部位に結合する様子を示す。
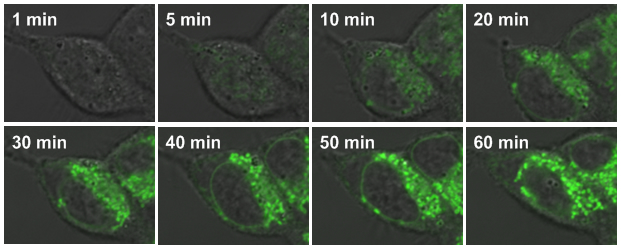
図3 PIGAと相互作用するたんぱく質の生細胞イメージング
腎臓由来の培養細胞をPIGAおよびO-NBDからなるプローブ分子でラベル化した。ラベル化は時間経過とともにTSPO-VDAC-ANT複合体が存在するミトコンドリアで選択的に進行した。10分を過ぎると次第にミトコンドリアが緑色に発光し、ミトコンドリアのたんぱく質にプローブ分子が結合している様子が認められる。
<用語解説>
- 注1)標的たんぱく質
- リガンドの標的となるたんぱく質。創薬分野では創薬ターゲットということがある。
- 注2)アフィニティーラベル化法
- 親和性標識法。DNA-たんぱく質、たんぱく質-たんぱく質や生理活性物質-たんぱく質などの両者に特異的な相互作用を利用して、結合部位で架橋する方法。
- 注3)反応基
- 化学反応性を示す原子団。水酸基、アミノ基、アルコキシ基、カルボキシル基など。
- 注4)蛍光基
- 蛍光基は特定の波長の光を吸収し、蛍光を放つ性質を持つ。代表的なものとして、フルオロセインがあり、これは495nm付近で励起され、520nm付近に蛍光を発する。
- 注5)リガンド
- 特定の受容体に特異的に結合する物質。リガンドは受容体の特定の部位に結合し、高選択的な親和性を示す。
- 注6)官能基
- 性質・機能を与える原子団。反応基、蛍光基などが含まれる。
- 注7)ビオチン・アビジン
- アビジンは生卵白中に存在する低分子の塩基性糖たんぱく質で、4個のサブユニットから構成され、各サブユニットは1分子のビオチン(D-[(+)-cis-ヘキサヒドロ-2-オキソ-1H-チエノ-(3,4)-イミダゾール-4-吉草酸]、ビタミンB6)と強く結合する。生化学の研究用試薬あるいはがんの検査用試薬などに用いられる。
<論文タイトル>
“Turn-ON fluorescent affinity labeling using a small bifunctional O-nitorobenzoxadiazole unit”
(小さな2官能性O-ニトロベンゾオキサジアゾールを用いたターンオン型蛍光アフィニティーラベル化)
doi: 10.1039/C3SC52704B
<お問い合わせ先>
<研究に関すること>
袖岡 幹子(ソデオカ ミキコ)
理化学研究所 袖岡有機合成化学研究室 主任研究員
〒351-0198 埼玉県和光市広沢2-1
Tel:048-467-9373 Fax:048-462-4666
E-mail:
<JSTの事業に関すること>
坂本 祥純(サカモト ヨシズミ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail: