ポイント
- アレルギー疾患発症は免疫系の過剰反応やバランスの乱れが原因です。
- 遺伝子発現を抑制するたんぱく質「EZH2」分子が免疫反応のブレーキ役として免疫系のバランスを調節する機構を解明しました。
- EZH2分子を制御すれば、アレルギー疾患の治療への道が開けると期待されます。
JST 課題達成型基礎研究の一環として、千葉大学 大学院医学研究院の中山 俊憲 教授らのグループは、遺伝子発現を抑制するたんぱく質「EZH2」分子が免疫反応のブレーキ役であることを発見しました。
ぜんそく、アトピー性皮膚炎、アレルギー性鼻炎などのアレルギー疾患は増加の一途をたどっており、国民の約3割がこれに罹患しているとの報告もあります。従来のアレルギー疾患に対する治療法は対症療法しかなく、根治療法の開発が望まれています。
本研究グループは、遺伝子発現を抑制するたんぱく質として知られていたEZH2が、免疫系にも作用して過剰な免疫応答を抑える働きがあることを明らかにしました。さらに、EZH2結合遺伝子の遺伝子地図注1)を作製することで、EZH2が免疫系の遺伝子に直接作用する機構の一端を解明しました。
今後、EZH2やEZH2が結合しているたんぱく質を創薬ターゲットとすることで、将来的に慢性の難治性アレルギー疾患の治療開発に役立つことが期待されます。また、それとは逆に、免疫力の低下した患者に対する治療への応用も考えられます。
本研究は、理化学研究所 統合生命医科学研究センターの古関 明彦 グループディレクター、東京大学の鈴木 穣 教授の協力を得て行いました。
本研究成果は、2013年11月14日(米国東部時間)発行の米国科学誌「Immunity」オンライン版に掲載されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域 |
「炎症の慢性化機構の解明と制御に向けた基盤技術の創出」
(研究総括:宮坂 昌之 大阪大学 未来戦略機構 特任教授)
|
| 研究課題名 |
「気道炎症の慢性化機構の解明と病態制御治療戦略の基盤構築」 |
| 研究代表者 |
中山 俊憲(千葉大学 大学院医学研究院 教授) |
| 研究期間 |
平成23年10月~平成29年3月 |
JSTはこの領域で、炎症が慢性化する機構を明らかにし、慢性炎症を早期に検出し、制御し、消退させ、修復する基盤技術の創出を目的とします。上記研究課題では、記憶Th細胞分画のサイトカイン産生制御機構に着目した解析を行うことで気道炎症の慢性化のメカニズムを解明し治療戦略の基盤構築を目指します。
<研究の背景と経緯>
アレルギー疾患は、国民の3人に1人が罹患しているにもかかわらず、未だに効果的な予防法や根治療法は開発されていません。一旦発症すると慢性化することが多く治療が長期にわたり、患者の肉体的、精神的、経済的負担が極めて大きいことから、現代医学が解決すべき大きな課題の1つとなっています。
アレルギー疾患の発症や病態には、免疫反応が過剰になることが原因となっています。免疫反応の司令塔であるヘルパーT(Th)細胞注2)は、産生するサイトカイン注3)の種類によって、免疫反応を活性化に関わるTh1、Th2、Th17細胞と、逆に免疫反応の収束や抑制に関わる制御性T(Treg)細胞に分けられます(図1)。これらのT細胞は、通常は互いにバランスを取りながら正常な免疫反応を担っていますが、バランスが崩れてTh2細胞優位になった場合に、アレルギー疾患が発症すると考えられています。Th2細胞は、インターロイキン(IL)-4や、IL-5、IL-13といったサイトカイン(Th2サイトカイン)を分泌して、抗体(IgE)産生や好酸球の遊走・組織浸潤などを誘発することから、アレルギー疾患の根幹に位置する細胞であると言えます。
本研究グループは、このTh2細胞の分化や機能を制御することによりアレルギー反応の抑制が可能となり、将来的には難治性の慢性アレルギー疾患の根治療法の開発につながると考えて、研究を行ってきました。
一方、たんぱく質「EZH2」は遺伝子に後天的(エピジェネティック)な作用を加えて遺伝子の発現を抑制するたんぱく質で、ポリコーム群たんぱく質注4)と呼ばれます。ポリコーム群たんぱく質は元々ショウジョウバエで発見されましたが、その後の研究によりヒトES細胞などの幹細胞で重要な働きをしていること、この変異ががん細胞の発生の引き金になることなどが分かってきました。しかしEZH2の免疫系での働きについてはほとんど解明されていませんでした。
<研究の内容>
本研究グループは、EZH2は生体内の遺伝子発現に対して抑制的に働くことから、免疫系においては過剰な免疫反応を抑える機能があるのではないかという仮説を立て、EZH2欠損マウスを用いた研究を行いました。
EZH2欠損マウス由来のTh細胞は、予想通りにTh1サイトカインであるインターフェロンガンマ(IFNγ)とTh2サイトカインであるIL-4、IL-5、IL-13を過剰に産生することが分かりました(図3)。次に、この原因を詳しく調べるために、ChIP-seq法注5)という最先端の手法で、EZH2が結合する場所の遺伝子地図を作製しました。当初の予想に反して、EZH2欠損マウスで過剰に産生されていたサイトカイン遺伝子にはEZH2が結合しにくく、EZH2は直接サイトカインの産生を抑制していないことが明らかになりました。一方で、これらのサイトカインを上流で制御している転写因子注6)の遺伝子にはEZH2が結合しやすく、その発現を抑制しやすいということが分かりました(図4)。以前の研究により、IFNγの産生にはT-betという転写因子が、IL-4、IL-5、IL-13の産生にはGATA3という転写因子がそれぞれ重要であることが分かっています。今回の研究で新たに解明されたメカニズムは、EZH2はT-betやGATA3の発現を適切なレベルに制御することにより、その下流にあるサイトカインの過剰産生、すなわち過剰な免疫応答を抑制していることです(図5)。
このメカニズムは、マウス個体を用いた実験でも確認されました。アレルギー性気道炎症モデルマウス(マウス喘息モデル)に野生型とEZH2欠損型のTh2細胞を移入し、アレルギーの発症と病態について検討しました。その結果、EZH2欠損型マウスのTh2細胞を移入すると、アレルギーの指標である気道肺胞洗浄液中への好酸球の浸潤や気道過敏性の反応が見られ、EZH2による過剰な免疫応答のブレーキ機能が破綻していると考えられます(図6)。
<今後の展開>
遺伝子抑制性たんぱく質EZH2は、Th1、Th2サイトカインの両方を制御する働きがあることから、過剰な免疫応答を抑制する基本的な分子であると言えます。ただし生体内での異常から推測すると、Th2細胞抑制に対する寄与の方が大きいと考えられます。また、本研究結果から、慢性的にアレルゲンにさらされ、ヘルパーT細胞が持続的に刺激されると、EZH2による免疫系のブレーキ機構が破綻することが新たに分かりました。EZH2の異常がアレルギーの慢性化を引き起こす原因となるといった新たな炎症の慢性化の仮説も提唱できます。
EZH2やEZH2が結合しているたんぱく質複合体(ヒストンH3K27メチル化酵素複合体)を創薬ターゲットとしてさらにその詳細なメカニズムを解明し、EZH2を適切に働かせることで過剰な免疫応答の抑制法に、逆にEZH2を抑制させることで免疫力の低下した患者に対する治療法につながることが期待されます。
<参考図>
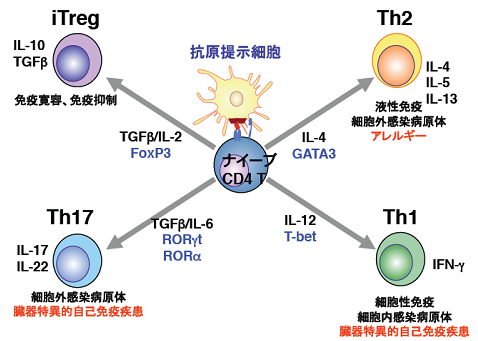
図1 ヘルパーT細胞(Th1/Th2/Th17/iTreg細胞)の分化と免疫応答・疾患
ナイーブCD4 T細胞は、抗原提示細胞が提示する抗原によって活性化され、周囲の環境中にあるサイトカインなどの影響によりさまざまな種類のヘルパーT細胞へと分化する。図中に、各ヘルパーT細胞の種類、分化に必要なサイトカインなどの因子、細胞自身が分泌するサイトカイン、関係する疾患を示した。
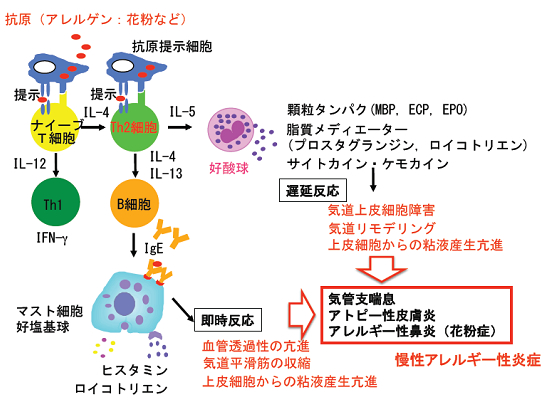
図2 アレルギー炎症の発症メカニズムの概要
ナイーブCD4 T細胞は、IL-4の存在下で抗原提示細胞によって活性化されるとTh2細胞へと分化する。Th2細胞が炎症局所へ移動し再度抗原提示を受けると、IL-4、IL-5、IL-13などのTh2サイトカインを大量に分泌する。IL-4とIL-13はB細胞に働きかけ、IgE抗体の分泌を促進する。抗原と結合したIgE抗体を、マスト細胞や好塩基球が捕捉すると、ヒスタミンやロイコトリエンなどを分泌し、即時反応が起こる。一方、IL-5は好酸球に働きかけ、顆粒タンパク、脂質メディエーター、サイトカイン、ケモカインなどを分泌させる。これらは遅延反応を引き起こす。これらが複合することで気管支喘息、アトピー性皮膚炎、花粉症などの慢性アレルギー性炎症が発症する。
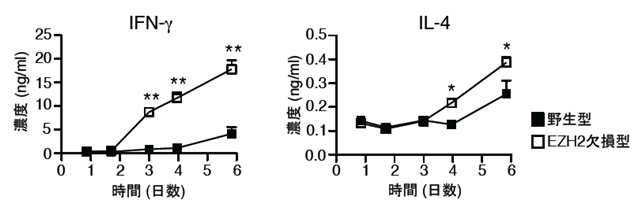
図3 EZH2欠損マウス由来のTh細胞はIFNγとIL-4の過剰な産生が見られる
野生型(黒)とEZH2欠損型(白)マウス由来のTh細胞から分泌されるサイトカイン(左:IFNγ、右:IL-4)を測定した結果を示す。
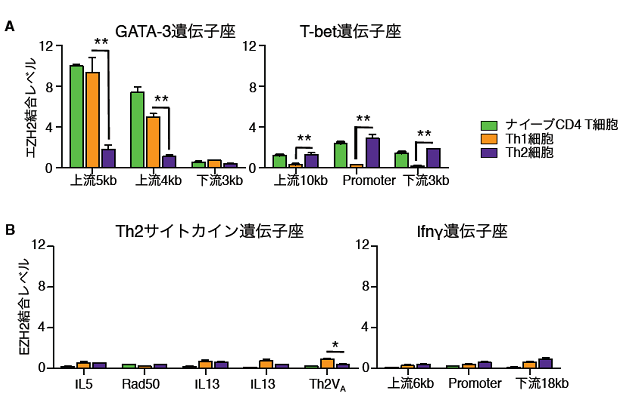
図4 サイトカインを上流で制御する転写因子をコードする遺伝子座において、EZH2の強い結合が見られる
A:転写因子をコードする遺伝子座ではEZH2の結合レベルが高い。
B:サイトカインをコードする遺伝子座ではEZH2の結合レベルが低い。
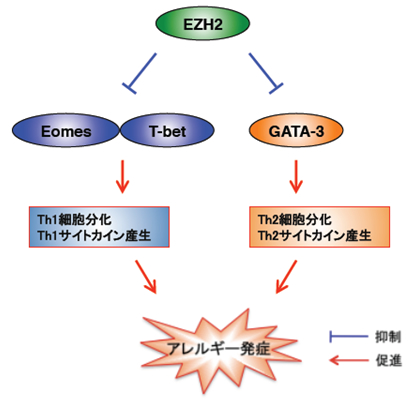
図5 本研究で明らかとなった免疫系のブレーキ機構
EZH2は、Th1サイトカイン、Th2サイトカインをそれぞれ上流で制御する転写因子(T-bet、EomesとGATA-3)の発現のブレーキ役となる。今回の研究で、EZH2が適切に働くことで過剰な免疫反応が抑制されることが分かった。EZH2はアレルギー発症の最上流に位置することから、今回の研究は免疫反応や炎症反応の発症メカニズムの基本原理の一端を解明できたといえる。
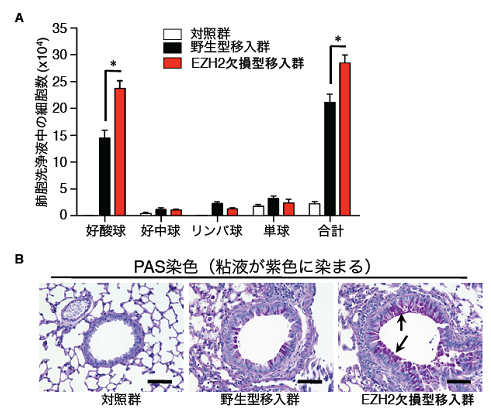
図6 EZH2欠損マウスではアレルギー性気道炎症モデルの病態が増悪する
- A:EZH2欠損型Th2細胞を移入した群では、肺胞洗浄液中の好酸球数が上昇する。
- B:EZH2欠損型Th2細胞を移入した群では、アレルギー炎症で誘導される気管支からの粘液産生(矢印で示す濃い紫部分)が亢進する。
<用語解説>
- 注1)遺伝子地図
- 21世紀初頭にヒトやマウスのゲノムが解読されて、染色体のどの場所にそれぞれの遺伝子が存在するかが明らかとなった。これがゲノムの“白地図”である。近年登場した高速シークエンサーの技術により、この白地図上にたんぱく質の結合レベルの情報をプロットできるようになった。これは例えば日本地図上に降水量をプロットする気象情報のようなものである。降水量の載った日本地図を見れば一目でどの都市で雨が降っているかが分かるように、EZH2結合の遺伝子地図を見れば一目でどの遺伝子にEZH2が結合しているかが分かる。
- 注2)ヘルパーT(Th)細胞
- 白血球の1種でB細胞とともにリンパ球に分類される。T細胞はさらにキラーT細胞とヘルパーT細胞に分類され、前者はがん細胞やウイルスに感染した細胞などを攻撃し排除する。後者はサイトカインと呼ばれる液性因子を分泌し、B細胞やキラーT細胞の働きを助ける役割を担う。
- 注3)サイトカイン
- 細胞が分泌する液性因子であり、細胞間の情報伝達を仲介する。なかでもインターロイキン(IL)と呼ばれる一連のグループは主に免疫系の細胞から分泌され、免疫系が正常に働くために重要である。
- 注4)ポリコーム群たんぱく質
- DNAに結合する抑制性のたんぱく質である。ポリコーム群たんぱく質が結合したDNA領域の周辺の遺伝子は発現しにくくなる。つまり、ポリコーム群たんぱく質は抑制すべき遺伝子の周辺に結合してその機能を発揮するのである。
- 注5)ChIP-seq法
- たんぱく質結合の遺伝子地図を作成する手法のことである。具体的には、たんぱく質とDNAを結合させたまま回収し、その後調べたいたんぱく質と結合しているDNAだけを選択的に抽出し、高速シークエンサーで解析して遺伝子地図を作成する。
- 注6)転写因子
- DNAに結合して、その周辺の遺伝子の発現ON/OFFを調節するスイッチ機能を持つたんぱく質。ヒトやマウスで数百種類存在する。
<論文タイトル>
“The polycomb protein Ezh2 regulates differentiation and plasticity of CD4+ T helper type-1 and type-2 cells”
(ポリコーム群たんぱく質EZH2はCD4陽性T細胞タイプ1およびタイプ2の分化と可塑性を制御する)
doi: 10.1016/j.immuni.2013.09.012
<お問い合わせ先>
<研究に関すること>
中山 俊憲(ナカヤマ トシノリ)
千葉大学 大学院医学研究院 免疫発生学(H3) 教授
〒263-8522 千葉県千葉市中央区亥鼻1-8-1
Tel:043-226-2185 Fax:043-227-1498
E-mail:
<JSTの事業に関すること>
川口 貴史(カワグチ タカフミ)
科学技術振興機構 戦略研究推進部 ライフイノベーショングループ
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail: