ポイント
- 2011年にマウスでは2つのリプログラミング注1)因子と1つの軟骨因子を用いて、皮膚細胞から軟骨様細胞にすることを報告した。
- 今回の研究ではマウスと同じ因子を用いて、ヒト皮膚線維芽細胞から軟骨細胞様細胞にすることができた。
王谷 英達(大阪大学 医学系研究科/前 京都大学 CiRA)、妻木 範行 教授(京都大学 CiRA/JST CREST注2)らの研究グループは、ヒトの皮膚線維芽細胞注3)からiPS細胞を経ずに軟骨細胞様細胞(induced chondrogenic cell:iChon cell)へと直接変換すること(ダイレクト・リプログラミング)に成功しました。
関節軟骨は骨の端を覆い、滑らかな関節運動を行うにあたって重要な役割を果たしています。軟骨は修復能力が乏しく、損傷を放置すると広い範囲で線維化注4)などの変性が生じ、関節機能への障害や痛みを引き起こします。治療法の1つとして、細胞移植が試みられていますが、高品質な軟骨細胞を充分量用意することが困難で、どうしても修復された組織には線維性組織が含まれてしまいます。そこで、高品質な軟骨細胞の供給源を開発することを目標に、妻木教授らのグループでは皮膚の線維芽細胞を軟骨細胞へと直接変換することを試みています。
これまでに妻木教授らのグループではマウス皮膚線維芽細胞に2つのリプログラミング因子(c-MYC、KLF4)と1つの軟骨因子(SOX9)を導入することで、iPS細胞の状態を経ることなく、軟骨細胞様細胞へとダイレクト・リプログラミングできることを報告しています。今回は、ヒト皮膚線維芽細胞を用いて同じ3つの因子(c-MYC、KLF4、SOX9)を導入することにより、軟骨細胞様細胞(iChon cell)を直接誘導できることを明らかにしました。iChon細胞は軟骨細胞の遺伝子パターンを示しており、線維芽細胞特有の遺伝子パターンは消去されていました。また、iChon細胞を免疫不全マウスに移植すると、軟骨組織を作り、奇形腫注5)などの腫瘍はできませんでした。
本研究により、ヒトの細胞においても線維芽細胞を軟骨細胞へと直接変換しうることが示されました。変換の際に腫瘍形成に大きな影響を与えるとされるc-MYCの遺伝子を導入していることなどから、ヒトでの治療に応用するためにはさらなる改善が必要ですが、細胞を直接変換する方法は軟骨再生において軟骨細胞を供給する手段の1つとなることが期待できます。本研究成果は2013年10月16日(米国東部時間)に米国科学誌「PLOS ONE」のオンライン版に掲載されます。
<研究の背景>
関節軟骨は軟骨細胞と細胞外物質のⅡ型・Ⅸ型・Ⅺ型コラーゲンおよびプロテオグリカンにより作られ、関節の滑らかな動きとショックを和らげる役割を果たしています。軟骨は再生能力が低く、ケガや加齢などの原因により失われてゆきます。
通常関節軟骨は硝子軟骨により構成されていますが、損傷すると一部が線維軟骨に置き換わります。線維軟骨はⅠ型コラーゲンを作り、軟骨特有の細胞外物質構造が失われてしまいます。そのため、軟骨の機能を取り戻すためには、線維軟骨を含まない高純度の硝子軟骨を用意し、軟骨が失われた部分に移植するか、線維軟骨をその場で硝子軟骨に変える必要があります。
軟骨を作製する方法の1つとして、iPS細胞から誘導する方法が考えられます。また、もしiPS細胞を経ないで、線維芽細胞から直接軟骨細胞へと変換することができれば、iPS細胞を使う方法よりも短期間で軟骨細胞が得られると考えられます。2011年、妻木教授らのグループはマウスにおいて線維芽細胞から軟骨細胞へとダイレクト・リプログラミングすることに成功したと報告していました。
<研究結果>
1) ヒト皮膚線維芽細胞からiChon細胞へのダイレクト・リプログラミング
ヒト皮膚の線維芽細胞にレトロウイルスを使ってc-MYC、KLF4、SOX9の因子を導入すると、14日後には軟骨細胞に特徴的な細胞の塊が生じました。この塊は軟骨を青く染めるアルシアンブルーで染色されました(図1)。このことからヒトの線維芽細胞がiChon細胞へと分化していることがわかりました。
2) 作製したiChon細胞の性質
ヒト線維芽細胞から作製したiChon細胞では、線維化した細胞で多く発現しているⅠ型コラーゲンは検出されず、軟骨細胞に特徴的なⅡ型コラーゲンやACANという遺伝子の発現が検出されました。これらの遺伝子発現のパターンからもiChon細胞が軟骨細胞に近いことがわかりました。(図2)
3) iChon細胞は生体内で硝子軟骨を作る
ヒトiChon細胞が硝子軟骨を作る能力を確かめるために、免疫不全マウスにiChon細胞を移植したところ、42ヶ所に移植したうち14ヶ所で硝子軟骨様組織の形成が確認できました。硝子軟骨が形成されている部分の組織観察を行うと、硝子軟骨様の部分は硝子軟骨に特有のⅡ型コラーゲンは見られるものの、Ⅰ型コラーゲンは見られず(図3)、iChon細胞から形成された組織は硝子軟骨であることが確認されました。iChon細胞の移植後最長3ヶ月間観察しましたが、腫瘍化は見られませんでした。
<まとめ>
本研究により、ヒトの細胞においても線維芽細胞を軟骨細胞へとダイレクト・リプログラミングしうることが示されました。これにより短期間で目的の硝子軟骨を作ることができ、軟骨再生医療において新たな軟骨細胞の供給源になると考えられます。今回用いた方法では、腫瘍化に大きな影響を与えるとされるc-MYCを使用しており、またレトロウイルスを用いて遺伝子導入をしています。ヒトの治療に応用するためには、これらの課題を克服する必要があります。
軟骨の再生という点では、CiRAが現在進めているiPS細胞ストックを利用して軟骨細胞を作製することも可能です。iPS細胞ストックを利用する場合、自家移植ではなく同種移植(他家移植)であるため、拒絶反応などのリスクを検討する必要はありますが、コスト面でのメリットが大きくなります。ダイレクト・リプログラミングは線維化した軟骨を生体内で局所的にリプログラミングすることに応用が開けます。そのためには今後、遺伝子導入を伴わない化合物などを用いて、軟骨組織周辺で局所的にリプログラミングを誘導する技術を開発する必要があります。iPS細胞ストックを用いる方法と、今回のダイレクト・リプログラミングの手法を上手く使い分ける必要があります。
今回見いだした手法が、軟骨再生において高純度の軟骨細胞を供給する手段の1つとなること、また軟骨に関連する疾患の病態解明に貢献することが期待されます。
<論文名、著者およびその所属>
○論文名
“Direct induction of chondrogenic cells from human dermal fibroblast culture by defined factors”
doi: 10.1371/journal.pone.0077365
○ジャーナル名
PLOS ONE
○著者
Hidetatsu Outani1,2 , Minoru Okada1 , Akihiro Yamashita1, Kanako Nakagawa2,3, Hideki Yoshikawa2, and Noriyuki Tsumaki1,2,3*
*)責任著者
○著者の所属機関
1)京都大学 iPS細胞研究所(CiRA)
2)大阪大学 大学院医学系研究科
3)科学技術振興機構(JST) CREST
<本研究への支援>
本研究は、下記機関より資金的支援を受けて実施されました。
● JST CREST
● 文部科学省科学研究費補助金(基盤研究B)
● 文部科学省科学研究費補助金(萌芽研究)
<参考図>

図1 ヒト線維芽細胞からできた細胞の塊
右側はアルシアンブルーで青色に染めている。図中のバーは500μmを示す。
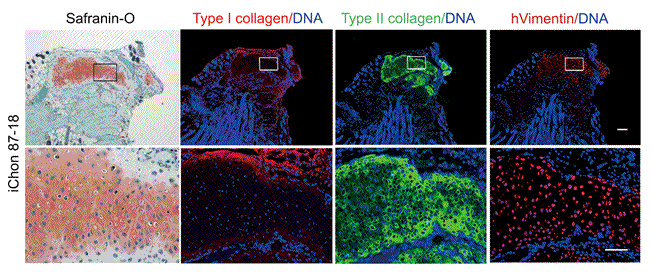
図3 マウスに移植したiChon細胞から作られた硝子軟骨様組織
図中のバーは500μmを示す。
Safranin-O:軟骨を染める染料 (図中のオレンジ色の部分。紫色は核を示している)
Vimentin:細胞骨格タンパク質 (移植したiChon細胞が軟骨として生着していることを確認している)
<用語解説>
- 注1) リプログラミング(=初期化)
- 分化した体細胞の核がリセットされ受精卵のような発生初期の細胞核の状態に戻り、多能性幹細胞などに変化すること。リプログラミングを引き起こす因子をリプログラミング因子と表現することもある。
- 注2) JST戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域
| 「人工多能性幹細胞(iPS細胞)作製・制御等の医療基盤技術」
(研究総括:須田 年生 慶應義塾大学 医学部 教授) |
| 研究課題名
| 「組織幹細胞/前駆細胞を誘導するディレクテッドリプログラミング技術の開発」 |
| 代表研究者
| 妻木 範行(京都大学 iPS細胞研究所 教授) |
| 研究期間
| 平成21年10月~27年3月 |
- 注3) 線維芽細胞
- 結合組織を構成する最も主要な細胞。多くの臓器に存在する。何らかの損傷により組織に傷が生じると、この細胞が増殖し修復する。
- 注4) 線維化
- 軟骨の場合、Ⅰ型コラーゲンを主体とする細胞外基質を作り、組織本来の構造・機能が損なわれる。損傷から治癒する過程の組織(瘢痕組織)形成と関連する。
- 注5) 奇形腫(テラトーマ)
- ES細胞やiPS細胞を免疫不全マウスの皮下などに注射すると、腫瘍を形成する。この腫瘍はテラトーマと呼ばれ、様々な種類の組織が混在している。テラトーマを観察し、様々な組織に分化していることを確認することは、細胞の分化多能性を調べる一般的な方法の1つである。
- 注6) HFC(human fetal chondrocytes):ヒト培養軟骨細胞
- ヒトの軟骨細胞から取り出した細胞を培養したもの。本実験ではポジティブ・コントロール(実験が正しくできているかどうかを確認する標準)として利用している。培養するとどうしても一部が線維化してしまうため、Ⅰ型コラーゲンが検出されてしまう。
<お問い合わせ先>
<研究に関すること>
京都大学 iPS細胞研究所(CiRA)
研究支援部門 国際広報室
和田濵・遠山
TEL:075-366-7005 FAX:075-366-7023
E-mail:
<JSTの事業に関すること>
科学技術振興機構 戦略研究推進部
TEL:03-3512-3525 FAX:03-3222-2063