大阪大学 大学院生命機能研究科/医学系研究科の吉森 保 教授と前島 郁子 CREST研究員らの研究グループは、同医学系研究科の猪阪 善隆 准教授らとともにオートファジー注1)により、損傷を受けたリソソーム注2)が除去・修復されることを明らかにしました。細胞の胃腸に当たる細胞内小器官リソソームは、様々な要因で穴が開くことがあります。穴が開くと内部の消化酵素や活性酸素が流出し、細胞にとって有害な存在となります。本研究グループは、この損傷リソソームを、細胞内の老廃物などを清掃するシステムであるオートファジーが感知し効率よく除去していることを発見しました。損傷を受けていない正常なリソソームを除去することはありません。細胞あたりのリソソーム数は損傷のあるなしに関わらず常に一定で、損傷リソソームが除去されないと新しいリソソームが形成されず細胞の消化能力が低下してしまいます。さらにマウスを用いた実験から、高尿酸血症で起こる腎症が、尿酸結晶で損傷したリソソームのオートファジーによる除去ができないと悪化することを見いだしました。2型糖尿病、動脈硬化、痛風などの生活習慣病の発症因子にはリソソームに損傷を与えるものがあり、これらの疾患でオートファジーの低下が起こることが最近明らかになってきていることから、オートファジーを標的とした新規治療法の開発が期待されます。
本研究成果は、文部科学省 科学研究費補助 金新学術領域研究「細胞内ロジスティクス:病態の理解に向けた細胞内物流システムの融合研究」と、科学技術振興機構(JST) CREST研究領域「生体恒常性維持・変容・破綻機構のネットワーク的理解に基づく最適医療実現のための技術創出」(研究総括:永井 良三)における研究課題「恒常性維持機構オートファジーに着目した栄養素過剰摂取に起因する疾患の原因解明と治療法確立」(研究代表者:吉森 保)の一環で行われました。
なお、本成果は平成25年8月6日(英国時間)に欧州科学雑誌「The EMBO Journal」のオンライン速報版で公開されます。
<研究の背景>
リソソームは生体内においてシリカや尿酸結晶などの結晶物、細菌毒素、脂質や薬剤などで損傷されることが報告されています。損傷リソソームが有害であることも言われていましたが、細胞がそれにどのように対処しているかは、わかっていませんでした。一方、オートファジーは近年急速に理解が進んできた細胞内の浄化システムで、オートファゴソームという膜構造で老廃物や病原体を包み込み隔離することができます。本研究グループは、このオートファジーが損傷リソソーム除去に働いているのではないかと考え研究を開始し、以下の結果を得ました。
まず損傷したリソソームがオートファジーの標的になるかを、培養哺乳類細胞を用いて検討しました。その結果、薬剤などで人為的にリソソームを損傷すると、損傷リソソームがオートファゴソームに包み込まれることを見いだしました。短時間の薬剤処理により一時的に損傷リソソームを発生させると、通常の細胞では経時的に損傷リソソームが減少し正常なリソソーム数が増加したのに対し、オートファジー欠損細胞では損傷リソソームの減少はほとんど見られませんでした。さらに、オートファジー欠損細胞では損傷リソソームが減少しないにも関わらず細胞全体のリソソーム数に変化はありませんでした。これらの結果より、損傷リソソームがオートファジーによって選択的に隔離されることで、新しいリソソームが形成されリソソームの機能が回復していることが明らかとなりました(図1)。
次に損傷リソソーム除去の生理的な意義を検討するために、本研究では急性高尿酸血性腎症に着目しマウス個体を用いて解析を行いました。急性高尿酸血性腎症は、血中の尿酸値の上昇により起こる腎障害で、リソソームを損傷する尿酸結晶の形成を伴います。マウスに尿酸を投与し高尿酸血症を誘発させると、腎臓の細胞のリソソームが損傷し、オートファゴソームによって隔離されている様子が多数観察されました。一方、オートファジーに必須の遺伝子を腎臓細胞特異的に破壊したマウスではリソソームの損傷は見られたものの、損傷リソソーム周囲でのオートファゴソーム形成は認められませんでした(図2)。尿酸を投与した腎臓細胞特異的オートファジー遺伝子破壊マウスでは腎組織傷害の重篤化と腎機能の低下が見られたことから、オートファジーは尿酸結晶により損傷したリソソームを隔離することで、高尿酸血性腎症の病態悪化を防ぐのに貢献していると考えられます。
<本研究成果が社会に与える影響>
損傷を受けたリソソームを、細胞が排除するためにオートファジーを用いていることがわかりました。また損傷リソソーム除去がリソソームの新生に必要であることや、高尿酸血症性腎炎の悪化を防いでいることも明らかになり、その生理的な重要性が示されました。尿酸は痛風の原因にもなりますが、2型糖尿病を起こすヒトIAPP、動脈硬化を起こすコレステロール結晶などもリソソームに穴をあけることが知られています。これらの生活習慣病の発症抑制にオートファジーが関与するという報告があり、それは損傷リソソーム除去による可能性があります。他方これらの疾患の患者さんのオートファジー能力が低下していることが徐々に明らかになりつつあるので、オートファジーを人為的に活性化することで現代社会の大きな課題である生活習慣病の予防治療が可能になるかもしれません。
<参考図>
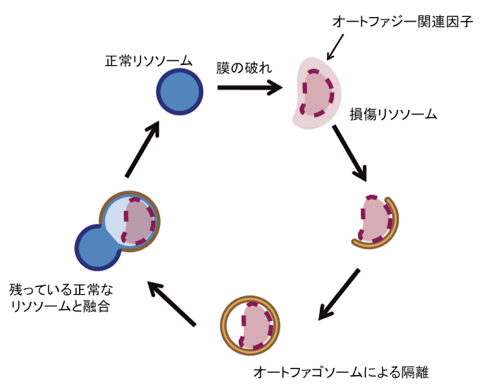
図1 オートファジーによるリソソームの品質管理
リソソームの膜が破れると、オートファゴソームがそれを隔離します。その後、正常なリソソームがそれに融合し、修復が行われます。その結果リソソーム数が減少するので、新しいリソソームも作られます。
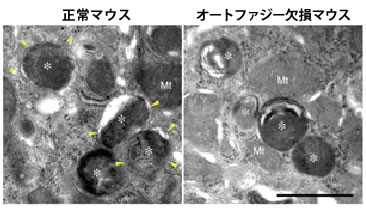
図2 オートファゴソームによって隔離される損傷リソソーム
尿酸投与した正常マウスの腎臓(尿細管)細胞内では、1重膜のリソソームが2重膜のオートファゴソームによって隔離されている様子が多数観察された。黄色矢頭:オートファゴソーム、アスタリスク:リソソーム、Mt:ミトコンドリア
<用語解説>
- 注1)オートファジー
- 細胞内部を「清掃」する仕組み。オートファゴソームと呼ばれる直径1μmの小さな膜構造が多数細胞内に形成され、それがロボット掃除機のように細胞内の老廃物や有害物を取り込み(実際には膜が伸びて包み込む)、分解する。飢餓状態になったときに、細胞成分を分解して栄養源にすることもできる。近年オートファジーが、がん、神経変性疾患(アルツハイマー病やパーキンソン病)、心不全、腎不全、炎症性疾患、感染症、生活習慣病(2型糖尿病、動脈硬化、痛風など)など多岐に亘る重要疾患の抑制に働いていることが明らかになり大変注目されている。オートファジー研究は日本が世界をリードしている。
- 注2)リソソーム
- 細胞内外の物質を取り込んで分解する細胞の胃腸にあたる細胞内小器官(細胞の器官のこと)。多種の消化酵素を内蔵している。オートファジーにおける分解も、オートファゴソームとリソソームが融合することで起こる。しかし、今回そのリソソームが損傷するとそれ自体がオートファジーの対象になることがわかった。
<お問い合わせ先>
<研究内容に関すること>
吉森 保(ヨシモリ タモツ)
大阪大学 大学院生命機能研究科/医学系研究科 教授
Tel:06-6879-3580 Fax:06-6879-3589
E-mail:
<JSTの事業に関すること>
川口 貴史(カワグチ タカフミ)
科学技術振興機構 戦略研究推進部
Tel:03-3512-3524 Fax:03-3222-2064
E-mail: