ポイント
- マウスのES細胞を用いて、生殖細胞を直接誘導する遺伝子(転写因子)を発見
- サイトカインを用いた従来の方法よりも、高効率、短時間で誘導可能
- 誘導された生殖細胞は精子に分化し、体外受精により健常なマウスを得ることに成功
- 生殖細胞形成過程のメカニズム解明に大きく前進
京都大学 大学院医学研究科の斎藤 通紀 教授(兼 JST ERATO研究総括、京都大学 物質-細胞統合システム拠点(iCeMS=アイセムス) 主任研究者、京都大学 iPS細胞研究所 研究員)と同研究科の中木 文雄さん(博士課程学生)らの研究グループは、多能性幹細胞であるマウスES細胞注1)から、3種類の遺伝子(転写因子注2))を用いて始原生殖細胞注3)を誘導する培養系を開発しました。また、この培養系で得られた始原生殖細胞から精子を作製し、子供を産み出すことにも成功しました。
これまで本研究チームは、マウスES細胞やマウスiPS細胞注4)から始原生殖細胞をサイトカイン注5)により誘導し、さらに精子、卵子を作製することに成功していましたが、精子、卵子の元となる始原生殖細胞を直接誘導する遺伝子は特定されていませんでした。
本研究グループは今回、ES細胞を分化させたエピブラスト様細胞(EpiLCs注6))に、Blimp1注7)、Prdm14注8)、Tfap2c注9)の3種類の遺伝子(転写因子)を発現させることにより、始原生殖細胞様の細胞を得ることに成功しました。この細胞を不妊の雄マウスの精巣に移植したところ、正常な精子形成が確認されました。さらに、この精子を正常な卵子と体外受精させたところ、健常なマウスが得られました。これらのマウスは正常に成長し、子供を作る能力があることも分かりました。
この研究により、生殖細胞の形成過程の解明に向けて大きく前進することが期待されます。また、この成果は世界で初めて生殖細胞が特定の遺伝子で誘導されうることを示したものであり、マウスのみならず、ヒトを始めとしたほかの動物種でも同様のアプローチがなされうるものと期待されます。
本研究成果は、JST 戦略的創造研究推進事業 ERATOの一環として行われ、2013年8月4日18時(ロンドン時間)に英国科学誌「Nature」のオンライン速報版で公開されます。
本成果は、以下の事業・研究プロジェクトによって得られました。
戦略的創造研究推進事業 ERATO型研究
| 研究プロジェクト |
「斎藤全能性エピゲノムプロジェクト」 |
| 研究総括 |
斎藤 通紀(京都大学 大学院医学研究科 教授) |
| 研究期間 |
平成23年度~平成28年度 |
<研究の背景と経緯>
卵子や精子を生み出す生殖細胞系列は、生体内の細胞系譜の中で唯一次世代に遺伝情報を伝達できる細胞系列であり、その発生異常は不妊や次世代の個体の疾患に深く関わることが知られています。全ての卵子や精子の起源となる細胞は始原生殖細胞と呼ばれ、個体の発生過程の比較的早い段階で分化します。始原生殖細胞は様々な発生過程を経て、雌では卵子に雄では精子に分化しますが、その発生過程の多くが胎仔期に行われていることもあり、解明されていない部分が多く残されています。
胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)といった多能性幹細胞は、体を構成するいずれの細胞にも分化する能力を持っており、生殖細胞にも分化することができます。多能性幹細胞を任意の細胞に分化させる培養技術を開発することにより、細胞の発生過程を体外培養で再現することが可能となります。これによって体内では解析困難であった現象を詳細に研究することが可能となるため、発生・細胞・幹細胞生物学分野の研究を大きく前進させるとともに、再生医学などの応用分野にも大きく貢献することとなります。
昨年までに、本研究グループはマウスのES細胞やiPS細胞から始原生殖細胞(Primordial germ cells:PGCs)に類似した始原生殖細胞様細胞(Primordial germ cell like-cells:PGCLCs注10))を試験管内で分化させて、それらを元に健常な精子、卵子と子孫を得ることに成功しました(Cell ,2011;Science ,2012)。これにより、体外で作製したPGCLCsは機能的な精子・卵子まで分化する能力があることが明らかとなりましたが、これらの分化を制御するのに十分な遺伝子群は不明でした。本研究グループでは、これらの精子・卵子を作製する際に用いたPGCLCsの培養技術を利用して、生殖細胞の運命決定を制御する遺伝子群を特定する研究を進めてきました。
<研究の内容>
本研究では、マウスES細胞を起点として、遺伝子を人為的に発現させることにより、PGC様の細胞を誘導し、生殖細胞の運命決定を行うのに十分な遺伝子群を特定することを目的として実験を行いました。
実験の概要は以下の通りです(図1)。まず、始原生殖細胞が誘導されたときに蛍光タンパク質を発現する(レポーター遺伝子を持つ)とともに、目的の外来遺伝子を任意のタイミングで人為的に発現させることが可能なES細胞を樹立しました。このうち雄の細胞を用いて実験を行いました。
(詳細は以下の通りです。このES細胞は、始原生殖細胞に発現する遺伝子Blimp1と始原生殖細胞や卵子に発現する遺伝子stella注11)が発現している場合に、蛍光タンパク質が発現するように遺伝子(レポーター遺伝子)を改変したマウスから樹立しました。これは先行研究でも用いられていたものです。これにより、始原生殖細胞に分化した細胞は蛍光タンパク質によって光を発するため、蛍光顕微鏡下で容易に観察できます。また、人為的な遺伝子発現は、テトラサイクリン誘導システムを用いて行いました。このシステムは、テトラサイクリン系抗菌薬を培地に添加することにより、導入した目的の外来遺伝子を任意のタイミングで人為的に発現させることが可能なシステムです。今回用いたES細胞は、これらレポーター遺伝子とテトラサイクリン誘導システムの両方を備えたものです。)
先行研究同様、ES細胞をエピブラスト様細胞(Epiblast-like cells;EpiLCs)に分化させ、細胞を2,000細胞程度で凝集させました。そして、生殖細胞の運命決定に十分な遺伝子群を特定するために、培地にドキシサイクリン(テトラサイクリン系抗菌薬の一種)を加え、Blimp1、Prdm14、Tfap2cという3種類の遺伝子を発現させました。その結果、レポーター遺伝子が陽性となりました(図2)。陽性率はBMP4などのサイトカインを利用した従来の方法による誘導効率(約40%)よりも高く、約80%に達し、また48時間以内に両方のレポーター遺伝子が陽性となり、誘導に要する時間も半分程度に短縮されました。今回は直接転写因子群を発現させたため、高効率、短時間で誘導が成功したと考えられます。
これらのレポーター陽性細胞を、不妊の新生児マウスの精巣に注入すると、10週間後に精子形成が観察されました。回収した精子を正常な卵子と体外受精させたところ、健常なマウスが誕生しました。これらのマウスには導入した外来遺伝子が組み込まれていました。これらのマウスは正常に成長し、雌雄ともに子供を作る能力があることも確認されました(図3)。今回、遺伝子により誘導したPGC様の細胞を、TF-PGCLCs(Transcription factor-induced primordial germ cell-like cells)と命名しました。
TF-PGCLCsの遺伝子発現全体を調べるために、DNAマイクロアレイ注12)解析を行いました。得られた遺伝子発現情報について主成分分析を行った結果、従来のサイトカインを用いた方法で誘導した場合は一時的に体細胞への分化プロセスを経てPGCLCsへと分化するのに対し、転写因子を用いて誘導した場合は、体細胞への分化プロセスを経ることなく速やかにPGCLCsへと分化することが分かりました。なお、ES細胞に直接遺伝子を発現させた場合は、PGCLCsが得られませんでした(図4)。
また、これら3種類の遺伝子を、それぞれ1種類ずつ人為的に発現させることによって、各遺伝子が果たしている役割について検討しました。遺伝子発現情報を比較した結果、特にPrdm14遺伝子が、生殖細胞プログラムの誘導において中心的な役割を果たしていることが明らかとなりました。
なお、今回は多能性幹細胞としてES細胞を用いて実験を行いました。iPS細胞を用いた実験は行っていませんが、同様の方法でPGCLCsを誘導可能であると考えられます。
<今後の展開>
本成果は、生殖細胞発生過程のメカニズム解明に向け、大きな前進といえるものです。生殖細胞はその数の少なさから、発生過程のメカニズムには不明な点が多く残されていました。以前の研究により、体外培養系を用いてPGCLCsを多数得ることが可能となっていました。今回はさらに、PGCLCsの誘導に中心的に機能する遺伝子を絞り込むことに成功しました。これによって、生殖細胞の発生がどのように進んでいくのか、これらの遺伝子を中心に解析することが可能になります。実際、今回絞り込んだ遺伝子は、生体において生殖細胞の運命決定においてごく初期に発現しています。この培養系は、生体内で起こる現象を体外で再現する上で基盤となるものです。
また、本成果は、哺乳類の生殖細胞が特定の遺伝子によって誘導可能であることを世界で初めて示すものです。iPS細胞や、心筋細胞や神経細胞などの体細胞は、特定の遺伝子によって誘導可能であることが示されてきましたが、機能的な生殖細胞を誘導した例はありませんでした。ほかの細胞種では、動物種の垣根を越えて同一の遺伝子群で誘導が可能な場合があります。今回の結果は、ほかの動物、特にヒトにおいて生殖細胞を人為的に誘導する可能性を広げるものです。ただし、ヒトにおける生殖細胞の研究は、倫理的な課題を慎重に検討した上で実施を判断する必要があります。
<参考図>
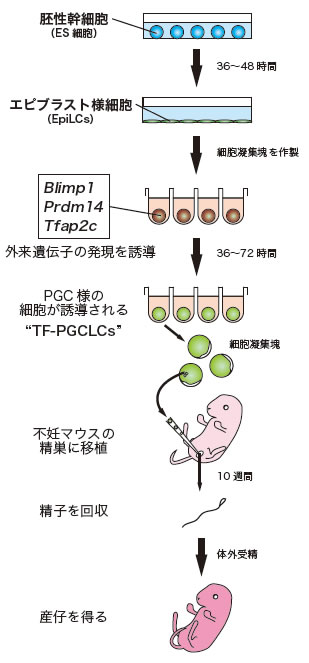
図1 ES細胞から遺伝子を用いて生殖細胞を誘導する際の実験手順
まずES細胞をエピブラスト様細胞(EpiLCs)に分化させる。EpiLCsを回収し、細胞凝集塊を作製して、3遺伝子を人為的に発現させると、約36時間以降に凝集塊中にPGC様の細胞が誘導される(Blimp1およびstella陽性細胞)。これらの細胞を不妊マウスの精巣に移植すると、約10週間で精子形成が認められる。この精子を体外受精させると、仔が得られる。
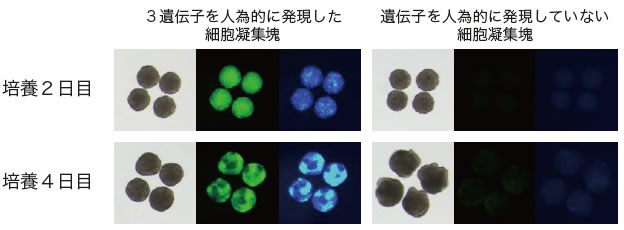
図2 遺伝子を用いて誘導されたPGCLCs(TF-PGCLCs)
EpiLCsを回収し、細胞凝集塊を作製して、3遺伝子を強制発現させたもの。それぞれ、(左)明視野、(中)黄~緑色蛍光タンパク質(Blimp1遺伝子の発現を示す)(右)青色蛍光タンパク質(stella遺伝子の発現を示す)。培養2日目には、凝集塊のほとんどの細胞で緑色、青色蛍光タンパク質が陽性になっている。右側は遺伝子を発現させずに培養したもの。蛍光タンパク質は観察されない。細胞凝集塊の大きさは、直径約0.3~0.5mm。

図3 TF-PGCLCs由来の精子と、体外受精により得られた産仔
(左)図2で示した蛍光タンパク質陽性の細胞を回収し、不妊マウスの精巣に移植し、10週間経過したところで精巣を摘出して観察したところ、精子形成が認められた。写真は得られた精子。(中)得られた精子を正常な卵子と体外受精したところ、産仔を得た。写真はTF-PGCLCs由来の精子から誕生したマウス(出生直後)。(右)TF-PGCLCs由来の精子から誕生したマウスは正常に成長し、雌雄とも子孫を作る能力が確認された。写真は、出産直後の雌マウス(約14週齢)とその仔マウス。
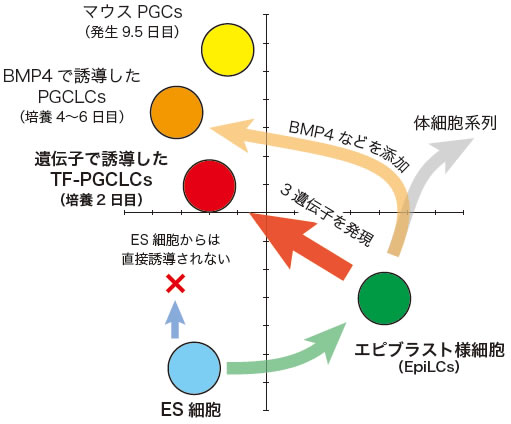
図4 ES細胞、EpiLCs、TF-PGCLCsなどの遺伝子発現情報を比較した主成分分析の概略図
DNAマイクロアレイ解析によって各細胞種の遺伝子発現を網羅的に調べ、その発現情報を主成分分析した結果の概略。左下のES細胞を起点に、まずエピブラスト様細胞(EpiLCs)へと分化させた後、3遺伝子を発現させると、培養2日目にPGCLCsが誘導される。BMP4などのサイトカインを用いて誘導した場合は、体細胞系列に一度近づいた後、培養4~6日目にPGCLCsが誘導される。これらの遺伝子発現の状態は、発生9.5日目のPGCsに近い。なお、ES細胞に直接3遺伝子を発現させても、PGCLCsは得られなかった。
<用語解説>
- 注1)ES細胞
- 胚性幹細胞(Embyronic Stem Cells)のこと。マウスの場合は受精後3~4日目の胚盤胞の内部細胞塊から、培養により得られる。体外培養により無限に増殖し、生殖細胞を含むほぼ全ての組織の細胞に分化することができる。
- 注2) 転写因子
- DNAからメッセンジャーRNAへの転写を制御するタンパク質。遺伝子が機能するには、DNAの情報がまずメッセンジャーRNAへと転写され、その後タンパク質へと翻訳される必要がある。このうち転写を制御するのが転写因子であり、生物の発生過程では様々な転写因子によってゲノムのどの情報を利用するかが規定され、様々な細胞が生み出される。細胞内では多数の転写因子が機能しているが、細胞の種類に応じて、特徴的な転写因子は異なる。なお、特徴的な転写因子を人為的に発現させることにより、細胞の状態を変化させることが実験で示されている。例えばiPS細胞(注4参照)を樹立する際に用いられる遺伝子も、転写因子に含まれる。
- 注3) 始原生殖細胞
- 全ての卵子もしくは精子の源となる細胞。発生の初期、マウスの場合は胚齢6.5日前後に分化する。発生初期は少数の細胞集団であり、その発生様式に性差はないが、胚齢12日目前後に体細胞の性によって、卵子もしくは精子へと分化することが決定される。
- 注4) iPS細胞
- 人工多能性幹細胞(induced Pluripotent Stem Cells)のこと。皮膚などの体細胞に特定の因子を導入することにより作製される。ES細胞(注1参照)のように、無限に増殖し、生殖細胞を含むほぼ全ての組織に分化することができる。ES細胞と異なり、あらゆる個体の体細胞から作製が可能であり、自家移植により免疫拒絶を起こさない細胞である。
- 注5) サイトカイン
- 細胞間で情報を伝達する因子。多くの種類があり、細胞の分化、形態変化、遊走、成長、増殖などに大きな影響を与える。先行研究で、BMP4というサイトカインを用いることで、PGC様の細胞が誘導されることが示されていた。
- 注6) EpiLCs
- エピブラスト様細胞(Epiblast-like Cells)のこと。ES細胞やiPS細胞から特定の培養条件で分化させた細胞。エピブラスト(生体内で始原生殖細胞へと分化する組織)によく似た特徴を持つ。体外培養系において、PGCLCs(注10参照)へと分化する能力があることが知られていた。
- 注7) Blimp1
- 始原生殖細胞の発生に重要なはたらきを持つ遺伝子のひとつ。始原生殖細胞の発生の最も初期に発現する。この遺伝子は始原生殖細胞のほかに、免疫細胞などでも重要なはたらきがあることが知られている。
- 注8) Prdm14
- 始原生殖細胞に特異的に発現する遺伝子のひとつ。始原生殖細胞の発生初期に発現し、その発生過程に必須の因子であることが知られている。
- 注9) Tfap2c
- 始原生殖細胞の発生に重要なはたらきを持つ遺伝子のひとつ。始原生殖細胞の発生初期に発現し、その発生過程に必須の因子であることが知られている。この遺伝子は体組織を含む様々な組織の発生過程に関与している。
- 注10) PGCLCs
- 始原生殖細胞様細胞(Primordial Germ Cell-like Cells)のこと。ES細胞やiPS細胞からEpiLCsを経て特定の培養条件で分化させた細胞。始原生殖細胞によく似た特徴を持つ。精子および卵に分化することが知られていた。
- 注11) stella
- 始原生殖細胞と卵子に特異的に発現する遺伝子のひとつ。始原生殖細胞および未成熟卵子から成熟卵子まで多量に発現しており、DNAメチル化制御に関与することが知られている。
- 注12) DNAマイクロアレイ
- プローブと呼ばれるDNA断片を多数固定した小さなチップを用いて、全遺伝子の発現量を調べる技術。
<論文名>
“Induction of mouse germ-cell fate by transcription factors in vitro”
(体外培養系を用いたマウス生殖細胞系列の転写因子による誘導)
doi: 10.1038/nature12417
<お問い合わせ先>
<研究に関すること>
斎藤 通紀(サイトウ ミチノリ)
京都大学 大学院医学研究科 生体構造医学講座 機能微細形態学 教授
〒606-8501 京都府京都市左京区吉田近衛町
Tel:075-753-4335 Fax:075-751-7286
E-mail:
<iCeMSに関すること>
今羽右左 デイヴィッド 甫(コンハウザ デイヴィッド ハジメ)
京都大学 iCeMS 国際企画掛・広報掛 掛長
〒606-8501 京都府京都市左京区吉田牛ノ宮町 iCeMS本館
Tel:075-753-9755 Fax:075-753-9759
E-mail:
<JSTの事業に関すること>
坂本 祥純(サカモト ヨシズミ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail: