米田 悦啓 医薬基盤研究所 理事長・大阪大学 名誉教授(本研究成果は大阪大学 生命機能研究科 教授、医学系研究科 兼任教授在籍時のものである)、特任研究員・安原 徳子らの阪大のグループと金子 寛生 教授(日本大学 文理学部 物理生命システム科学科)、研究員・山岸 良介の日大のグループは、マウス胚性幹細胞(ES細胞)を用いた解析と計算構造生物学の手法を使い、動物細胞核へのタンパク質輸送を担う輸送受容体importinα2(インポーティンアルファ)注1)が哺乳類のES細胞における未分化性を維持する機構の一端を明らかにしました。
importinαは真核生物の細胞核に、タンパク質を運び入れる輸送因子です。転写因子をはじめ、核で機能する重要なタンパク質の輸送に関わります。これまでに、importinαの1つであるimportinα2は、未分化なES細胞で高く発現すること、さらに初期化に必要なOct3/4タンパク質などの核局在化シグナル(NLS)注2)に結合し、その核内への輸送に働くことが知られていました。
本研究ではこのimportinα2に、既知のものとは異なる新たな核局在化シグナル認識部位があることを発見し、こちらの部位では分化を促進する特定の転写因子(Oct6など)と結合しその輸送を選択的に阻害することを発見しました。つまり、importinα2は複数の基質認識部位を持ち、未分化性を維持する転写因子の輸送を促進するだけでなく、阻害活性により細胞分化を誘導する転写因子の核内輸送を阻害することにより細胞の分化を抑制するという、2つの制御を行うことで未分化性が維持されることを世界で初めて明らかにしました。
本成果はJSTの戦略的創造研究推進事業(CREST)研究領域「人工多能性幹細胞(iPS細胞)作成・制御等の医療基盤技術」(研究総括:須田 年生)研究課題「人工染色体を用いた新たな細胞リプログラミング技術開発」(研究代表:米田 悦啓)の一環で行われた研究成果です。「Developmental Cell」から2013年7月29日(米国東部時間)オンライン速報版に掲載され、出版されます。
<研究の背景と内容>
真核細胞の核は核膜により覆われ、大きな分子の核内外への移行は自由ではありません。タンパク質などの機能性分子の多くは、エネルギーと輸送受容体を必要とする選択的な輸送により核内外へ運ばれます。私どもは、これまでに、核輸送受容体の1つであるimportinα2が未分化な細胞で高く発現し、細胞分化に伴って発現が低くなることを見出すとともに、importinα2の発現はES細胞の未分化性維持に必要であり、その発現低下は分化を誘導することを明らかにしてきました。しかし、importinα2がどのように細胞の未分化性維持に関わるのかは明らかではありませんでした。本研究では、ES細胞を用いた解析から得られた情報を手掛かりに、コンピューターシミュレーションを用いた立体構造予測によって、importinα2に未知の基質認識部位が存在することを発見しました(図1)。
そして、この部位に分化を進めるOct6などの転写因子が結合すると核へと運ばれなくなります(図2および図3)。核へとタンパク質を運ぶ受容体として知られていたimportinα2に、輸送を止めるという全く逆の活性があることは驚くべきことです。
また、野生型のimportinα2を恒常的に発現させたES細胞は、分化させても未分化性を維持することがわかりました。代わりに、Oct6結合部位にアミノ酸置換を加えた変異型importinα2では、分化への影響は見られませんでした。したがって、importinα2の輸送阻害活性により、ES細胞の未分化性が保たれることを明らかにしました。
一方、未分化性維持に働く転写因子であるOct3/4は新たに見つかった基質認識部位ではなく、既知の基質認識部位に結合することで効率よく核へと運ばれます。つまり、importinα2は複数の基質認識部位を持ち、、転写因子の種類によってその部位を使い分けることにより、核へと運ぶか否かを決定し、ES細胞の未分化性を保っていることがわかりました。
<本研究成果が社会に与える影響>
本研究は、従来の発生・分化の研究の対象である転写因子ではなく、それの輸送に関わる核輸送受容体の機能というユニークな切り口から、未知の分化制御系を見出しました。importinαは多様な細胞分化に関わると考えられ、発生・分化研究領域の新たな展開が期待されます。例えば、特定の転写因子の核輸送を制御するという全く新規な方法により、iPS細胞を効率よく作製し、さらにそれを必要な細胞へ効率よく分化させるなど、再生医療分野への応用が考えられます。また、新たに発見したimportinα2の基質結合領域は、わずか1アミノ酸の変異によりその能力を失うことも明らかにしております。このことは、ごく限られた部分の構造に着目するだけで輸送の制御が行える可能性を示唆しており、幹細胞研究に利用可能な低分子化合物の開発につながると期待します。
<参考図>
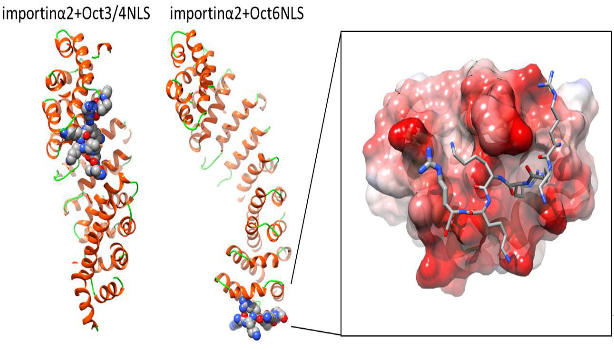
図1 立体構造予測によるimportinα2とNLSの結合モデル
左は、転写因子Oct3/4(ES細胞の未分化に寄与する転写因子。iPS細胞作製時における山中ファクターの1つ。)が、importinα2によって運ばれる時の既知の結合様式を表します。中央は、転写因子Oct6(ES細胞を神経細胞などへ分化させる転写因子)が、importinα2によって運ばれる時の結合様式を表し、今回新規に発見したものです。右は、結合している部分の構造を拡大表示したものです。
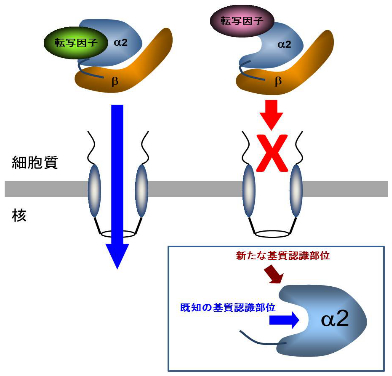
図2 importinα2の基質認識様式と輸送
importinα2は未分化なES細胞に高く発現し、細胞の未分化性を維持する転写因子(Oct3/4など)を効率よく核へと運びます。この場合の結合部位は、importinα2に存在する既知の核局在化シグナル認識部位(図1左の結合様式)です。一方、ES細胞の分化を促進する転写因子(Oct6など)は本研究で見つけた新たな核局在化シグナル認識部位に結合します(図1右側の結合様式)。この状態では転写因子は核へと運ばれず、機能しません。このような核輸送の阻害活性により、importinα2はES細胞の未分化性を保つと考えられます。
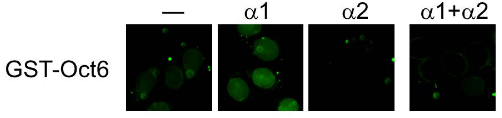
図3 importinα2によるOct6の輸送阻害
動物の培養細胞を用いて、importinα2がOct6の輸送を阻害することを突き止めました。薬剤
処理により細胞膜を透過性にして核だけにした培養細胞に、それぞれの輸送因子とOct6を加えて輸送の様子を観察しました。importinα1はOct6を核に輸送しますが、importinα2は輸送しません。importinα1とimportinα2を同時に加えると、Oct6は核に入らなくなります。つまり、importinα1によるOct6の輸送が、importinα2により阻害されます。
<用語解説>
- 注1) importinα
- 米田教授らの研究グループで1994年から1995年にかけて同定された、ポリオーマウイルス腫瘍抗原を細胞質から核膜を貫通する穴を通して核内に運搬する最初の輸送因子。importinαは基質とimportinβ間のアダプターとして働き、基質/importinα/importinβという3者の複合体を形成して、基質を核内へ輸送する。
- 注2) 核局在化シグナル(nuclear localization signal:NLS)
- 核で機能するタンパク質のほとんどは細胞質で作られ、アミノ酸配列の内部にある核に運ばれる目印となる核局在化シグナル(NLS)を介した輸送により核へ運ばれる。importinαは、このNLSのうち塩基性アミノ酸を多く含む特定の配列を特異的に認識し、結合・輸送することが知られている。
<お問い合わせ先>
<研究に関すること>
安原 徳子(ヤスハラ ノリコ)
大阪大学 大学院生命機能研究科 細胞ネットワーク講座 特任研究員
Tel:06-6879-4606 Fax:06-6879-4609
E-mail:
<JSTの事業に関すること>
川口 貴史(カワグチ タカフミ)
科学技術振興機構 戦略研究推進部
Tel:03-3512-3531 Fax:03-3222-2064
E-mail: