ポイント
- エピジェネティクスは、細胞の多様性を生み出す仕組みとして近年注目されている。
- 従来エピジェネティックな変化は細胞集団で追跡していたが、今回一細胞ごとの比較に成功し、それが規則性を持って特定の遺伝子によって制御されることを発見。
- 本手法で酵母によって得られた知見をヒトに応用することで、関連遺伝子を同定し、将来的にがんをはじめとする後天性疾患の解明に期待。
JST 戦略的創造研究推進事業(さきがけ)の一環として、福井大学 大学院工学研究科の沖 昌也 准教授らは、単一細胞のエピジェネティックな遺伝子の発現状態の変化を可視化・解析する追跡手法を開発し、その変化に規則性と制御法を発見しました。
「エピジェネティクス」とは、DNA塩基配列の変化を伴わずに遺伝子の発現状態が変化する制御機構で、細胞の多様性を生み出す仕組みや後天性疾患の要因を解明するヒントになるものとして近年注目を集めています。
その機構解明には、個々の細胞の挙動を追跡することが必要ですが、従来は細胞集団の平均値でしか発現状態を知ることができませんでした。しかし、細胞は1つ1つ遺伝子の発現状態が異なるため、単一細胞のエピジェネティックな発現状態の変化を知る新たな追跡手法の開発が望まれていました。
今回沖准教授らは、出芽酵母をモデル生物に用いて単一細胞の染色体上のヘテロクロマチン領域(多数の遺伝子発現が抑制された領域)の近くで、遺伝子の発現状態が一定の規則性を持ってエピジェネティックに切り替わる領域があることを発見しました。そこに、わずかな励起光で測定可能な蛍光タンパク質になる遺伝子を挿入し、単一細胞の生涯におけるエピジェネティックな遺伝子の発現変化の可視化に成功しました。さらに、その結果に統計処理の解析を加え、単一細胞の世代を超えた発現状態の変化を定量的に解析し、一定の規則性を持って発現状態が切り替わること、またその切り替わりをつかさどる制御遺伝子(GCN5 遺伝子)を明らかにしました。この結果は、それらの制御遺伝子の機能を支配することで、遺伝子の発現に新たな規則性を与え、例えば寿命などの細胞の運命を意図的に制御できることを示唆しています。
今後、本手法により出芽酵母で得られた栄養状態あるいは放射線などの外的要因が1つ1つの細胞に与える影響とその原因遺伝子が特定されれば、将来的にその知見をヒトにおけるさまざまな後天性疾患の原因解明に役立てるとともに、創薬の分野にも新たな方向性を提示することが期待されます。本研究は、東京大学 生産技術研究所の小林 徹也 准教授と共同で行い、本研究成果は、2013年7月2日(米国東部時間)発行の国際科学誌「PLOS Biology」に掲載されます。
<研究の背景と経緯>
「エピジェネティクス」とは、同じDNA塩基配列を持っているにも関わらず、DNA塩基配列に依存せずに遺伝子の発現状態が変化する制御機構で、この制御機構が個々の細胞の多様性を生み出し、また、子孫にも受け継がれて行くため、がんをはじめとするさまざまな後天性疾患の原因の1つであることが報告され注目を集めています。
ところが、エピジェネティックな制御機構について、細胞ごとに違いがあるのか、また何らかの規則性があるのか、ということの実態は不明でした。
このメカニズムを解明するためには、個々の細胞の挙動を追跡する必要がありますが、これまでは、単一細胞でエピジェネティックな遺伝子の発現状態の変化を追跡できる可視化・解析手法は存在していませんでした。そのため、さまざまな発現状態が混在している細胞集団を用いてその平均値によって発現状態の解析を行ってきましたが、それでは、個々の細胞の持つ特性を見いだすことはできなかったため、新たな追跡手法の開発が望まれていました。
そこで今回、単一細胞におけるエピジェネティックな発現状態変化を追跡する独自な手法の開発を目指しました。
<研究の内容>
沖 昌也 准教授らは、親子関係の同定が容易に行える出芽酵母を用いて、そのエピジェネティックな発現状態について研究を行いました。最初に、染色体上で高度に凝集したヘテロクロマチン構造(多数の遺伝子発現が抑制された領域)を形成する領域の近くで、分裂を繰り返すだけで遺伝子の発現状態がエピジェネティックに変化する領域を同定しました。そこに蛍光タンパク質になる遺伝子を挿入し、蛍光顕微鏡下で培養したところ、1つの細胞の生涯を通して、さらに世代を超えて遺伝子のエピジェネティックな発現状態変化を追跡することに成功しました(図1)。
本追跡手法では、細胞をわずかな隙間に挟み込み、1次元方向にのみ増殖できる特殊な環境下で培地を継続的に供給し続けました。このことにより、世代を超えたエピジェネティックな発現状態変化を追跡するために必要な長時間培養を可能としました。また、励起光としてLEDを用いることで細胞へのダメージを減らし、さらに一細胞周期で発現し、細胞内に局在できて、わずかな励起光でも測定可能な遺伝子と蛍光タンパク質になる遺伝子を融合することによって、蛍光輝度を正確に定量することが可能となり、エピジェネティックな発現状態の変化の可視化に成功しました。
しかし、本来生物の持つエピジェネティックな揺らぎ(細胞内のさまざまな状況によって生じる遺伝子発現の個体間のばらつき)の規則性を見いだすには、イメージング実験で得られたデータ(図2)の蓄積だけでは不足だったため、別途、統計処理法を開発し、規則性および有意差を数値で表す必要がありました。
そこで、東京大学 生産技術研究所の小林 徹也 准教授(元 JST さきがけ「生命現象の革新モデルと展開」研究領域研究者)と共同研究を行い、統計検定法を用いて、エピジェネティックな発現状態変化を解析することで、個々の細胞における揺らぎの規則性を定量的に解析し、数値で表すことが可能となりました。その結果、単一細胞遺伝子の発現状態の変化について世代を超えて可視化・追跡し、さらに、その変化を定量的に解析する一連の手法の開発に成功しました。
個々の細胞は、分裂を繰り返して、世代を超えてエピジェネティックに発現状態が変化する際に、一定の規則性を持って切り替わることを解明しました(図3(A)、表1)。
また、その規則性を保つために必要なGCN5 やSAS2 (ともに遺伝子の転写調節などの機能を持つことで知られる遺伝子)などの遺伝子を発見しました。これらの遺伝子を破壊すると、ある遺伝子は、生まれてから死ぬまでの遺伝子の発現状態の切り替わる頻度(遺伝子が発現状態から休止する状態(OFF)、または逆の状態(ON)への切り替わり)を下げて、一方向に偏りを持たせられることが分かりました(図3(B)、表1)。また、逆に切り替わりの頻度を上昇させることができる遺伝子(制御遺伝子)が存在することも分かりました(図3(C)、表1)。これら規則性の違いは、統計処理により有意差を数字で表すことができたことによって明らかになったものです(表1)。
なお、本研究は、JST 戦略的創造研究推進事業 個人型研究(さきがけ)の「エピジェネティクスの制御と生命機能」研究領域(研究総括:向井 常博 西九州大学 学長)における研究課題「エピジェネティックな遺伝子発現切り替わりメカニズムの解明」(研究者:沖 昌也)の一環として行われました。
<今後の展開>
今回、単一細胞での解析によって得られた結果は、細胞集団での解析結果では明らかにできなかった新たな知見を多く見いだしました。本成果は、個々の細胞がエピジェネティックな発現制御機構により多様性を生み出す仕組みは、遺伝子レベルの制御によって一定の方向性を持たせることが可能であることを示します。例えば、今回特定したGCN5 制御遺伝子の働きを弱める薬剤などを用いて機能を支配することにより、遺伝子の発現に新たな規則性を与え、細胞の運命を操作することが可能であることを示唆しています。
また、エピジェネティックな制御に関わる遺伝子は、酵母からヒトまで幅広く保存されており、上記酵母の解析から得られた知見は、ヒト細胞にも幅広く応用できることが展望されます。
今後、この単一細胞の解析法を用いて、「培養液中のグルコース濃度を変化させ生活習慣の違いによりエピジェネティックな発現状態はどのように変化し、細胞の寿命にどのように影響してくるのか」、「低濃度の発がん性物質を接収し続けるとエピジェネティックな発現がどのような影響を及ぼし、細胞はどの程度のダメージを受けるのか」、「生まれたての細胞が低線量の放射線を浴び続けた場合、寿命も含め将来的にどのような影響が現れてくるのか」という栄養状態・発がん性物質・放射線などの外的要因が1つ1つの細胞に与える影響を調べ、それぞれの現象においてエピジェネティックに制御されている原因遺伝子を特定できれば、将来的にその知見をヒトにおけるさまざまな後天性疾患の根源の解明に役立て、創薬の分野にも新たな方向性を提示することが期待されます。
<参考図>

図1 単一細胞における遺伝子の発現変化の可視化・追跡結果
1つの細胞から分裂を開始し0時間(00:00)、1時間20分後(01:20)、2時間40分後(02:40)と、遺伝子の発現状態の変化を継時的に追跡している。緑の点がある細胞では遺伝子が発現し、ない細胞では発現していない。元は同じ遺伝子を持った1つの細胞から分裂しているにも関わらず、分裂を繰り返すとさまざまな発現状態の細胞が混在していく。各写真の右上には、それぞれの時間における同一の細胞を拡大し、矢印で示しているが、分裂を繰り返すと、時間経過とともに遺伝子の発現が抑えられている(03:20までは発現し、04:40以降の発現はない)。
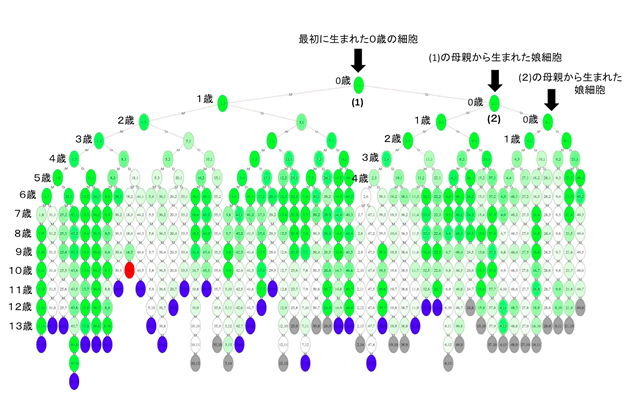
図2 単一細胞の遺伝子の発現状態の変化を示した樹系図
図1の追跡結果をもとに、1つの細胞から分裂を開始して生涯における世代を超えた発現状態の変化を表す、小林准教授作成の統計処理プログラム。緑は遺伝子が発現した細胞、白は発現していない細胞、赤はその時点で分裂が止まった細胞(細胞の寿命)、青はスペースの都合上、それ以降の追跡結果を図から省略した細胞、灰色はデータ量が膨大でそれ以降の追跡結果がない細胞。
1番上が0歳の細胞で、その右下の細胞は最初の子供(娘細胞)、左下の細胞は子供を産んだことで1歳年を取った「最初に生まれた細胞を示す(左に行くほど年齢を重ねて一番左下は13歳の発現状態)。この樹形図によって同一の細胞でも年齢を重ねると発現状態が変化し、最初は同じDNAを持った1つの細胞から分裂を開始したにも関わらず、個々の細胞がその後、さまざまな発現状態に変化していることが明らかになった。(※色や図の見方は図3も同様)
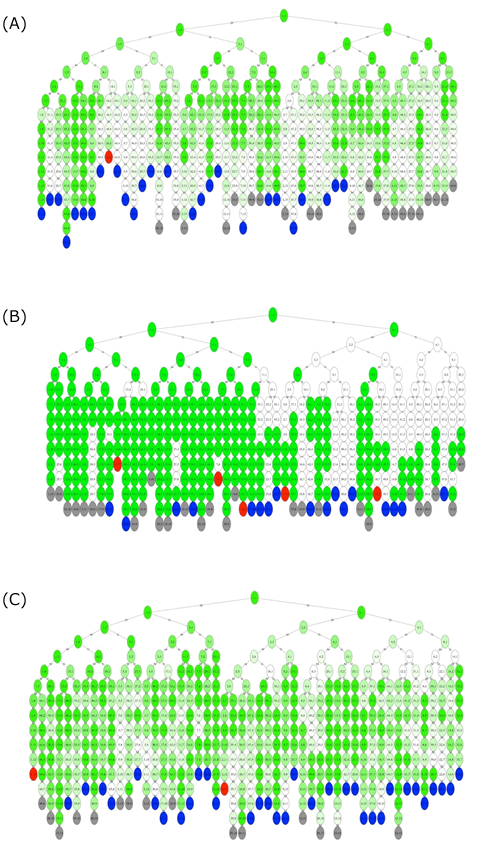
図3 遺伝子を破壊した際のエピジェネティックな発現状態の変化(模式図)
(A) 遺伝子を破壊していない野生株の追跡結果(発現制御遺伝子を破壊する前)
(B) (A)の細胞からGCN5 遺伝子を破壊した株:切り替わりの頻度が下がった
(C) (A)の細胞からSAS2 遺伝子を破壊した株:切り替わりの頻度が上がった
(A)と比べて (B)の左側には発現状態が ON(緑)の細胞が増え、右側には発現状態がOFF(白)の細胞が増えており、ONからOFF、OFFからONの切り替わりの頻度が下がり、同じ発現状態が世代を超えて維持されやすくなったことを示している。また、同一細胞を表す縦のラインに注目すると、(A)と比較して(C)は分裂を繰り返すことで同じ発現状態が維持されにくくなり、ONからOFF、OFFからONの切り替わりの頻度が上昇している。この結果から、発現制御遺伝子の機能を支配することで、細胞の運命を意図的に制御できることが分かる。
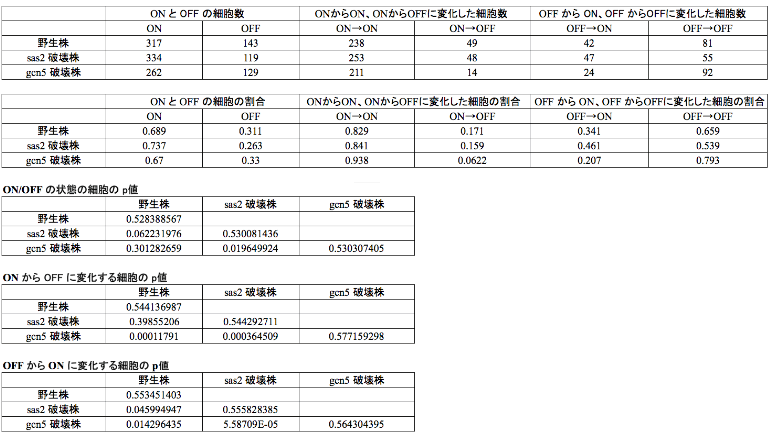
表1 遺伝子を破壊した際のエピジェネティックな発現状態の変化(統計処理データ)
図3(A)の野生株、(B)のGCN5 破壊株、(C)のSAS2 破壊株の発現状態遷移の頻度を統計処理した結果のデータ。GCN5 やSAS2 を破壊すると、破壊する前の株(野生株)と比較して、数値的にONとOFFの細胞の割合や切り替わりの頻度が変化していることが分かる(2番目のカラム)。また、統計処理を行っても(A)~(C)の間の発現状態の変化には定量的な有意差が見られる(3~5番目のカラム)。この結果は、エピジェネティックな発現状態が特定の遺伝子によって制御されていることを示している。
<論文タイトル>
“Single cell visualization of yeast gene expression shows correlation of epigenetic switching between multiple heterochromatic regions through multiple generations.”
(単一細胞可視化システムによる世代を超えたエピジェネティックな発現制御機構の解明)
doi: 10.1371/journal.pbio.1001601
<お問い合わせ先>
<研究に関すること>
沖 昌也(おき まさや)
福井大学 大学院工学研究科 生物応用化学専攻 准教授
〒910-8507 福井県福井市文京3-9-1
Tel:0776-27-8640 Fax:0776-27-8747
E-mail:
<JSTの事業に関すること>
木村 文治(きむら ふみはる)、川口 貴史(かわぐち たかふみ)
科学技術振興機構 戦略研究推進部 ライフイノベーショングループ
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3525 Fax:03-3222-2067
E-mail:
<報道担当>
福井大学 総合戦略部門 広報室
〒910-8507 福井県福井市文京3-9-1
Tel:0776-27-9850 Fax:0776-27-8518
E-mail:
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
Tel:03-5214-8404 Fax:03-5214-8432