<要旨>
酵素は環境に優しい理想的な高機能触媒であるが、その精巧な鍵穴注1)をもった数万から数10万の分子量を有する触媒注2)を単一分子として人工的に設計・合成するのは技術的に困難である。名古屋大学 大学院工学研究科 化学・生物工学専攻の石原 一彰 教授らの研究グループでは、JST・CRESTの研究の一環として、『予め分子設計しておいた数種類の小分子をフラスコ内で混ぜ、分子が自発的に集まって機能化する自己組織化注3)を利用し一種類の超分子錯体注4)に一気に収束させて、酵素機能を凌駕するナノサイズの高機能触媒を設計・開発する』ことを目的に研究を行っている。
この度、同研究グループは、ミネラルとして体内の必須元素でもあるマグネシウムイオンと入手容易で安価な光学活性注5)ジオールを2:3のモル比で混ぜるだけで自己組織化し一種類の超分子錯体に収束することを見出した。さらに、この超分子錯体(3or4)を不斉触媒として、不飽和カルボニル化合物への有機リン化合物の付加反応を試したところ、用いる基質に応じて、高選択的に光学活性β-ホスホリルエステルや光学活性α-ヒドロキシホスホン酸エステルが合成できることがわかった。光学活性β-ホスホリルエステルは様々なP,N-配位子注6)へと合成変換できるため、新たな不斉触媒の開発に繋がる。また、光学活性α-ヒドロキシホスホン酸エステルは、加水分解酵素であるプロテアーゼやエステラーゼの阻害剤合成の鍵中間体となることが知られているため、新薬の開発への貢献が期待される。本触媒反応はグラムスケールでも再現性よく進行し、簡便な実験操作で実施できるため、極めて実用性の高い技術である。
なお、本研究成果はドイツ化学会誌アンゲヴァンテ・ケミー・インターナショナル・エディションから注目の論文(VIP = very important paper)として評価され、近日中に同誌のオンライン版に公開される。また掲載号の表紙を飾ることも決定している。
本研究は科学技術振興機構(JST)の戦略的創造研究推進事業(CREST)として実施した。
| 研究領域 |
「プロセスインテグレーションに向けた高機能ナノ構造体の創出」
(研究総括:入江 正浩(立教大学)) |
| 研究課題 |
「酸・塩基複合型超分子動的錯体を鍵とする高機能触媒の創製」
(研究代表者:石原 一彰(名古屋大学)) |
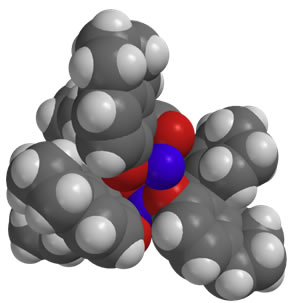
Mg2・((R )-H8-BINOLate)3超分子錯体触媒(3)
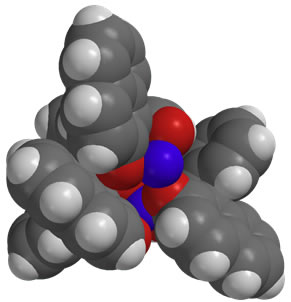
Mg2・((R )-H8-BINOLate)3超分子錯体触媒(4)
<背景>
医薬品の多くは光学活性化合物であり、その選択的合成法の開発は重要な研究課題である。なかでも、触媒は合成反応の活性化・選択性を制御する要の分子であり、より優れた触媒を求めて、世界中で激しい研究競争が繰り広げられている。酵素は自然界に存在する天然の触媒であり、生命活動に必要な様々な反応を司る。しかし、自然界には一方の鏡像異性体注7)のみしか存在しないため、酵素反応では標的化合物の一方の鏡像異性体しか合成することができない。しかし、医薬品等の開発には両鏡像異性体を作り分ける技術が必要である。また、酵素は数万~数十万の分子量を有する巨大で複雑なタンパク質からできており、非天然型の鏡像異性体を人工的に合成することは困難である。酵素の種類もその基質適応範囲も限られており、自在に標的有機化合物の両鏡像異性体を作り分けるためには、両鏡像異性体の入手が容易な人工触媒の開発が必要不可欠である。
有機反応の活性化・選択性は、触媒活性中心元素の電子的効果と、酵素の鍵穴に相当する反応場注8)のなかに遷移状態注9)を包摂する効果で決まる。酵素はその大きな分子サイズゆえ、精巧な鍵穴を触媒活性中心近傍にもつことができる。一方、現在、人工触媒の主流は単一分子触媒注10)であるが、単一分子内に選択性を誘導する反応場を設計・合成するのは容易ではない。触媒分子のサイズと複雑さに比例して、触媒自身の合成が難しくなるのは必然であり、製造コストの壁が実用化を阻むという問題が生じている。
例えば、上図に示すように、市販の比較的単純な構造を有する光学活性化合物を配位子注11)として単一分子触媒(1)を調製しても、触媒活性中心が剥き出しになり、その近傍にはオープンなスペースが出来るだけである。これでは鍵穴とは言えず、反応の選択性を制御することはできない。単一分子触媒(2)を用いて鍵穴を構築すれば、鍵穴に適合した触媒・基質複合体の形成によって標的化合物を得ることができるが、2を得るためには、市販の光学活性化合物を出発原料に数段階の反応を経て配位子を合成する必要がある。その分、触媒の製造コストは上がり実用化が難しくなる。また、触媒の製造に時間を要するということは、触媒の最適化にも時間を要することを意味する。
名古屋大学 大学院工学研究科 化学・生物工学専攻の石原 一彰 教授らの研究グループでは、JST・CRESTの研究の一環として、超分子化学の概念を触媒設計に導入し、予め精密設計した複数の小分子をフラスコ内で混ぜ合わせるだけで分子同士が自己組織化し、その結果、生じるナノサイズの超分子を触媒として用いる研究に取り組んでいる。この方法では、設計・合成すべき配位子のサイズは単一分子触媒の配位子より小さく、比較的単純な分子構造でもよいので、製造コストを抑えることができる。また、超分子設計では、単一分子触媒では困難な、反応遷移状態を包摂するような精巧な鍵穴を触媒内に作り上げることができる。さらに、超分子触媒の構成成分である小分子の組み合わせは無尽蔵であるため、触媒設計の多様性の点で優れている。その反面、一つの狙った超分子構造だけに自己組織化せず、複数の構造の超分子ができることによって目的反応の選択性や反応性がむしろ低下する危険性もあり、配位子の設計が極めて重要である。
下図は先に示した単一分子触媒(1)が会合していく過程を示しているが、これを制御して選択的にどれか一つの超分子構造にするのは容易なことではない。酵素を凌駕する高活性と高選択性を発現する人工触媒の開発には、超分子触媒の合成技術を高めることが急務である。
研究成果その1:不斉1,4-ヒドロホスフィニル化反応
マグネシウムは動物においては骨、血液、筋肉などに、植物においては光合成色素クロロフィルなどに含まれる代表的なミネラルであり、毒性も低く安価である。このマグネシウムに着目し、不斉超分子触媒の開発研究を行なった。その結果、下図に示すように、市販の光学活性ジオール (R )-8H-BINOL (正式名称:5,5’,6,6’,7,7’,8.8’-オクタヒドロ-1,1’-ビ-2-ナフトール)とマグネシウムイオン(正式名称:ジブチルマグネシウム)を3:2のモル比で混合すると、一種類の超分子構造(3)に収束することがわかった。
この超分子3を不斉触媒注12)(触媒量2.5~5mol%[1mol%の触媒とは基質分子100molに対し1molの触媒を用いるという意味])に用いてα,β-不飽和エステルとリン化合物(正式名称:ジアリールホスフィンオキシド)を反応させると、>90%ee注13)のエナンチオ選択性注14)と100%の位置選択性で光学活性β-ホスホリルエステルが得られることがわかった(不斉1,4-ヒドロホスフィニル化反応注15))。生成物から誘導される光学活性ホスファニルオキサゾリンは、新たな遷移金属触媒開発のための光学活性P,N-配位子として期待される。
遷移金属触媒の光学活性配位子としては、野依良治らのBINAPに代表されるC2対称注16)P,P-配位子注17)、正宗悟やD.A.Evansらの光学活性ビス(オキサオゾリン)に代表される>C2対称N,N-配位子注18)などが有名であるが、最近、非対称なP,N-配位子についても、A.Pfaltzらによってその有効性が報告されている。特に、Ubaphox(市販)と呼ばれるP,N配位子とイリジウムの錯体は不斉水素化反応の極めて優れた触媒となることが知られており、重要な医薬品中間体である光学活性クロマンやインドール類の不斉合成に役立っている。今回、開発した反応によって下図のようなホスファニルオキサゾリンが得られれば、これまで合成困難であったUbaphoxの類縁体を精密に分子設計し合成できるので、Ubaphoxを凌ぐ不斉配位子の開発に繋がると期待される。
予想される反応機構
上述の超分子触媒には活性な酸点と塩基点がそれぞれ1つずつ存在する。前者はマグネシウムカチオン(Mg2+)、後者はオキシアニオン(O-)である。これら酸・塩基の近傍には酵素の鍵穴に相当する不斉反応場が存在する。リン化合物は、そのプロトンをオキシアニオンによって引き抜かれ、アニオン性求核剤注19)としてマグネシウムカチオンに捕獲される。一方、α,β-不飽和エステルはフェノール性プロトンによって求電子剤注20)として活性化される。この二重活性化が駆動力となり不斉1,4-ヒドロホスフィニル化反応が進行する。
研究成果その2:不斉1,2-ヒドロホスホニル化反応(Pudovik反応)
ホスホン酸(R-PO(OH)2)はカルボン酸(R-CO2H)の生物学的等価体として機能し、医薬品の開発において、生物活性物質のアミド結合やエステル結合をホスホン酸アミドやホスホン酸エステルに置き換える方法が広く取り入れられている。例えば、α-ヒドロキシホスホン酸誘導体はα-アミノ酸由来のペプチド結合やα-ヒドロキシカルボン酸由来のエステル結合が加水分解される際の遷移状態アナログ注21)であり、レニン阻害剤、HIVプロテアーゼ阻害剤等、種々のプロテアーゼ阻害剤やエステラーゼ阻害剤の合成に利用されている。
光学活性α-ヒドロキシホスホン酸エステルはアルデヒドと亜リン酸ジアルキルとの不斉1,2-ヒドロホスホニル化反応(Pudovik反応)注22)によって合成可能であり、渋谷 皓(東京薬科大学)や柴崎 正勝(元 東京大学)らによる先駆的な業績があるものの基質一般性などの課題も残っている。
今回、市販の光学活性ジオール(R )-BINOL(正式名称:1,1’-ビ-2-ナフトール)とマグネシウムイオン(正式名称:ジブチルマグネシウム)を3:2のモル比で混合して調製される超分子触媒(4)(触媒量5mol%[1mol%の触媒とは基質分子100molに対し1molの触媒を用いるという意味])は、α,β-不飽和ケトンと亜リン酸ジメチルとの不斉1,2-ヒドロホスホニル化反応に有効であることがわかった。この反応によって>80%eeのエナンチオ選択性と100%の位置選択性で得られる光学活性α-ヒドロキシホスホン酸エステルは1回の再結晶操作で光学純度を>97.5:<2.5にすることができた。
こうして得られた高純度の光学活性α-ヒドロキシホスホン酸エステルはプロテアーゼ阻害剤やエステラーゼ阻害剤の合成に利用できる。また、生成物を立体選択的に環化して得られるオキサホスホラノール類のなかにはアセチルコリンを分解する酵素の働きを抑える抗コリンエステラーゼ作用があるものが既に報告されており、生成物がアセチルコリンの量が減少するアルツハイマー病の特効薬の鍵合成中間体になる可能性がある。
予想される反応機構
前述の超分子触媒と同様に、この超分子触媒にも活性な酸点と塩基点がそれぞれ1つずつ存在する。前者はマグネシウムカチオン、後者はオキシアニオンである。これら酸・塩基の近傍には酵素の鍵穴に相当する不斉反応場が存在する。亜リン酸ジメチルは、そのプロトンをオキシアニオンによって引き抜かれ、アニオン性求核剤としてマグネシウムカチオンに捕獲される。一方、α,β-不飽和ケトンはフェノール性プロトンによって求電子剤として活性化される。こうして二重活性化に伴い、両者間の不斉1,2-ヒドロホスホニル化反応が進行する。1,4-または1,2-付加の位置選択性はリン求核剤のハード・ソフト注23)に依存しており、触媒による制御ではない。亜リン酸ジメチルはジアルキルホスフィンオキシドよりもハード塩基であり、1,2-付加しやすい。
<結論>
これら2つの超分子触媒3,4は安全・安価な2種類の試薬を3:2のモル比で混ぜるだけで調製できる点が画期的であり、単一分子触媒から超分子触媒へと発想を転換したことが功を奏した。これらの触媒反応はミリグラムスケールからグラムスケールにアップしても問題なく進行することを確かめており、キログラムスケールにアップすることも可能であると予想される。実験操作も簡便で、安全・安価な触媒を用いる本触媒技術は極めて実用性が高いと言える。
今回の成功例が示すように、他の入手容易な光学活性配位子と金属イオンの組み合わせのなかにも、一種類の超分子錯体に自己組織化する「黄金のモル比」があるかもしれない。また、これまでに単一分子触媒として報告されたもののなかにも、実のところ、真の触媒活性種は超分子錯体触媒であるという例もあるかもしれない。単一分子触媒としての設計だけでなく、超分子錯体への自己組織化の可能性も十分に考慮し、触媒設計すれば、複雑な構造分子の設計・合成に頼ることなく、優れた不斉触媒を開発できる可能性があると言えよう。既に、当研究室では、今回の例以外にも、いくつかの超分子錯体触媒を見出し、ユニークな選択性の発現に成功している。
<用語解説>
- 注1) 鍵穴
- 酵素や触媒の活性中心近傍に存在する溝またはポケット。一方、反応基質は鍵に喩えられる。反応は鍵穴のなかで活性化される。
- 注2) 触媒
- 特定の化学反応の反応速度を速める物質で、自身は反応の前後で変化しないものをいう。また、反応によって消費されても、反応の完了と同時に再生するものも触媒とされる。
- 注3) 自己組織化
- 自然に秩序が生じて、自分自身でパターンのある構造を作り出して組織化していく現象。
- 注4) 超分子錯体(触媒)
- 複数の分子が共有結合以外の結合(配位結合、水素結合など)や比較的弱い相互作用により秩序だって集合してできる錯体(触媒)。
- 注5) 光学活性
- 両鏡像異性体のどちらかが過剰に存在するために旋光性を示す性質。
- 注6) P,N-配位子
- 窒素原子とリン原子で中心原子にキレートする配位子。
- 注7) 鏡像異性体
- 原子の立体配置が互いに鏡像の関係となる立体異性体。光学異性体あるいはエナンチオマーとも呼ぶ。
- 注8) 反応場
- 反応が起こる空間。鍵穴も反応場である。
- 注9) 遷移状態
- 化学反応の過程で原系から生成系に変換するときに通る最もエネルギーの高い状態。
- 注10) 単一分子触媒
- 共有結合で結合した単一分子の触媒。
- 注11) 配位子
- 触媒活性中心原子に配位する化合物のことで、触媒活性、反応場、立体選択性を制御するための制御分子である。
- 注12) 不斉触媒
- 一方の鏡像異性体を選択的に合成する触媒。
- 注13) ee
- enantiomeric excessの略で、キラルな化合物の光学純度(鏡像異性体過剰率)を表す言葉。eeは多い方の物質量から少ない方の物質量を引き、全体の物質量で割った値である。
- 注14) エナンチオ選択性
- 両鏡像異性体の一方が生成する選択性。
- 注15) (不斉)1,4-ヒドロホスフィニル化反応
- 1,4-ヒドロホスフィニル化反応とはα,β不飽和カルボニル化合物とジアリールホスフィンオキシド(R2P=O)との1,4-付加反応のことである。生成物はβ-ホスホリルカルボニル化合物であり、その不斉反応では光学活性体が生成する。
- 注16) C2対称
- ある軸に対して180度回転させても、その分子が同じに見える場合、C2対称性があるという。
- 注17) P,P-配位子
- 2つのリン原子で中心原子にキレートする配位子。
- 注18) N,N-配位子
- 2つの窒素原子で中心原子にキレートする配位子。
- 注19) 求核剤
- 異なる化学種の間で電子の授受をともないながら化学結合を生成する反応において、電子を与える側の化学種を指す。
- 注20) 求電子剤
- 異なる化学種の間で電子の授受をともないながら化学結合を生成する反応において、電子を受け取る側の化学種を指す。
- 注21) 遷移状態アナログ
- 酵素反応において、酵素と基質が「遷移状態」を形成した後に生成物を生じる。この過渡的にしか存在しない遷移状態とよく似た構造をもち安定な化合物を遷移状態アナログと呼ぶ。遷移状態アナログは酵素活性中心と直接相互作用し、強力な酵素阻害剤として利用できる。
- 注22) (不斉)1,2-ヒドロホスホニル化反応(Pudovik反応)
- 1,2-ヒドロホスホニル化反応とはカルボニル化合物と亜リン酸エステル((RO)2P(=O)H)との1,2-付加反応のことである。生成物はα-ヒドロキシホスホン酸エステルであり、その不斉反応では光学活性体が生成する。
- 注23) ハード・ソフト
- HSAB則(hard and soft acids and Bases)は酸および塩基の相性を、硬い、軟らかい、という表現を使って分類したものである。一般に軟らかい酸と軟らかい塩基のペアは反応しやすく強い結合を形成する。一方、硬い酸と硬い塩基のペアもまた反応しやすく、強い結合を形成する。
<掲載論文>
Chiral Magnesium(II) Binaphtholates as Cooperative Brφnsted/Lewis Acid-Base Catalysts for Highly Enantioselective Addition of Phosphorous Nucleophiles to α,β-Unsaturated Esters and Ketones
キラルマグネシウム(ⅠⅠ)ビナフトラートを酸・塩基協同機能触媒として用いるリン求核剤のα,β—不飽和エステル及びケトンへの高エナンチオ選択的付加反応
<著者>
Manabu Hatano, Takahiro Horibe, Kazuaki Ishihara
波多野 学(准教授)、堀部 貴大(大学院生)、石原 一彰(教授)
名古屋大学 大学院工学研究科 化学・生物工学専攻
<掲載誌>
Angewandte Chemie International Edition
アンゲヴァンテ・ケミー・インターナショナル・エディション
ドイツ化学会誌、Wiley-VCHより出版
化学の分野ではNature Chem.やJ.Am.Chem.Soc.と肩を並べる最高峰の学術誌である本誌に掲載されることが決定したのみならず、掲載論文のなかでも特にVIP(very important paper)の栄誉が与えられ、掲載号の表紙を飾ることになった。
<連絡先>
<研究成果に関すること>

石原 一彰(教授)
名古屋大学 大学院工学研究科 化学・生物工学専攻 生物機能工学分野
電話:052-789-3331 Fax:052-789-3331
E-mail:
<報道に関する問い合わせ先>
名古屋大学 広報室
電話:052-789-2016 Fax:052-788-6272
E-mail:
<JSTの事業に関すること>
古川 雅士
科学技術振興機構 戦略研究推進部
電話:03-3512-3531 Fax:03-3222-2066
E-mail: