本研究成果のポイント
- 代謝産物濃度の実測データに、統計学的な理論と数式モデリング理論を組み合わせる
- 乳酸菌の解糖系で実証し、未発見だったフィードバック制御の存在の可能性も見いだす
- 理論的な代謝経路の設計により、有用代謝産物の生産性向上に貢献
理化学研究所(野依 良治 理事長)と九州大学(有川 節夫 総長)は、生体内で作り出される代謝産物の濃度を測定し、その経時変化データだけを用いて、「代謝反応ネットワーク」を推定する手法を開発しました。これは、理研 植物科学研究センター(篠崎 一雄 センター長) 代謝システム解析チームの平井 優美 チームリーダー、シユタサ・カンスポーン 特別研究員、九州大学 大学院農学研究院の白石 文秀 教授らの共同研究グループによる成果です。
分析機器の性能向上により、生体内の低分子成分である全ての代謝産物(メタボローム注1))が一斉分析できるようになりました。そのため、現在ではさまざまな生体試料から、複雑な「代謝反応ネットワーク(生物の代謝経路とその制御)」の情報を含むメタボロームデータが得られています。しかし、メタボロームデータは情報量が非常に大きいため解析が困難です。そこで、数式モデルを構築し、コンピューターを使ったシステム解析によって、生命現象の仕組みを理解しようとする試みが活発に行われています。一方、微生物や植物を利用して有用物質を大量生産させる代謝工学の分野では、その生物が持つ代謝反応ネットワークを正確に理解し人為的に制御することが求められています。しかし、未発見の代謝経路や、既知ではあるもののその制御の仕組みが十分に理解されていない代謝経路がまだ多く残されています。
今回、共同研究グループは、既知の代謝経路の知見を使わずに、代謝産物濃度の経時変化の実測データだけで代謝反応ネットワークを推定する手法を開発しました。この手法は、統計学的な理論と数式モデリングの理論を組み合わせているため、代謝反応ネットワークの推定と同時に、数式モデルも構築することができます。この数式を用いると、目的物質の生産速度を決める主要な代謝経路を推定することも可能です。実際に、既に知られている乳酸菌の解糖系注2)とその周辺の代謝経路にこの手法を適用し、代謝反応ネットワークや主要な代謝経路を推定しただけでなく、これまで未発見だったフィードバック制御注3)が存在する可能性も見いだしました。
今後、医薬品分野などで利用されているものの、生合成経路が未解明な有用代謝産物に対してこの手法を適用することで、代謝反応ネットワークを正確に理解して生産性の向上を図る、といった新しい応用への展開が可能になると期待できます。
本研究成果は、JST 戦略的創造研究推進事業 チーム型研究(CREST)(研究代表者:平井 優美)の一環として行われ、米国のオンライン科学雑誌『PLOS ONE 』(1月10日付け:日本時間1月11日)に掲載されます。
1.背景
「代謝」とは生体内で起こる化学反応のことで、体外から取り入れた物質を用いて自身を構成する新たな成分を合成したり、または、分解してエネルギーを取り出したりします。代謝は全ての生物が持つ仕組みで、代謝の結果生じる物質を「代謝産物」と呼びます。特に植物やある種の微生物は、人間にとって有用な代謝産物(アミノ酸や医薬品原料など)を合成する代謝経路を持つため、これを人為的に改変し効率よく合成させる「代謝工学」が注目されてきています。
生体内のさまざまな化学反応からなる代謝経路は、酵素と呼ばれる多種類のタンパク質を触媒にして行われており、その経路はまるで大都市の地下鉄路線のように複雑なネットワークを構成しています。さらに酵素は、さまざまな代謝産物によってフィードバック制御を受けており、代謝産物間の関係をさらに複雑にしています。このため、特定の有用物質の生産量増大を目指す代謝工学では、どの代謝産物が反応してどの代謝産物に変換されるか、その反応はどの代謝産物によって制御されているか、といった「代謝反応ネットワーク」を網羅的に理解することが必要です。これまでは、個々の化学反応の仕組みやそれを触媒する酵素の特性を、生化学的な方法で一つ一つ明らかにすることで、代謝経路は少しずつ解明されてきました。しかし、生体内に何百、何千種類もある化学反応を一つ一つ検討することは容易ではありません。
一方、近年になって、全ての代謝産物(メタボローム)を網羅的かつ一斉に解析する分析技術が発達し、多くの代謝産物の量と種類を測定できるようになりました。そこで共同研究グループは、代謝産物濃度の実測データだけを用いて、代謝反応ネットワーク全体を1回で推定する方法の開発に挑みました。
2.研究手法と成果
代謝が安定している定常状態では、各代謝産物の生体内の濃度は一定です。しかし、生育環境を変化させたり、化合物を投与したりするなどの小さな攪乱(かくらん)を生体外から与えると、各代謝産物の濃度は一時的に変化して、その後、元の定常状態に戻ります。この一時的な増減の経時変化は代謝産物によって異なり、個々の代謝産物の代謝反応ネットワークでの位置に基づく結果と考えられます。
そこで共同研究グループは、攪乱後の代謝産物濃度の経時変化を測定して、代謝反応ネットワークとその特徴を推定する手法を開発しました。具体的には、①時系列データをつなぐ近似曲線の補正(局所回帰注4)によるスムージング)、②時系列データに基づくグレンジャーの因果関係注5)の検定、③バイオケミカルシステム理論注6)による代謝反応ネットワークのモデリング、④非線形最小二乗法注7)によるパラメータ決定、という4つの理論を組み合わせた新たなアルゴリズムです(図1、図2)。
まず、代謝産物濃度の経時変化を示す実測データは、生物学的ばらつきや解析誤差を含んでいるため、局所回帰を行って各データをつなぐ近似曲線を求めます。次に、代謝産物同士は直接的または間接的に相互作用しているため、各代謝産物を他の代謝産物と組み合わせてグレンジャーの因果関係を検定します。その結果、統計的に有意な因果関係があると判断できた代謝産物だけで仮の代謝反応ネットワークを構成します。併せて、この仮の代謝反応ネットワークにバイオケミカルシステム理論を適用し、数式モデルを構築します。このモデルには、代謝反応やその制御関係を表すパラメータが多数含まれています。最後に、数式モデル中のパラメータを非線形最小二乗法で決定します。ここで、ある代謝産物が他の代謝産物に与える影響の大きさを表す反応次数という複数のパラメータのうち、他に比べて小さい値となったものについては、その関係性を仮の代謝反応ネットワークから削除し、もう一度数式モデルを構築し直します。この検討を計算が収束するまで繰り返し、最後に残ったパラメータに基づいて代謝反応ネットワークを推定します。
実際に、14個の代謝産物でネットワークが構成されることが知られている乳酸菌の解糖系とその周辺の代謝経路に着目し、そのうち5個の代謝産物濃度の経時変化を既報の論文より取得して代謝反応ネットワークを求めました。その結果、これら5個の代謝産物のネットワーク内での相対的な位置を再現し、代謝反応ネットワークを正しく推定しました。さらに、これまで同定されていなかったフィードバック制御の存在の可能性も見いだしました。また、数式モデルに基づいて解析したところ、グルコースからグルコース-6-リン酸に至る反応が、乳酸生合成の速度を決める主要な代謝経路であることも推定できました(図3)。
3.今後の期待
微生物を用いた有用代謝産物の生産は、これまで産業界でも実用化されてきました。しかし、代謝反応ネットワークの全体を解明し、理論的に代謝経路を設計する研究はまだ始まったばかりです。また、地球温暖化の問題が近年顕著になってきており、植物の光合成能力を最大限に活用し、二酸化炭素を資源にさまざまな有用代謝産物を生産することが期待されています。しかし、植物の代謝反応ネットワークは微生物よりもさらに複雑で、その解明のための研究手法の開発が求められています。
今回開発した手法は、微生物や植物を用いた代謝工学の発展に大きく貢献すると期待できます。
なお、本研究成果は、JST 戦略的創造研究推進事業 チーム型研究(CREST)の「代謝調節機構解析に基づく細胞機能制御基盤技術」研究領域(研究総括:昭和薬科大学 西島 正弘 学長)における研究課題「植物アミノ酸代謝のオミクス統合解析による解明(研究代表者:平井 優美)」の一環として行われました。
原論文情報:
Kansuporn Sriyudthsak, Fumihide Shiraishi, and Masami Yokota Hirai.
“Identification of a Metabolic Reaction Network from Time-Series Data of Metabolite Concentrations.”,PLOS ONE, 2012,
doi: 10.1371/journal.pone.0051212
<参考図>
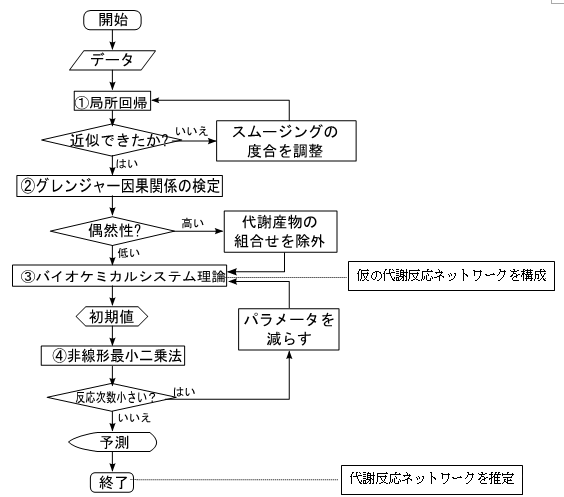
図1 開発した4つの理論を組み合わせたアルゴリズム
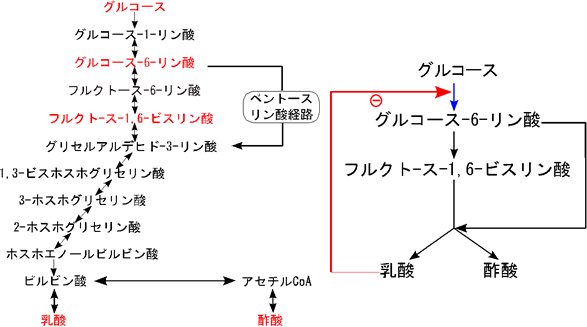
図3 乳酸菌がグルコースを解糖するときの代謝反応ネットワーク
- 左:14個の代謝産物で構成される既知の解糖系とその周辺の代謝経路。このうち5個の代謝産物(赤字)の実測データを用いて、代謝反応ネットワークを推定した。
- 右:5個の代謝産物の経時変化データから推定した代謝反応ネットワーク。乳酸が増えるとグルコースがグルコース-6-リン酸になる反応が抑制されるという、これまで同定されていなかったフィードバック制御の存在の可能性を見いだした(赤点線矢印)。また、グルコースからグルコース-6-リン酸に至る代謝経路が乳酸生合成の速度を決める主要な代謝経路(青矢印)と推定できた。
<用語解説>
- 注1) メタボローム
- メタボローム(metabolome)の-omeはラテン語で全体や総体という意味を表す。つまりメタボロームは、細胞内で合成された全代謝物質(metabolite+ome)の総体を指す。ゲノム(genome)が細胞内の全遺伝子(gene+ome)を指すのと同じ。
- 注2) 解糖系
- グルコース(ブドウ糖)を初発物質とし、一連の酵素反応により最終的にピルビン酸を生成するとともに、その分解過程で代謝に必要なエネルギーを獲得したり、他の代謝系で用いられる代謝物を生合成したりする代謝反応系。ほとんど全ての生物が解糖系を持ち、最も原始的な代謝系とされる。
- 注3) フィードバック制御
- 工学の概念であり、システムの状態や動作を維持するために、入力量の制御が出力量により行われること。代謝においては、経路の下流の代謝産物が上流の酵素反応に対して負の制御(システムの現在の状態と望まれる状態との差の方向に対して反対方向の制御)を行い、生体内で一定の量的バランスを維持する。
- 注4) 局所回帰
- 取得した狭い範囲のデータに対して、従属変数(例えば代謝産物濃度)が独立変数(例えば時間)にどう関わるかを推定すること。
- 注5) グレンジャーの因果関係
- ノーベル経済学賞を受賞したイギリスのグレンジャー(Granger)の定義による因果関係のこと。例えば、2つの要素XとYがあって、Xが変化した時にYもまた変化するならば、XからYへのグレンジャー因果があると呼ぶ。グレンジャー因果関係の有無は、F検定という統計的検定で検証する。
- 注6) バイオケミカルシステム理論
- 細胞内の酵素による触媒反応で構成する複雑な代謝反応ネットワークの特性を明らかにするための理論。各代謝産物濃度(Xi)の時間変化を以下の微分方程式で表す。右辺の第1項は代謝物Xiのプールへの正味の流入流束(単位時間、単位体積当たりで、その代謝産物が合成される速度をまとめたもの)、第2項は正味の流出流束(単位時間、単位体積当たりで、その代謝産物が分解される速度をまとめたもの)を表し、それぞれ合成、分解に影響を与える他の代謝産物濃度の累乗に比例する。
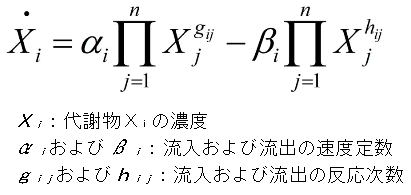
- 注7) 非線形最小二乗法
- 従属変数(例えば代謝産物濃度)と独立変数(例えば時間)の関係が直線的ではない、すなわち非線形の関係にある測定データに対して、最も適合する曲線を決定する手法の1つ。測定値と計算値の差の2乗和が最小となるように、両者の関係を表す式中のパラメータを決定し、結果としてそのような曲線を得る。代表的な手法にレーベンバーグ・マルカート(Levenberg-Marquardt)法がある。
<報道担当・問い合わせ先>
<問い合わせ先>
独立行政法人 理化学研究所
植物科学研究センター 代謝システム解析チーム
チームリーダー 平井 優美(ひらい まさみ)
特別研究員 シユタサ・カンスポーン
Tel:045-503-9491 Fax:045-503-9489
横浜研究推進部 企画課
Tel:045-503-9117 Fax:045-503-9113
国立大学法人 九州大学 大学院農学研究院
教授 白石 文秀(しらいし ふみひで)
Tel:092-642-7603 Fax:092-642-7603
<JSTの事業に関すること>
独立行政法人 科学技術振興機構 戦略研究推進部
石正 茂(いしまさ しげる)
Tel:03-3512-3524 Fax:03-3222-2064
<報道担当>
独立行政法人 理化学研究所 広報室 報道担当
Tel:048-467-9272 Fax:048-462-4715
独立行政法人 科学技術振興機構 広報課
Tel:03-5214-8404 Fax:03-5214-8432