ポイント
- マウスのES細胞、iPS細胞から卵子を作製
- 作製された卵子から体外授精により健常なマウスを得ることに成功
- 卵子形成メカニズムの解明、不妊症の原因究明などに貢献
京都大学 大学院医学研究科の斎藤 通紀 教授と林 克彦 准教授らの研究グループは、マウスで多能性幹細胞であるES細胞注1)とiPS細胞注2)から卵子を作製し、それらの卵子から子供を産み出すことに成功しました。これまで本研究チームは、雄のES細胞やiPS細胞から精子を作製することには成功していましたが、雌のES細胞やiPS細胞から機能的な卵子を作製した成功例は世界でもなく、その技術開発が望まれていました。
本研究グループは今回、雌のマウスのES細胞やiPS細胞を卵子や精子を作る元となる始原生殖細胞注3)に試験管内で分化させて、それらをマウス胎仔の中から取り出した将来の卵巣になる体細胞と共に培養した後に、雌マウスの卵巣に移植することで未成熟卵子注4)を得ました。それらの未成熟卵子を体外培養により受精可能な卵子にまで成熟させた後に、体外受精させることにより健常なマウスを得ました。これらのマウスは正常に成長し、子供を作る能力があることも分かりました。
この技術の開発により、卵子が形成されていくメカニズムの解明に貢献するものと期待されます。また、この技術を応用することで不妊症の原因究明などにも役立つものと期待されます。
本研究成果は、JST 戦略的創造研究推進事業の一環として行われ、2012年10月4日(米国東部時間)に米国科学誌「Science」のオンライン速報版「Science express」で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 ERATO型研究
| 研究プロジェクト |
「斎藤全能性エピゲノムプロジェクト」 |
| 研究総括 |
斎藤 通紀(京都大学 大学院医学研究科 教授) |
| 研究期間 |
平成23年度~平成28年度 |
戦略的創造研究推進事業 個人型研究(さきがけ)
| 研究領域 |
「エピジェネティクスの制御と生命機能」
(研究総括:向井 常博(佐賀大学 名誉教授))
|
| 研究課題名 |
「始原生殖細胞の内因性リプログラミング機構による幹細胞制御」 |
| 研究者 |
林 克彦(京都大学 大学院医学研究科 生体構造医学講座 機能微細形態学 准教授) |
| 研究期間 |
平成23年10月~平成27年3月 |
<研究の背景と経緯>
胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)は生殖細胞を含む体を構成するいずれの細胞にも分化することのできる細胞です。これらの細胞を任意の細胞に分化させる培養技術の開発は、再生医学領域の前進に大きく貢献するばかりでなく、体内では解析が不十分な発生や生理現象を体外培養により再現できることから、発生・細胞・幹細胞生物学分野においても非常に意義の深いものと考えられます。
卵子や精子を生み出す生殖細胞系列は、生体内の細胞系譜の中で唯一次世代に遺伝情報を伝達できる細胞系列であり、その発生異常は不妊や次世代の個体の疾患に深く関わることが知られています。全ての卵子や精子の起源となる細胞は始原生殖細胞と呼ばれ、個体の発生過程の比較的早い段階で分化します。始原生殖細胞はさまざまな発生過程を経て、雌では卵子に雄では精子に分化しますが、その発生過程の多くが胎仔期に行われていることもあり、解明されていない部分が多く残されています。
昨年までに、本研究グループは雄のマウスのES細胞やiPS細胞から始原生殖細胞に類似した始原生殖細胞様細胞(Primordial Germ Cell-like Cells:PGCLCs注5))を試験管内で分化させて、それらをもとに健常な精子と子孫を得ることに成功しました(Cell 2011)。これにより、体外で作製したPGCLCsは機能的な精子まで分化する能力があることが明らかとなりましたが、これらが卵子へ分化できる能力を持つかどうかについては不明でした。本研究グループでは、精子を作製する際に用いたPGCLCsの培養方法を応用して、マウスの雌のES細胞やiPS細胞から卵子を作製する培養技術を開発する研究を進めてきました。
<研究の内容>
本研究では、ES細胞やiPS細胞から試験管内で分化させたPGCLCsから機能的な卵子を作製することを目的として実験を行いました。正常な卵子は雌の始原生殖細胞から生じることが知られているために、まず本研究では新たに雌のES細胞を樹立しました。このES細胞は、始原生殖細胞に発現する遺伝子Blimp1注6)と始原生殖細胞や卵子に発現する遺伝子Stella注7)が発現している場合に、蛍光たんぱく質が発現するように遺伝子(レポーター遺伝子)を改変したマウスから樹立しました。これにより、始原生殖細胞または卵子に分化した細胞は蛍光たんぱく質によって光を発するため、蛍光顕微鏡下で容易に観察できます。このレポーター遺伝子を持つ雌のES細胞から、精子を作製したときと同様の方法で、PGCLCsを分化させました。
これまでの研究により、ES細胞やiPS細胞から試験管内で分化させたPGCLCsは、培養1週間程度で発生を停止することが明らかになっていました。つまり、このままでは卵子まで分化させることは不可能です。そこで、本研究グループはマウス胎仔の中から将来の卵巣になる体細胞(雌生殖巣体細胞注8))を取り出し、ES細胞から分化させた始原生殖細胞と共に培養(凝集培養)しました(図1)。それにより、凝集された細胞塊中のES細胞由来のPGCLCsは増殖を開始しました。また、生体内の始原生殖細胞の発生過程に起こるX染色体の再活性化や刷り込み遺伝子の消去、減数分裂への移行がES細胞由来のPGCLCsで観察されました。これらのことから雌生殖巣体細胞の助けにより、PGCLCsは発生の停止を回避できることが明らかとなりました。
次に、雌生殖巣体細胞とES細胞由来のPGCLCsの細胞凝集を、免疫拒絶反応を起こさない雌のマウスの卵巣被膜下に移植しました。その結果、約4週間後の移植片に未成熟な卵子が多数観察されました(図2)。移植片より採取したこれらの未成熟卵子は、Stellaの発現制御下にある蛍光たんぱく質を発現しており、ES細胞から分化させたPGCLCs由来であることが確認されました。さらに、これらの未成熟卵子を体外培養条件下で卵子を成熟させることにより、受精可能な成熟卵子を得ました。これらの成熟卵子を精子と体外受精させることにより得られた受精卵を仮親の雌マウスに移植した結果、健常なマウスが世界で初めて得られました(図2)。このマウスは正常に発達し、雌雄ともに生殖能力があると確認されました。
上記の研究に加え、雌の胎仔の繊維芽細胞から樹立したiPS細胞から卵子を作製する実験を行いました。実験に用いたiPS細胞はレポーター遺伝子を持たないことから、始原生殖細胞に発現する表面抗原SSEA1とIntegrin-β3を認識する抗体により、iPS細胞から分化させたPGCLCsを採取しました。それらを用いて、ES細胞を用いた場合と同様の凝集培養と雌マウスへの移植を行った結果、受精可能な成熟卵子の作製、健常マウスの取得に世界で初めて成功しました(図3)。
<今後の展開>
本成果は基礎および応用面の双方において大きな効果が期待できます。基礎面においては、始原生殖細胞の発生メカニズムの解明や卵子形成の初期段階の解析が可能になることです。生体内の始原生殖細胞は非常に少数であり、その増殖や分化のメカニズムや、卵子形成の初期段階である減数分裂への移行メカニズムなどに不明な点が数多く残されています。本研究による体外培養技術の開発によって、多数のPGCLCsを容易に作製でき、それらと雌生殖巣体細胞との相互作用を調べることが可能となりました。今後はこの体外培養技術を用いて、始原生殖細胞の増殖や分化のメカニズムや、減数分裂への移行メカニズムを明らかにできると考えられます。
また応用面においては、不妊症の原因究明に効果が期待できます。この体外培養技術では、ES/iPS細胞を起点として、始原生殖細胞から卵子形成の初期段階までの一連の分化過程を追えることから、この培養系を発生モデルとして用いて、始原生殖細胞の発生や卵子の分化・成熟に必要な遺伝子の単離に貢献すると考えられます。これらの遺伝子はヒトの不妊症の原因遺伝子となっている可能性があります。特に、iPS細胞からも卵子を作製できることから、不妊症患者さんからのiPS細胞を用いることにより、疾患原因遺伝子の同定を行うことが可能になると考えられます。しかしながら、本研究はマウスを用いた試験段階であり、マウスとヒトの相違点を考慮すると、応用面での貢献のためには、さらなる基礎研究が必要であると考えられます。また、卵子は生命の根源となる細胞ですので、倫理的な課題を慎重に検討する必要があると考えられます。
<参考図>
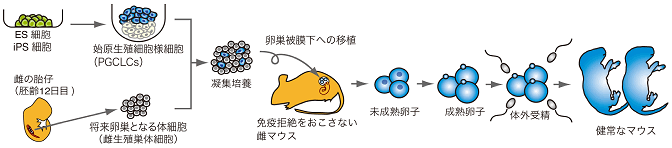
図1 ES/iPS細胞から卵子を作製するための実験手順
ES細胞から分化させたPGCLCsを将来卵巣となる体細胞(雌生殖巣体細胞)と凝集培養を行い、細胞の凝集塊を免疫拒絶のない雌マウスの卵巣被膜下に移植した。約4週間後の移植片から未成熟卵子を取り出し、体外培養により受精可能な成熟卵子まで分化させ、体外受精を行った。得られた受精卵を雌のマウスの卵管に移植することにより健常な個体を得ることに成功した。

図2 ES細胞から分化させたPGCLCs由来の卵子とそれらの体外受精により得られた産仔
- (上左)PGCLCsと雌生殖巣体細胞との凝集塊を移植してから約4週間後の移植片の写真を蛍光顕微鏡写真と合成したもの。移植片の中に蛍光を発する未成熟卵子がいることが観察される。
- (上中左)移植片から採取された未成熟卵子。
- (上中右)未成熟卵子の写真を蛍光顕微鏡写真と合成したもの。青色の蛍光たんぱく質を発現する様子が分かる。
- (上右)体外培養により成熟させた受精可能な成熟卵子。
- (下左)体外受精により得られた産仔。矢印で示した目の黒いものがES細胞由来のもの。
- (下右)得られた産仔は成長し、次世代のマウスを産んだ。
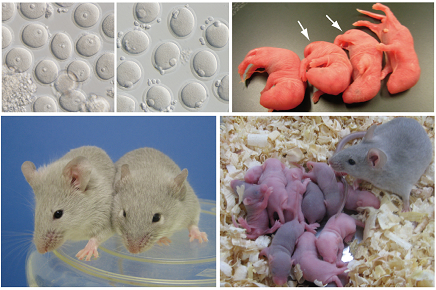
図3 iPS細胞から分化させたPGCLCs由来の卵子とそれらの体外受精により得られた産仔
- (上左)iPS細胞から分化させたPGCLCsと雌生殖巣体細胞との凝集塊を移植してから約4週間後の移植片から採取された未成熟卵子。
- (上中)体外培養により成熟させた受精可能な成熟卵子。
- (上右)成熟卵子の体外受精により得られた産仔。矢印で示したものがiPS細胞由来のもの。
- (下左)得られた産仔は通常のマウスと同様に成長した。
- (下右)成長したiPS細胞由来のマウスは次世代のマウスを産んだ。
<用語解説>
- 注1) ES細胞
- 胚性幹細胞(Embryonic Stem Cells)のこと。マウスの場合は受精後3~4日目の胚盤胞の内部細胞塊から、培養により得られる。体外培養により無限に増殖し、生殖細胞を含むほぼ全ての組織の細胞に分化することができる。
- 注2) iPS細胞
- 人工多能性幹細胞(induced Pluripotent Stem Cells)のこと。皮膚などの体細胞に特定の因子を導入することにより作製される。ES細胞(注1参照)のように、無限に増殖し、生殖細胞を含むほぼ全ての組織に分化することができる。ES細胞と異なり、あらゆる個体の体細胞から作製が可能であり、自家移植により免疫拒絶を起こさない細胞である。
- 注3) 始原生殖細胞
- 全ての卵子もしくは精子の源となる細胞。発生の初期、マウスの場合は胚齢6.5日前後に分化する。発生初期は少数の細胞集団であり、その発生様式に性差はないが、胚齢12日目前後に体細胞の性によって、卵子もしくは精子へと分化することが決定される。
- 注4) 未成熟卵子
- 受精可能な卵子になる前の段階の卵子。卵子は生体内では卵巣の中で受精可能な状態まで成熟してから排卵される。成熟前の卵子は、そのままでは受精する能力がない。
- 注5) PGCLCs
- 始原生殖細胞様細胞(Primordial Germ Cell-like Cells)のこと。ES細胞やiPS細胞から特定の培養条件で分化させた細胞。始原生殖細胞によく似た特徴を持つ。雄の精巣への移植により精子に分化することが知られていた。
- 注6) Blimp1
- 始原生殖細胞の発生に重要なはたらきを持つ遺伝子の1つ。始原生殖細胞の発生の最も初期に発現する。この遺伝子は始原生殖細胞のほかに、免疫細胞などでも重要なはたらきがあることが知られている。
- 注7) Stella
- 始原生殖細胞と卵子に特異的に発現する遺伝子の1つ。その機能は十分に解明されていないが、始原生殖細および未成熟卵子から成熟卵子まで多量に発現している。
- 注8) 雌生殖巣体細胞
- 将来卵巣になる胎仔期の細胞。卵巣は卵子のほかに、卵子の発育を助けるさまざまな細胞により構成されている。卵巣や精巣の原基は胚齢10日目前後に雌雄同様に現われる。12日目前後には卵巣として形態的特徴を持つようになり精巣と区別できる。始原生殖細胞は、胚齢10日前後にこの卵巣もしくは精巣の原基に移動してくる。
<論文名>
“Offspring from Oocytes Derived from in vitro Primordial Germ Cell-like Cells in Mice”
(体外培養にて得られた始原生殖細胞に由来する卵子からのマウス産出に成功)
doi: 10.1126/science.1226889
<お問い合わせ先>
<研究に関すること>
林 克彦(ハヤシ カツヒコ)
京都大学 大学院医学研究科 生体構造医学講座 機能微細形態学 准教授
〒606-8501 京都府京都市左京区吉田近衛町
Tel:075-753-4335 Fax:075-751-7286
E-mail:
斎藤 通紀(サイトウ ミチノリ)
京都大学 大学院医学研究科 生体構造医学講座 機能微細形態学 教授
〒606-8501 京都府京都市左京区吉田近衛町
Tel:075-753-4335 Fax:075-751-7286
E-mail:
<JSTの事業に関すること>
金子 博之(カネコ ヒロユキ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町ビル
Tel:03-3512-3528 Fax:03-3222-2068