ポイント
- 神経細胞は、脳内のガイダンス因子の誘導を受けながら伸長して神経回路を形成
- 軸索ガイダンス因子セマフォリンが、「樹状突起ガイダンス因子」としても働くことを発見
- セマフォリン受容体の活性抑制で、生体内での樹状突起増加を確認 再生医療への応用に期待
JST 課題達成型基礎研究の一環として、京都大学 大学院生命科学研究科の生沼 泉 助教と田坂 元一 大学院生らは、マウスの大脳皮質において、神経細胞が自身の周辺の「道しるべ」を感知して自らの樹状突起の形と向きを決定していくメカニズムを解明しました。
神経細胞は、1本の長い軸索と複数の複雑に分枝した樹状突起を持っています。軸索は、他の細胞への情報の出力元として、樹状突起は他の細胞からの情報の受け手として働きます。胎児の脳内で神経回路網が形成される際、軸索や樹状突起が的確な位置へ伸びていきシナプス注1)を形成しますが、その際迷子になったり混線したりしないのは、脳内に「軸索ガイダンス因子」という物質が「道しるべ」として働き、軸索の形や向きを変化させるからです。軸索側を制御するガイダンス因子は、20年ほど前からよく研究されてきました。しかし、的確な回路網形成には、軸索だけでなく、樹状突起側の制御も必要ですが、樹状突起側の詳しい制御メカニズムは明らかになっていませんでした。
生沼助教らは今回、マウスの脳で軸索ガイダンス因子の1つであるセマフォリンと結合する受容体たんぱく質「プレキシン注2)」が、樹状突起の形や向きを制御していることを突き止めました。さらに、プレキシンの活性を阻害する分子をマウスの大脳皮質に遺伝子導入したところ、神経細胞の樹状突起の枝分かれを増加させることに成功しました。これまで、セマフォリンがプレキシンを介して、軸索の伸長を阻害することは分かっていましたが、今回、樹状突起の伸長をも阻害することが世界で初めて分かり、さらにはその阻害メカニズムの詳細も明らかになりました。
セマフォリンやプレキシンは線虫からヒトまで、種を超えて存在している重要な分子で、損傷後の神経再生を阻害することが知られています。今回の成果により、損傷神経細胞の神経突起の再生誘導への応用が期待されます。
本研究成果は、2012年6月12日(米国東部時間)発行の米国神経科学学会雑誌「The Jounal of Neuroscience」に掲載されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 個人型研究(さきがけ)
| 研究領域 |
「脳神経回路の形成・動作と制御」
(研究総括:村上 富士夫 大阪大学 大学院生命機能研究科 教授)
|
| 研究課題名 |
「ガイダンス因子シグナルで普遍的に駆動されるシグナル伝達経路の解明」 |
| 研究代表者 |
生沼 泉(京都大学 大学院生命科学研究科 助教) |
| 研究期間 |
平成23年10月~平成27年3月 |
JSTはこの領域で、脳の統合的理解を目指し、新たな視点に立って脳を構成する神経回路の形成やその動作原理、並びにその制御機構の解明に挑戦する研究を対象としています。上記研究課題では、複雑でありながら的確に構築される脳神経回路がどのような機構で形成されるかという問題に対して、神経細胞自身が周辺の環境情報を感知し、その情報を統合しています。最終的な目的の細胞に到達するに至るメカニズムを明らかにすることで、脳地図が形成されていく仕組みを解明し、脳の疾患の病因解明や治療法の開発の足がかりとしていきます。
<研究の背景と経緯>
学習や記憶といった高次脳機能を可能としているのは、神経細胞が神経突起を伸長し、お互いにシナプスを築くことによって形成される複雑な神経回路です。これまで解剖学的な研究により、多くの神経回路のパターンが分かってきました。しかし、それらの形成機構に関する分子レベルの研究は近年、始まったばかりです。脳神経系の構成単位である神経細胞は特異的な極性を持ち、通常は1本の長い軸索と複数の複雑に分枝した樹状突起を細胞体から伸展しています(図1)。神経細胞間の情報伝達は軸索と樹状突起で構築されるシナプスを介して行われます。樹状突起や細胞体で受け取った情報は、細胞体に集約され、軸索を通って隣の神経細胞の樹状突起や細胞体へ神経伝達物質が放出されることによって伝わります。複雑で正確な神経回路網を形成するために、神経細胞はさまざまな制御を受けており、その中の1つに軸索ガイダンス因子による誘導作用があります。これまでに、神経軸索はさまざまな軸索ガイダンス因子に導かれて伸長し、目的のターゲット細胞へと投射しシナプス形成をすることが分かってきました。軸索ガイダンス因子は、誘引作用(こちらに伸長して来い)を示す誘引性ガイダンス因子と、反発作用(こちらに伸長して来るな)を示す反発性ガイダンス因子とに大きく分けられ、誘引作用を示すガイダンス因子の方向に神経軸索は伸長していき、反発作用を示すガイダンス因子があると、軸索がそれを遠ざけるようにして伸長することが分かっています(図2)。これまでに軸索ガイダンス因子の軸索に対する作用メカニズムはとても良く研究されており、軸索内の細胞膜供給や細胞骨格(図3)を変化させることによって、形や向きの変化を引き起こすことが分かっていました。一方、的確な回路網形成には軸索と樹状突起の双方の制御が必要です。しかし、神経細胞がその周辺の因子を感知して自らの樹状突起の形や向きの変化を引き起こすメカニズムは明らかではなく、樹状突起の細胞骨格系の制御メカニズム自体も謎でした。
<研究の内容>
生沼助教らはこれまでに、ラットやマウスの脳から取り出して培養した神経細胞(初代培養神経細胞)や、マウス胎仔の生体の脳内への簡便な遺伝子導入法などを用いることにより、反発性ガイダンス因子「セマフォリン」が神経細胞に対して反発作用を示すメカニズムに関して明らかにしてきました。例えば、軸索にセマフォリンの刺激が入ると、受容体のプレキシンを介してRasファミリー低分子量Gたんぱく質注3)であるR-Rasを抑制し、軸索の伸長を阻害していることを明らかにしてきました(図4)。
本研究では、これまで軸索での研究が進んでいた「軸索」ガイダンス因子、セマフォリンおよびその受容体プレキシンが、樹状突起の向きや形を変化させる「樹状突起ガイダンス」における作用を検討し、そのメカニズムを世界で初めて明らかにしました。
ラット胎児の大脳皮質から未熟な神経細胞を取り出して培養皿の上で培養すると、培養後5日目には複雑に枝分かれされた、樹状突起が形成されます。その細胞に、セマフォリン刺激を90分間与えると、従来多くの研究者によって観察されていた軸索の退縮だけでなく、樹状突起の枝の部分も退縮して短くなっていました。そこで、この退縮反応には樹状突起内の何らかの細胞骨格系の変化を伴うと考え、細胞骨格系の1つであるアクチン骨格を蛍光染色して共焦点レーザ顕微鏡で観察してみました。その結果、セマフォリンの刺激によってアクチン骨格が樹状突起の先から消えてなくなっていることが分かりました(図5)。さらに、これらの樹状突起の枝の退縮やアクチン骨格の消失は、Rasファミリー低分子量Gたんぱく質であるM-Ras(エム・ラス)を常に活性化した神経細胞では、阻止できました。(図5)。つまり、セマフォリンの刺激によりプレキシンがM-Rasの活性を抑制することで、樹状突起のアクチン骨格が消えることを示しており、軸索の場合のR-Rasを抑制した阻害とは、別のメカニズムであることが分かりました。
では、プレキシンによってM-Rasの活性が抑制されるとなぜ、樹状突起内のアクチン骨格の崩壊が引き起こされるのでしょうか。生沼助教らは、生化学的な結合実験や細胞染色によって、M-Rasが、アクチン骨格の安定化に関わっているラメリポディン(Lamellipodin:Lpd)というたんぱく質に結合し、それを樹状突起の先端の細胞膜へ運ぶことを明らかにしました(図6)。セマフォリンがない状態ではM-Rasが運ぶラメリポディンによって、樹状突起先端のアクチン骨格系の伸長が促されます。一方、セマフォリンが存在すると、受容体のプレキシンによってM-Rasが不活性化され、ラメリポディンが樹状突起の先端へ運ばれなくなり、アクチン骨格系の伸長が抑制されるということが分かりました(図7)。
培養皿の上で培養した大脳皮質由来神経細胞に対しては、上記のようなメカニズムが明らかになったので、実際の脳内で検討しました。大脳皮質内に存在する神経細胞である錐体細胞は、脳内では樹状突起を脳の外側(上方向)に向かってあまり枝分かれさせることなく、整然と伸ばしています。また、セマフォリンはこれまでの報告により、大脳皮質において外側ほど多く存在していることが分かっていました(図8)。このことから、セマフォリンが大脳皮質の外側の部分で、樹状突起の枝分かれを抑制していると予想されます。そこで、プレキシンの細胞内領域に直接結合してプレキシンの活性をブロックすることができる分子を作って、マウスの大脳皮質に遺伝子導入したところ、樹状突起の枝の本数の著しい増加と向きの乱れが観察されました(図9)。また、同様の形と向きの変化は、M-Rasの活性型を遺伝子導入したり、ラメリポディンの活性型を遺伝子導入することによっても観察されました。これらの結果から、セマフォリンープレキシンのシグナルは、実際のマウスの脳内においても、M-Rasやラメリポディンの活性を抑制することによって、樹状突起の形や向きを制御する「樹状突起ガイダンス因子」として働いていることが明らかになりました。
<今後の展開>
軸索ガイダンス因子セマフォリンが、アクチン骨格系の制御を介して「樹状突起ガイダンス因子」としても働くというメカニズムは、これまで全く知られていなかった世界初のメカニズムです。今回の樹状突起に関する成果および、従来からの研究で明らかになっている軸索に関する知見を併せれば、セマフォリンはその受容体であるプレキシンを介して、神経細胞の軸索および樹状突起の双方の伸長に対して阻害的に働くということになります。
セマフォリンおよびその受容体プレキシンは線虫からヒトまで、種を超えて存在している重要な分子で、これまでの知見により、それらは神経損傷時の神経突起の枝分かれや伸長といった神経再生に阻害的に働くことが知られています。また、セマフォリンおよびその受容体プレキシンは脳以外にも、幅広い組織にあって、血管の枝分かれの形成においても阻害的に働くことが知られている物質です。本研究グループが作出したプレキシンの細胞内領域に直接結合してプレキシンの活性を生体内でブロックすることができる分子は、損傷神経細胞の神経突起や血管の再生誘導への応用が可能であると考えられることから、本研究成果は、神経科学分野のみならず、広範囲の生命科学分野や医学生物学分野にも貢献するものと期待されます。
<付記>
本研究は、京都大学 大学院生命科学研究科の根岸 学 教授の協力を得て行いました。
<参考図>
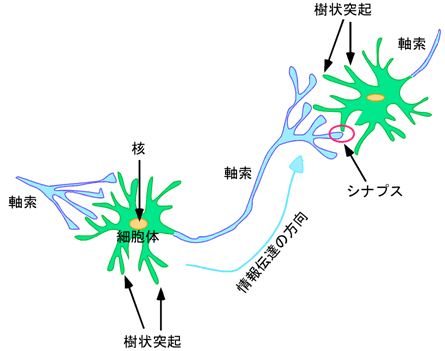
図1 神経細胞の構造
脳神経系の構成単位である神経細胞は、通常は1本の長い軸索と複数の複雑に枝分かれした樹状突起を細胞体から伸展している。神経細胞間の情報伝達は軸索と樹状突起で構成されるシナプスを介して行われていく。
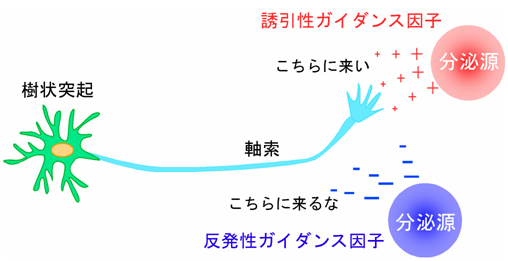
図2 軸索ガイダンス因子の軸索誘導作用
神経細胞の軸索は目的の細胞に到達するために、周囲に存在する軸索ガイダンス因子をたよりに方向を決定している。ガイダンス因子には、誘引性(こちらに来い)の作用を示すものと、反発性(こちらに来るな)の作用を示すものがある。
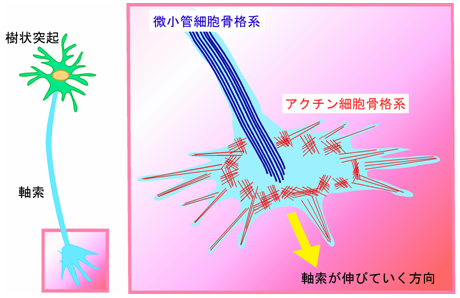
図3 軸索の細胞骨格系
軸索は、微小管細胞骨格系やアクチン細胞骨格系によって、形作られている。
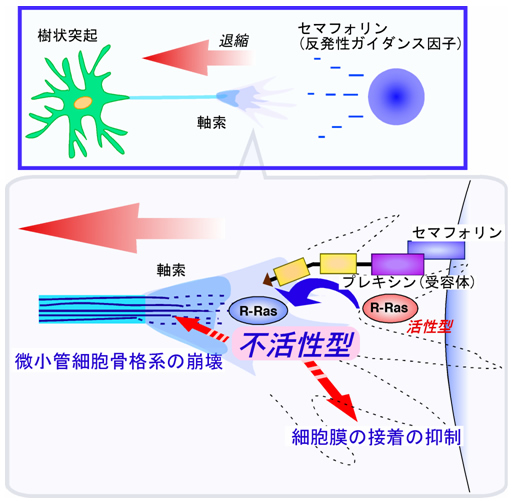
図4 セマフォリンによる軸索の退縮の作用機序
軸索において、セマフォリンは、軸索に発現している受容体のプレキシンを活性化する。これにより微小管細胞骨格系が崩壊し、細胞膜接着が抑制され、軸索の退縮が起こる。
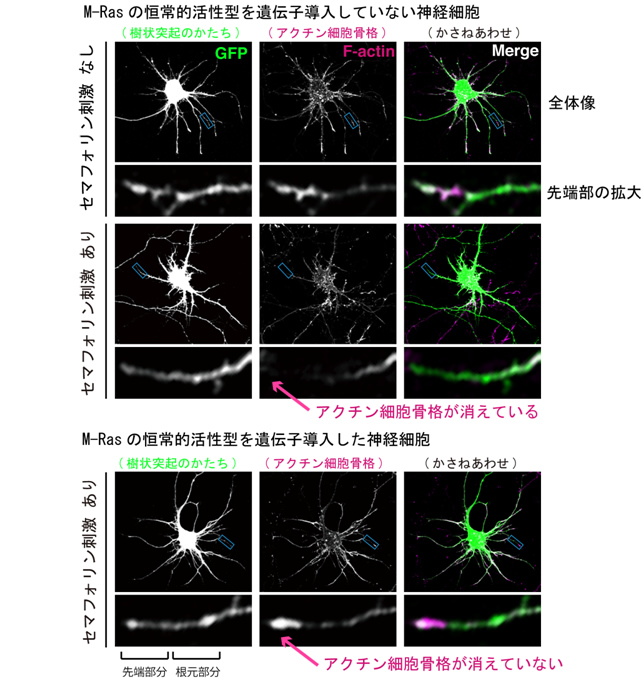
図5 セマフォリン刺激による樹状突起先端のアクチン骨格の消失
- (上段)セマフォリン刺激を与えない場合。アクチンが樹状突起の先端部分に見られる。
- (中段)セマフォリン刺激を与えた場合。樹状突起の先端にアクチンが見られない。樹状突起の枝自体の長さも縮んでいる。
- (下段)恒常的活性型M-Rasを遺伝子導入した神経細胞。セマフォリン刺激を与えても、樹状突起の枝は短くならないし、先端からアクチンがなくならない。神経細胞の形を確認するために同時にGFP遺伝子を導入して検出した。左列、中列の画像は見やすさのため白黒加工してある。
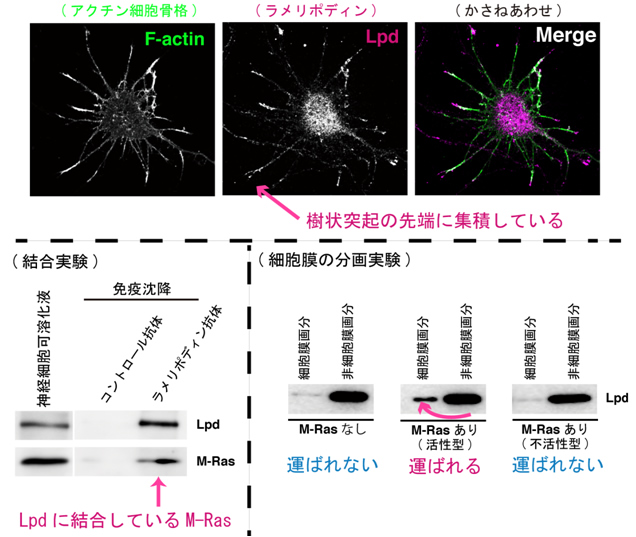
図6 ラメリポディンはM-Rasと結合し、樹状突起先端の膜に運ばれる
- (上段)樹状突起の先端部分にラメリポディンが集積している。
- (下段左)神経細胞を可溶化し結合実験を行った。ラメリポディンとM-Rasは神経細胞内で、結合している。
- (下段右)細胞膜の分画実験を行った。活性型M-Rasを遺伝子導入すると、ラメリポディンが細胞膜へ運ばれる。
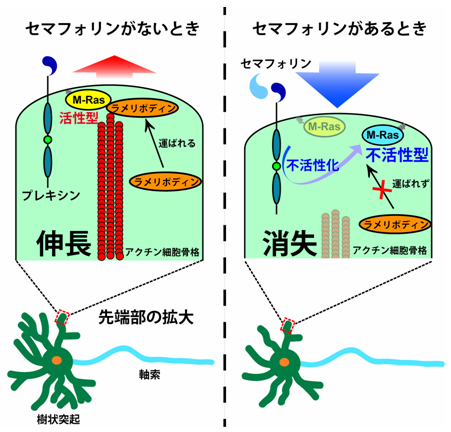
図7 セマフォリンによる樹状突起の退縮のメカニズム
- (左)セマフォリンがないときには、プレキシンは活性化されていないため、樹状突起内部のM-Rasの活性は高く、アクチン細胞骨格の伸長に促進的に関わる分子であるラメリポディンは、樹状突起の先端部に運ばれ、結果としてアクチン細胞骨格の伸長が可能となる。
- (右)一方で、セマフォリン刺激が入ると、プレキシンが活性化され、樹状突起内のM-Rasが不活性化されるため、ラメリポディンは樹状突起の先端部に運ばれない。結果として、アクチン細胞骨格の消失が起こり、樹状突起が退縮する。
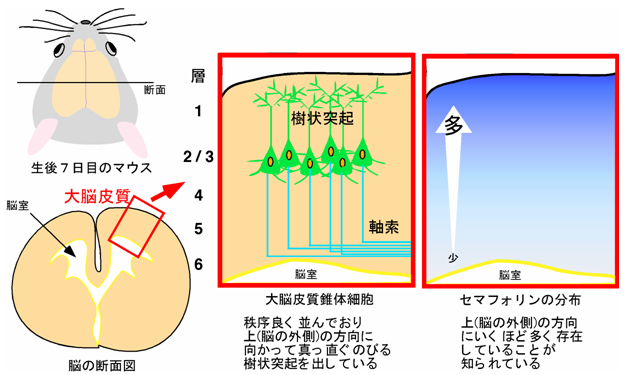
図8 哺乳類の大脳皮質の様子
マウスの大脳皮質(図は生後7日目のマウスの大脳皮質の模式図)の断面で見られる、錐体細胞の様子。錐体細胞は脳内で秩序良く並んでいる。また、セマフォリンの分布には大脳皮質内で勾配があることが知られている。
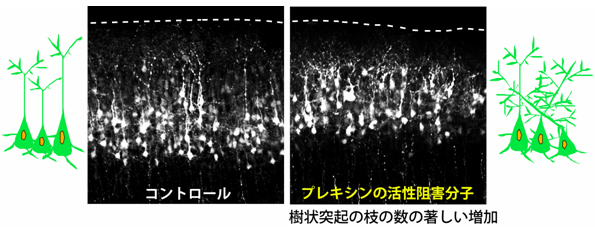
図9 プレキシンの活性阻害分子のマウス生体内への遺伝子導入
- (左)大脳皮質において、錐体細胞は内側から外側に向けて秩序良く並んでいる。
- (右)プレキシンの活性阻害分子をマウス生体の大脳皮質に遺伝子導入すると、樹状突起の枝の本数の著しい増加と、向きの乱れが引き起こされた。M-Rasやラメリポディンの活性型の導入でも、同様の効果が観察された。
<用語説明>
- 注1) シナプス
-
ニューロン間の接合部を指す。シナプスは次の神経細胞と密着しているのではなく、シナプス間隙と呼ばれるすき間を持つ。シナプスでは、軸索を伝ってきた電気信号を神経伝達物質と呼ばれる化学物質の信号に変えてそれを放出することで、次の神経細胞に伝えている。
- 注2) プレキシン
- 軸索ガイダンス因子セマフォリンの受容体である。細胞膜1回貫通型受容体であり、広範な組織で発現している。ヒトにおいては、AタイプからDタイプまでの4タイプが存在するが、それらは全て、Rasファミリー低分子量Gたんぱく質の活性を抑制することが知られている。
- 注3) Rasファミリー低分子量Gたんぱく質
低分子量のたんぱく質で、グアノシン3リン酸(GTP)を結合し、加水分解してGDP(グアノシン2リン酸)とし、さらにそのGDPをGTPに交換することで、細胞内シグナル伝達のスイッチ機能を担う。代表的なものに、がん遺伝子ras(ラス)の産物があることから、Rasスーパーファミリーと呼ばれる。GDP/GTP交換たんぱく質(GEF:ゲフ)およびGTPアーゼ活性化たんぱく質(GAP:ギャップ)による調節を受けながら、GTPとGDPが結合した状態がそれぞれ、オン/オフに相当することで、生体内分子スイッチとして機能しているたんぱく質である。
もともとRasファミリー低分子量Gたんぱく質は、がん遺伝子ras(ラス)の産物として研究されてきた背景から、細胞の増殖やがん化に関する情報伝達は良く研究されており、それに関与するさまざまな特異的エフェクター(直接結合する下流分子)も同定されている。しかし、Rasファミリー低分子量Gたんぱく質が、正常な神経細胞において細胞骨格系を変化させるための下流分子は、全く謎だった。M-RasはRasファミリー低分子量Gたんぱく質の一員であり、アクチン細胞骨格系の制御たんぱく質であるラメリポディンはとても新奇なエフェクターである。
<論文名>
“Semaphorin 4D/Plexin-B1-mediated M-Ras GAP activity regulates actin-based dendrite remodeling through Lamellipodin”
(セマフォリン4D-プレキシンB1によるM-Rasギャップ活性は、ラメリポディンを介してアクチン骨格依存的な樹状突起形態の制御を行う)
doi: 10.1523/JNEUROSCI.0799-12.2012
<お問い合わせ先>
<研究に関すること>
生沼 泉(オイヌマ イズミ)
京都大学 大学院生命科学研究科 生体システム学分野 助教
〒606-8501 京都府京都市左京区吉田近衛町 京都大学医学部構内 医学・生命科学総合研究棟1F
Tel:075-753-7687 Fax:075-753-7688
E-mail:
ホームページ:http://sakura.canvas.ne.jp/spr/izumi_presto/
<JSTの事業に関すること>
原口 亮治(ハラグチ リョウジ)、木村 文治(キムラ フミハル)、眞後 俊幸(シンゴ トシユキ)
科学技術振興機構 戦略研究推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2063
E-mail: