慶應義塾大学 先端医科学研究所 遺伝子制御研究部門(責任者:佐谷 秀行 教授)の永野 修(ながの おさむ) 専任講師、八戸 敏史(やえ としふみ) 研究員らの研究グループは、慶應義塾大学 医学部 医化学教室(責任者:末松 誠 教授)、東京大学 先端科学技術研究センターの油谷 浩幸 教授、南 敬 教授、順天堂大学 呼吸器内科教室の高橋 和久 教授らとの多施設共同研究によって、癌幹細胞表面マーカーである接着分子CD44が癌細胞の酸化ストレス注1)抵抗性を高めることによって、乳癌細胞の肺転移を促進する分子機構について解明しました。
今回の研究成果をもとに、転移性乳癌細胞を標的とした新たな治療法の開発が期待できます。この研究成果は英国科学専門誌「Nature Communications」オンライン版に2012年6月6日(英国時間)に掲載されます。
1.研究の背景と目的
癌幹細胞は腫瘍組織形成の大本になる細胞であり、治療に対する抵抗性が高いことから、癌の再発、転移などの起源になると考えられています。乳癌、膵臓癌、胃癌、大腸癌などの固形癌注2)においては、CD44陽性の癌細胞は免疫不全マウスでの腫瘍形成能力が高く、CD44陽性の癌細胞は癌幹細胞様の性質を持つことが報告されてきました。また、これまでの報告から、様々な固形癌におけるCD44のバリアントアイソフォーム(CD44v)注3)の発現は、遠隔転移と相関していることが知られていました。慶應義塾大学 医学部の研究チームは、CD44vがシスチントランスポーターxCT注4)の発現を上昇させ、抗酸化物質である還元型グルタチオン(GSH)の合成を促進することで、癌細胞における酸化ストレス抵抗性を高め、腫瘍の増大や治療抵抗性に寄与することを以前報告しています(Cancer Cell 19: 387-400, 2011.2011年3月9日に慶應義塾大学・科学技術振興機構からプレスリリース)。そこで今回、永野専任講師らは、CD44vが転移の過程で癌細胞が受ける酸化ストレスを抑えることにより転移を促進するのではないかと考え、その分子メカニズムの解明に向けて本研究に取り組みました。
2.主要な研究成果
今回の発表は、癌幹細胞の主要な表面マーカーの一つであるCD44を介した酸化ストレス抑制機構が、乳癌の肺への転移を促進することを明らかにしたものです。これらの知見は、CD44を高発現する転移性乳癌細胞を標的にした治療法の確立に繋がる大きな可能性を秘めています。
3.研究方法と研究成果の意義
まず、高転移性のマウス乳癌細胞株4T1細胞と、4T1細胞と同一の遺伝子背景を有する低転移性あるいは非転移性の乳癌細胞株(4TO7細胞、168FARN細胞、67NR細胞)を用いて、CD44vの発現を確認しました。その結果、高転移性である4T1細胞のみCD44vのmRNA注5)が多く作られていることが分かりました。そこで、細胞膜表面におけるCD44vの発現についてフローサイトメトリー注6)を用いて検出したところ、4T1細胞のみが、CD44vを高く発現していることが分かりました。さらに4T1細胞は、CD44v陽性細胞と、CD44v陰性でCD44スタンダードフォーム注7)(CD44s)陽性細胞の2種類の細胞画分に分離出来ることを見出だしました。そこで、CD44v陽性細胞およびCD44v陰性(CD44s陽性)細胞をそれぞれマウス乳腺へ同所移植した後に、肺への転移の有無や転移巣の大きさについて検討したところ、両群とも原発巣注8)の大きさについては、ほとんど変わらないものの、肺転移能はCD44v陰性細胞に比べて、CD44v陽性細胞で明らかに高いことが分かりました。
これまでの研究でCD44vは、癌細胞の細胞膜表面においてxCTを安定化させることで細胞外からのシスチンの取り込み量を増加させ、細胞内の主要な抗酸化物質であるGSHの生成を促進することを見出しています。そこで、肺転移巣におけるCD44v陽性細胞のGSH量を質量分析イメージング法により検討したところ、CD44vを高発現する肺転移巣では明らかにGSHが多く含まれていることが分かりました(図1)。
さらに、CD44 mRNAの選択的スプライシング注9)の制御因子であるESRP1タンパク質の発現を、RNA干渉法(RNAi)注10)を用いて抑制すると、xCTの細胞表面における発現および細胞内GSH含有量は著明に低下し、その結果、CD44v陽性4T1細胞の肺転移を著明に抑制できることが分かりました(図2)。また、xCTに対し特異的に阻害作用を示すことが知られているスルファサラジン(既存薬)によっても同様に肺転移を抑制できることなどから、ESRP1タンパク質によって促進されるCD44vの発現は、xCTの細胞膜における発現を上昇させることで抗酸化物質GSHの合成を促進し、乳癌細胞が転移の過程で受ける酸化ストレスに対して抵抗性を高め、転移を促進することが分かりました。
次に転移性乳癌細胞におけるESRP1の発現制御機構について調べました。これまでに上皮-間葉転換(EMT)注11)はESRP1の発現低下を誘導することが知られていました。そこでEMTマーカーの発現についてCD44v陽性4T1細胞とCD44v陰性細胞について検討したところ、ほとんど両者には差が無かったことから、EMT以外の機構でESRP1の発現が制御されていると考えました。近年、エピジェネティック注12)な制御機構、特にヒストン修飾注13)が選択的スプライシングの制御に重要であることが発表されていますので、ESRP1のエピジェネティックな制御機構について検討したところ、CD44v陽性4T1細胞とCD44v陰性細胞のESRP1の発現にはESRP1遺伝子座のヒストン修飾の変化が関連していることが分かりました。これらのことから、転移性乳癌細胞におけるESRP1およびCD44vの発現制御には、EMTよりも、むしろヒストン修飾によるエピジェネティックな発現制御機構が重要であると考えられました。
これらの結果から、CD44を介した酸化ストレス抑制機構は、腫瘍の増大や治療に対する抵抗性のみならず、癌の転移にも寄与していることが分かりました(図3)。本研究によって、CD44vの発現が高い癌においてはCD44vやxCTを標的とした治療を行うことで、癌幹細胞および転移性乳癌細胞を標的とした治療法を開発できる可能性が示されました。また、ESRP1のエピジェネティック制御という新たなCD44v発現制御機構の解明は、転移性乳癌細胞に対する治療の新規標的分子の発見に繋がることが予想され、癌転移治療薬開発において大変重要な意義を持つと考えられます。
4.今後の展開
xCTに対し特異的に阻害作用を示すことが知られている既存薬(スルファサラジン)を用いた動物実験により、有意な腫瘍抑制効果、抗癌剤感受性増強効果が得られています。現在、慶應義塾大学 医学部の研究グループは、スルファサラジンを用いた医師主導型第一相臨床治験を国立がん研究センター 東病院らと共同で実施すべく、計画を進めています。
5.特記すべき事項
今回のプロジェクトは、日本の異なった専門的知識と技能を持つ各分野のトップクラスの研究グループが、それらを結集することによって完成した研究成果であり、共同研究の相乗効果なしには到底為し得なかったと考えます。近年、領域を超えた多数のチームが、互いの力を融合させることによって成果を上げることが望まれていますが、その良い実例を示すことができたと思っています。
本研究は、JST 戦略的創造研究推進事業 チーム型研究(CREST)の研究課題「人工癌幹細胞を用いた分化制御異常解析と癌創薬研究」(研究代表者:佐谷 秀行)、および同事業、総括実施型研究(ERATO)「末松ガスバイオロジープロジェクト」(研究総括:末松 誠)、ならびに文部科学省 次世代がん研究戦略推進プロジェクト「酸化ストレス回避機構を標的とした癌幹細胞治療戦略の考案」(研究代表者:永野 修)における研究の一環として行われました。
<参考図>
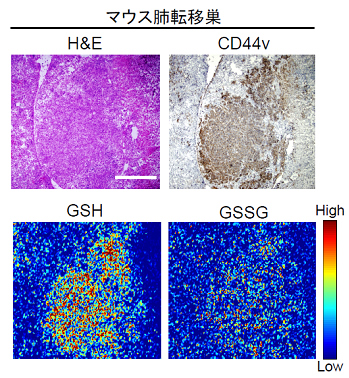
図1 マウス肺転移巣におけるCD44v発現とGSHの質量分析イメージング像
CD44vを高発現するマウス肺転移巣では、酸化型グルタチオン(GSSG)と比較して明らかに、還元型グルタチオン(GSH)が高く検出される。H&E:ヘマトキシリン・エオジン染色像。
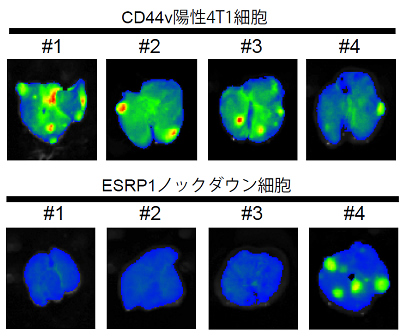
図2 マウス肺転移巣のイメージング
ESRP1の発現をノックダウン(抑制)することにより、高転移性であるCD44v陽性細胞による肺転移を著明に抑えることができた。それぞれ異なるマウス(#1~4)の肺の蛍光イメージング画像。ESRP1の発現をノックダウンした4T1細胞を同所移植したマウス肺では、蛍光シグナルが抑えられており、肺転移が抑制されていることが分かる。
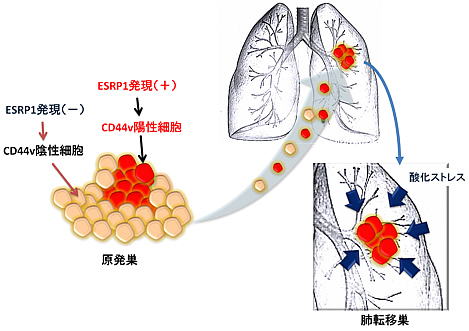
図3 CD44v陽性乳癌細胞の肺転移メカニズム
ESRP1の発現によってCD44vが陽性となった癌細胞は酸化ストレスを抑制する能力が高く、治療に対して抵抗性を示す細胞である。これらの細胞は転移の際に生じる酸化ストレスに対しても抵抗性を発揮し、転移巣の成立と拡大に関与する。
6.論文について
“Alternative splicing of CD44 mRNA by ESRP1 enhances lung colonization of metastatic cancer cell.”
[ESRP1を介したCD44 mRNAの選択的スプライシングは転移性癌細胞による肺転移巣の形成を促進する]
Yae T, Tsuchihashi K, Ishimoto T, Motohara T, Yoshikawa M, Yoshida GJ, Wada T, Masuko T, Mogushi K, Tanaka H, Osawa T, Kanki Y, Minami T, Aburatani H, Ohmura M, Kubo A, Suematsu M, Takahashi K, Saya H and Nagano O. Nat. Commun . 2012 (in press)
doi: 10.1038/ncomms1892
<用語解説>
- 注1) 酸化ストレス
- 生体の酸化反応と抗酸化反応のバランスが崩れた結果、過剰な酸化反応により生体に有害な作用が生じる状態。
- 注2) 固形癌
- 白血病のような血液の癌を除く癌のこと。
- 注3) CD44のバリアントアイソフォーム(CD44v)
- 接着分子CD44には、mRNAの選択的スプライシング(注9参照)により多種類の産物ができることが知られている。CD44vはそのうち癌組織で高発現するアイソフォーム(若干異なる構造を持つタンパク質)。
- 注4) シスチントランスポーターxCT
- アミノ酸の一つであるシスチンを細胞内に取り込むために必要なトランスポーターを構成するタンパク質。
- 注5) mRNA
- DNAから転写され、タンパク質に翻訳され得る塩基配列情報と構造を持ったリボ核酸。
- 注6) フローサイトメトリー
- 試料中の細胞の数や特徴(大きさ、形状、細胞表面のタンパク質発現の有無など)を計測するための分析手法。
- 注7) CD44スタンダードフォーム
- CD44バリアント領域を含まないアイソフォーム。
- 注8) 原発巣
- 転移巣に対して、最初に癌が発生した部位のこと。
- 注9) 選択的スプライシング
- DNAから転写されたmRNAが成熟する過程で、同一遺伝子から異なる組み合わせでエクソン(塩基配列中で成熟mRNAに残る部分)を結合したmRNA分子が生成され、遺伝子産物に多様性が増す機構。
- 注10) RNA干渉法(RNAi)
- 標的とするタンパク質のmRNA発現を特異的に抑制する方法。
- 注11) 上皮-間葉転換(EMT)
- 上皮系細胞が上皮としての特性を失い、周辺組織に移動しやすい間葉系細胞としての特徴を獲得する現象。
- 注12) エピジェネティック
- 真核生物においてDNAはヒストンと呼ばれるタンパク質に巻きついた構造をしており、このDNA-タンパク質複合体のことをクロマチンと呼ぶ。そのクロマチンへの修飾(DNA塩基のメチル化やヒストンの化学修飾など)により、遺伝子発現が後天的に制御されること。
- 注13) ヒストン修飾
- クロマチンを構成するヒストンタンパク質はアセチル化、メチル化、リン酸化といった様々な翻訳後修飾を受けることが知られており、これらのヒストン修飾はクロマチンの構造変化を引き起こし、その結果、遺伝子発現を変化させることが知られる。
<問い合わせ先>
慶應義塾大学 医学部 先端医科学研究所 遺伝子制御研究部門 永野 修、佐谷 秀行
〒160-8582 東京都新宿区信濃町35
TEL:03-5363-3982 FAX:03-5363-3982
E-mail:
ホームページ:http://genereg.jp/index.html
<本リリースの発信元>
慶應義塾大学 信濃町キャンパス 総務課(冨田、吉野)
TEL:03-5363-3611 FAX:03-5363-3612
E-mail:
ホームページ:http://www.med.keio.ac.jp/
科学技術振興機構 広報課
〒102-8666 東京都千代田区四番町5番地3
TEL:03-5214-8404 FAX:03-5214-8432
E-mail: