本研究成果のポイント
- グルタミンやアスパラギンに富むアミノ酸配列を持たない酵母プリオン「Mod5」を同定
- Mod5の凝集で、出芽酵母が抗真菌剤に対する抵抗性を獲得
- プリオン病に対する新たな治療・対処戦略や、抗菌剤の開発・応用にも道を開く
独立行政法人 理化学研究所(野依 良治 理事長)は、出芽酵母注1)を用いた実験により、プリオンタンパク質注2)が凝集し、その凝集体が細胞間や個体間を伝わることが、酵母の抗真菌剤に対する抵抗性獲得に重要であることを発見しました。これは理研 脳科学総合研究センター(利根川 進 センター長)タンパク質構造疾患研究チームの鈴木 元治郎 研究員、嶋津 直之 テクニカルスタッフ(当時)、田中 元雅 チームリーダーの研究による成果です。
哺乳動物のプリオン病注3)は、プリオンタンパク質が凝集して引き起こされると考えられています。近年、プリオン病の1つである狂牛病が、種の壁を超えてヒトへ感染し、BSE問題として脅威を与えました。プリオン病の感染は、ウイルスなどではなく、凝集したプリオンタンパク質によって引き起こされ、それが細胞間や個体間を伝わっていくためと考えられています。プリオン病研究のモデル生物として広く利用されている出芽酵母では、哺乳動物のプリオンタンパク質と同様に凝集するタンパク質が7個知られており、「酵母プリオン注4)」と呼ばれています。酵母プリオンの研究が進む中で、プリオンタンパク質の凝集は、病原因子という負の側面だけでなく、生物の生存や進化に有利に働いている可能性が示唆されています。しかし、具体的な報告はほとんどありませんでした。
研究チームは、出芽酵母の約6,000の遺伝子を探索し、新たな酵母プリオン「Mod5注5)」を同定しました。既知の7個の酵母プリオンには、凝集体を形成しやすいグルタミンやアスパラギンに富むアミノ酸配列がありますが、Mod5にはそうした配列がありませんでした。さらに、Mod5の凝集により出芽酵母は抗真菌剤に対する抵抗性を獲得すること、また、その性質を利用して環境ストレスに素早く適応することも分かりました。これらのことから、病原因子として認識されていたプリオンタンパク質の凝集が、生物の生存に有利に働くことを見いだしました。
哺乳動物のプリオンタンパク質も、グルタミンやアスパラギンに富むアミノ酸配列を持ちません。従って、Mod5の詳細な解析は哺乳動物のプリオン病の感染・発症メカニズムの解明に役立ちます。また、医療・農業などの現場で問題となっている薬剤耐性菌の発生メカニズムの解明や、抗菌剤の開発・応用にも貢献すると期待できます。
本研究成果は、最先端・次世代研究開発支援プログラム、JST さきがけ研究(「代謝と機能制御」領域)などの支援を受けて行われたもので、米国の科学雑誌『Science 』の4月20日号に掲載されます。
1.背景
神経変性疾患の1つであるクロイツフェルト・ヤコブ病や、2000年代初頭にBSE問題として大きな社会問題となった脳がスポンジ状になる狂牛病は、脳内でプリオンタンパク質が凝集して発症するプリオン病の一種です。プリオン病が感染するときは、細胞内で凝集し不溶性になったプリオンタンパク質が鋳型となって、正常な可溶性のタンパク質を自らと同じ凝集体に変換し、その凝集体が細胞間および個体間を伝わっていくと考えられています。また、出芽酵母では、哺乳動物のプリオンタンパク質と同様に凝集する「酵母プリオン」が7個知られていることから、プリオン病研究のモデルとしてプリオンタンパク質の凝集や伝播メカニズムの解明に多大な貢献をしてきました。2010年に研究チームは、酵母プリオンの1つであるSup35タンパク質を用いて、プリオンタンパク質の凝集メカニズムを解明しました(2010年1月18日プレスリリース:http://www.riken.jp/r-world/info/release/press/2010/100118/index.html)。
2008年、酵母プリオンの研究から、プリオンタンパク質の凝集が遺伝子発現を制御していることが報告されました。つまり、プリオンタンパク質は病原因子となって細胞や個体に不利に働くだけでなく、生物の生存や進化に有利に働いている可能性が示唆されてきました。しかし、具体的な例はほとんど報告されておらず、プリオンタンパク質凝集体の積極的な機能については、謎のままでした。
そこで研究チームは、新たな酵母プリオンを同定し、凝集したプリオンタンパク質が担う新たな機能の解明に挑みました。
2.研究手法と成果
まず、新たな酵母プリオンを同定するために、タンパク質の共凝集注6)という現象を利用した方法で、出芽酵母の約6,000の遺伝子を探索しました。その結果、プリオンタンパク質の候補を65個同定しました。既知の7個の酵母プリオンは、アミロイド注7)と呼ばれる線維状凝集体を形成しやすいグルタミンやアスパラギンに富むアミノ酸配列を持っています。候補の中にあった「Mod5」というタンパク質は、そのような配列を持たないにも関わらず、Mod5の溶液をゆっくりとかき混ぜると、線維状凝集体へ構造が変化することを発見しました(図1)。
この線維状凝集体を野生型の出芽酵母に導入したところ、導入前は細胞質全体に広がっていたMod5が、導入後は凝集体を形成し、細胞分裂後も安定的に伝播することが分かりました。既知の7個の酵母プリオンは、分子シャペロン注8)の1つであるHsp104タンパク質注9)を機能阻害すると、凝集体の伝播能力を喪失することが知られています。Mod5の凝集体を形成している酵母のHsp104遺伝子を破壊したところ、凝集体は元のように細胞質全体に広がり、伝播能力が喪失したことを確認しました。これらのことから、Mod5は新たな酵母プリオンであることが判明し、Mod5が凝集している酵母を[MOD +]酵母と名付けました(図2)。
[MOD +]酵母を詳しく調べると、凝集したMod5は、タンパク質の合成に関与する転移RNAの修飾といった本来の機能が低下していることが分かりました。また、[MOD +]酵母は、野生型酵母に比べて多くのエルゴステロールを含有していることも見いだしました。エルゴステロールは、酵母などの真菌類の細胞膜を構成する物質で、動物の細胞におけるコレステロールと同様な働きをします。動物には存在しないため、抗真菌剤の標的として知られています。そこで、抗真菌剤存在下で野生型と[MOD +]酵母を培養したところ、野生型は増殖できませんが、[MOD +]酵母は増殖できることが分かりました(図3A)。また、[MOD +]酵母の出現頻度は抗真菌剤存在下で上昇し、非存在下では出現しないこと(図3B)、抗真菌剤存在下では[MOD +]酵母の割合が増加するが、非存在下では野生型酵母の割合が増加することも発見しました(図3C)。
哺乳動物のプリオンタンパク質は、グルタミンやアスパラギンに富むアミノ酸配列を持っていません。今回、哺乳動物と同様に、そうした配列を持たない初めての酵母プリオンMod5を同定することができました。また、Mod5が凝集すると、細胞内のエルゴステロール量が増加し、抗真菌剤耐性を獲得するという、細胞の新たな薬剤耐性獲得メカニズムを発見しました。さらに、生物は自らの生存維持を図るため、プリオンタンパク質の凝集と非凝集状態を種々の環境変化に応じて素早く使い分ける、という新たな生存戦略を明らかにしました(図4)。
3.今後の期待
酵母プリオンMod5の発見は、酵母プリオンと哺乳動物のプリオンタンパク質との類似性を高める結果となり、プリオン病の感染・発症メカニズムの解明とその治療法の開発に大きく貢献すると期待できます。また、医療・農業の分野で薬剤耐性菌の出現は大きな問題となっていますが、薬剤耐性にプリオンタンパク質の凝集が関与するという知見は、感染症に対する新たな治療・対処戦略の開発にも道を開きます。さらに、環境ストレスに応じて凝集を制御するという事実は、プリオンタンパク質が、細胞の機能や生物の進化に関わっていることを示しています。プリオンタンパク質の理解は、生命科学のさまざまな分野の発展に幅広く貢献すると期待できます。
<原論文情報>
Suzuki, G. Shimazu, N., and Tanaka, M. “A Yeast Prion, Mod 5, Promotes Acquired Drug Resistance for Cell Survival under Environmental Stress.” Science, 2012,doi: 10.1126/science.1219491
<付記>
本成果は、一部、JST さきがけ研究領域「代謝と機能制御」研究課題名:「プリオン凝集体の代謝産物に着目した細胞機能制御」研究者:田中 元雅(理化学研究所 脳科学総合研究センター タンパク質構造疾患研究チーム チームリーダー)によって得られたものです。
<参考図>
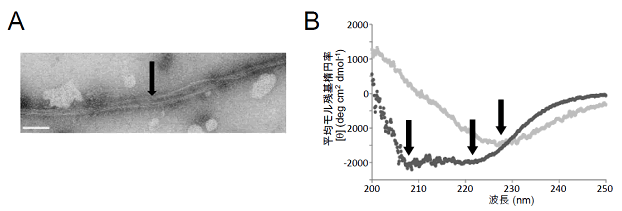
図1 Mod5タンパク質の線維状凝集体の形成
大腸菌でMod5遺伝子を発現させ、精製したMod5タンパク質含有溶液を穏やかにかき混ぜて、凝集体を形成させた。
-
(A)Mod5凝集体の電子顕微鏡画像。
線維状の凝集体(矢印)が確認できる。スケールバーは100nm。
-
(B)遠紫外円偏光二色性スペクトル。
Mod5の凝集前(黒)と凝集後(グレー)。タンパク質の構造変化がスペクトルの変化として示されている。凝集前はα-へリックスを示す208nmと222nm付近に負のピーク(矢印)が存在するが、凝集後はアミロイドに特徴的なβ-シートを示す227nm付近に負のピーク(矢印)が存在する。
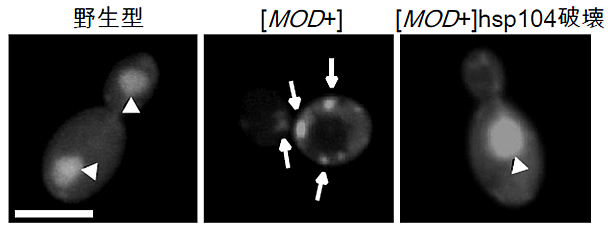
図2 [MOD +]酵母内のMod5タンパク質の局在
野生型、[MOD +]、[MOD +]Hsp104遺伝子破壊酵母それぞれにおいて、Mod5を蛍光タンパク質で標識し、細胞内局在の様子を観察した。野生型では細胞内全体と核(白矢頭)に存在するが、[MOD +]酵母では細胞質に凝集体を形成していることが分かる(白矢印)。しかし、Hsp104遺伝子を破壊すると、野生型と同様の局在に戻る。スケールバーは5μm。
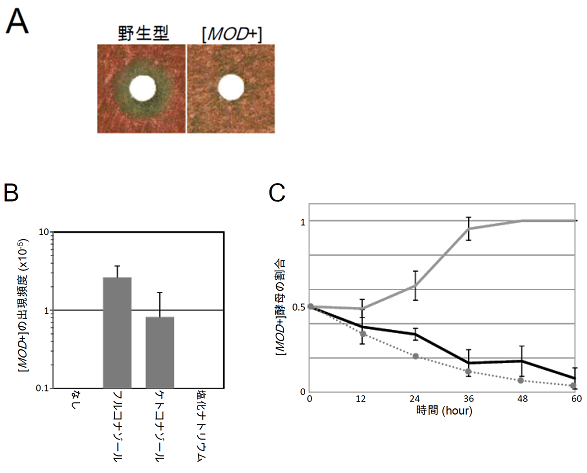
図3 [MOD +]酵母の抗真菌剤に対する応答
- A:野生型と[MOD +]酵母の抗真菌剤耐性。
抗真菌剤の一種であるフルコナゾールを染み込ませた丸い濾(ろ)紙を酵母細胞上に置き、抗真菌剤への耐性を調べた。野生型では濾紙の周りに酵母が増殖できない領域がドーナツ状にできたが、[MOD +]酵母は濾紙の周りでも増殖できた。
-
B:抗真菌剤存在下における[MOD +]酵母の出現頻度。
抗真菌剤であるフルコナゾール、ケトコナゾールを含む培地で培養すると、[MOD +]酵母の出現頻度が上昇するが、抗真菌剤の非存在下や、非特異的なストレス誘導剤である高濃度の塩化ナトリウムを含む培地では上昇しない。
-
C:抗真菌剤存在下における[MOD +]酵母の増殖優位性。
野生型酵母と[MOD +]酵母を等量に混ぜて、フルコナゾール存在下(グレー)と非存在下(黒)で[MOD +]酵母の割合がどのように変化するかを調べた。フルコナゾール存在下では、[MOD +]酵母の割合が上昇し、36時間後にはほぼ[MOD +]酵母になる。一方、フルコナゾール非存在下では[MOD +]酵母の割合が徐々に減少し、60時間後にはほぼ野生型酵母になる。非存在下での[MOD +]酵母の減少は、[MOD +]酵母と野生型酵母の細胞分裂の速度の違いから計算される理論値とほぼ一致する(点線)。
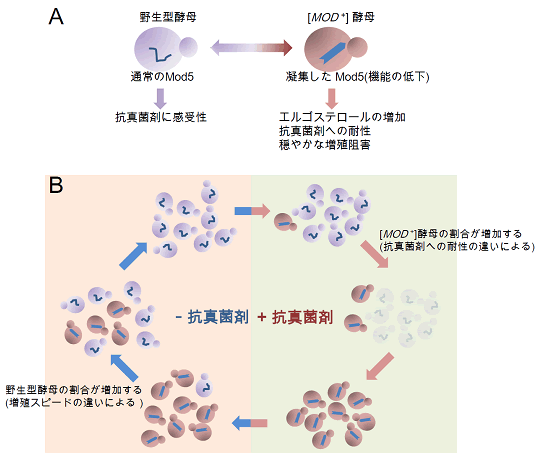
図4 プリオンタンパク質の凝集による環境変化への迅速な応答
- A:野生型酵母から[MOD +]酵母への変換は非常に低い割合で起きると考えられる。
-
B:抗真菌剤非存在下では野生型酵母が増殖の優位性を持っているので、ほぼ全てが野生型酵母となる。抗真菌剤存在下では、プリオン化した酵母が増殖の優位性を持つが、ストレスから解放されると、野生型酵母が優位性を持つようになる。
こうして、ゲノム変異を伴わないプリオンタンパク質の構造変換によって、刻々と変化する周辺の環境に迅速に適応できると考えられる。
<補足説明>
- 注1) 出芽酵母
- 出芽酵母は出芽により増殖する酵母の総称であるが、今回の研究では出芽酵母の一種Saccharomyces cerevisiae を利用している。出芽酵母は酒類やパンの製造などに工業的に利用されているだけでなく、真核生物のモデル生物として、細胞レベルの事象の研究に広く利用されている。
- 注2) プリオンタンパク質
- プリオンとはタンパク質からなる遺伝因子のことであり、プリオンを構成するタンパク質のことをプリオンタンパク質と呼ぶ。哺乳動物では、狂牛病などの原因となる哺乳動物プリオンタンパク質(PrP)が、出芽酵母では、Sup35やUre2といったタンパク質がプリオンタンパク質として知られている。
- 注3) プリオン病
- 認知力低下を伴う神経変性疾患の1つであり、代表的なものにクロイツフェルト・ヤコブ病(CJD)がある。プリオン病の原因は、プリオンタンパク質が脳内で凝集するためと考えられている。発症率は百万人に1人程度だが、近年の狂牛病の牛肉を食したことで、種の壁を越えてヒトへ感染し発症する新型CJDが人類に脅威を与えている。
- 注4) 酵母プリオン
- 哺乳動物のプリオンタンパク質と相同性はないものの、酵母の中にもプリオンのような振る舞いを示すタンパク質が7個知られている(2011年時点)。それらのタンパク質を酵母プリオンと総称し、プリオンの概念が哺乳動物以外のタンパク質にも拡張されている。
- 注5) Mod5
- 転移RNAのアンチコドン37位にあるアデノシンをイソペンテニル化修飾する酵素。種を超えて広く保存されているタンパク質であり、哺乳動物には、酵母のMod5にアミノ酸配列が類似した、TRIT1というタンパク質がある。
- 注6) 共凝集
- あるタンパク質の凝集体が鋳型となって、別のタンパク質の凝集が促進され、凝集体を形成すること。酵母プリオンの多くは、その凝集体が、別の酵母プリオンの凝集を促進することが知られている。
- 注7) アミロイド
- βシート構造に富んだタンパク質凝集体。電子顕微鏡などによる観察で、直径4~10nmからなる繊維状の構造体を示す。一般に、βシート構造による強固な規則正しい構造をとっているため、その規則的な構造がタンパク質の構造変化の鋳型となっている。βシート構造が集合すると、アルツハイマー病などの神経変性疾患が発症するといわれている。
- 注8) 分子シャペロン
- タンパク質は正常に働くためには正しく折り畳まれるフォールディングが必要である。これを助ける一群のタンパク質が、分子シャペロンと呼ばれ、熱ショックなどで誘導される。タンパク質の凝集・分解を防ぎ、活性制御にも関与する。
- 注9) Hsp104タンパク質
- 分子シャペロンの1つであり、細胞内のタンパク質凝集体を分解する。プリオンタンパク質が凝集した酵母内で、Hsp104タンパク質の機能を薬剤や遺伝学的操作で阻害すると、凝集体が細胞分裂の際に伝播するのに必要な小さいサイズまで断片化されなくなり、凝集体を持った酵母は凝集体を持たない酵母へ転換すると考えられている。
<報道担当・問い合わせ先>
(問い合わせ先)
理化学研究所 脳科学総合研究センター タンパク質構造疾患研究チーム
田中 元雅(タナカ モトマサ) チームリーダー
Tel:048-467-6072 Fax:048-462-4796
理化学研究所 脳科学研究推進部 企画課
入江 真理子(イリエ マリコ)
Tel:048-467-9757 Fax:048-467-4914
(報道担当)
理化学研究所 広報室 報道担当
Tel:048-467-9272 Fax:048-462-4715
科学技術振興機構 広報課
Tel:03-5214-8404 Fax:03-5214-8432