JST 課題達成型基礎研究の一環として、東京医科歯科大学 大学院医歯学総合研究科の高柳 広 教授と林 幹人 研究員らの研究グループは、Semaphorin 3A(セマフォリン スリー エー:Sema3A)注1)と呼ばれるたんぱく質が骨の健康を守り、このたんぱく質をマウスに投与すると骨が増加することを発見しました。
骨は硬く安定した組織に見えますが、その中には骨を作る骨芽細胞注2)、骨を壊す破骨細胞注3)とリンパ球など免疫細胞が存在し、皮膚などと同じように新陳代謝を繰り返しており、古くなった骨が破壊され新たな骨が形成されることで、丈夫さやしなやかさが維持されています。健康な状態では、骨の破壊(骨吸収と呼ばれる)と形成(骨形成と呼ばれる)の2つの作用のバランスは均衡しており、骨の量は一定に保たれていますが、加齢や閉経などの要因でこのバランスが崩れると骨粗しょう症などの疾患に陥ってしまいます。現在、骨粗しょう症の治療では、骨の吸収を抑える薬剤が主に使用されていますが、この場合、骨形成も同時に抑制されてしまうことがあり、吸収・形成の双方をバランスよく制御し、骨量を回復させる薬剤・治療法の開発が望まれています。そこで、このような骨の新陳代謝を担っている、骨に含まれる細胞(骨芽細胞、破骨細胞や免疫細胞)の相互作用のしくみを解明することが治療方法の開発に非常に重要です。
本研究グループは、これまで神経細胞が回路を作る過程や、免疫細胞であるT細胞の抑制などに関わることで知られていた「Sema3A」というたんぱく質が、骨芽細胞から産生され、骨芽細胞自身と破骨細胞の両者に働きかけることにより、骨吸収の抑制と骨形成の促進という2つの作用を持つことをマウスにおいて明らかにしました。
Sema3Aの機能を失ったマウスでは、骨吸収が促進するとともに骨形成が低下して骨量が異常に低下していました。また、骨を物理的に傷つけその再生過程を検証する骨再生モデルマウスや、骨粗しょう症モデルマウスにSema3Aたんぱく質を投与すると、骨の減少を食い止め、骨の再生を促進することができ、症状が改善されました。このように、骨吸収の抑制と骨形成の促進とを同時に行うたんぱく質はこれまで見つかっておらず、壊れた骨をバランスよく回復させる手段はこれまでありません。今回の発見により、骨粗しょう症や骨折、関節リウマチなどの新しい治療法の開発につながることが期待されます。また、老化して骨量が低下傾向にあるマウスでは、血中のSema3Aたんぱく質量が低下していることも観察でき、疾患診断バイオマーカーとしても利用できる可能性も示すことができました。
本研究成果は、大阪大学 大学院医学系研究科、札幌医科大学 医学部附属フロンティア医学研究所、東京大学 先端科学技術研究センターなどの研究グループとの共同研究で得られ、2012年4月18日18時(英国時間)に英国科学誌「Nature」のオンライン速報版で公開されます。
本成果は、以下の事業・研究プロジェクトによって得られました。
戦略的創造研究推進事業 ERATO型研究
| 研究プロジェクト |
「高柳オステオネットワークプロジェクト」
|
| 研究総括 |
高柳 広(東京医科歯科大学 大学院医歯学総合研究科 教授) |
| 研究期間 |
平成21~26年度 |
JSTはこのプロジェクトで、脊椎動物の生体系を「骨を中心とした全身制御システム=オステオネットワーク」として捉えて、その解明を進め、基礎生物学および臨床医学に貢献する研究を行っています。
<研究の背景と経緯>
超高齢社会である日本において、骨粗しょう症患者は推計1300万人(骨粗しょう症の予防と治療ガイドライン作成委員会/編(2011年)より)を超え、予備軍を含めると2000万人と言われており、増加の一途をたどっています。骨粗しょう症は骨質と骨密度の低下により骨の強度が低下し、骨折しやすくなる状態を引き起こします。この結果引き起こされる大腿骨頸部や椎骨の骨折は、寝たきり状態や慢性腰痛の原因となり、QOL(生活の質)を低下させ死亡率を高めることが知られています。健康寿命の延長と周囲の介護負担の軽減が重要課題ですが、その実現にも暗い影を落としています。また、関節リウマチも罹患率の高い関節疾患であり(日本では推計70~80万人、厚生労働省2011年6月17日 第5回厚生科学審議会疾病対策部会リウマチ・アレルギー対策委員会議事録より)、進行してしまうと骨・関節の破壊により患者の運動機能は著しく損なわれます。このような疾患に対する治療法の開発は喫緊の課題となっています。
現在、骨の形成を促進させる薬剤はほとんどなく、骨粗しょう症治療薬としては、ビスフォスフォネート製剤など骨吸収を抑えることで骨の減少を防ぐ薬剤が主に使用されていますが、生体内では吸収した骨と同量の骨を新たに形成するという共役機構(カップリング機構注4))があることから、骨の吸収を阻害すると形成も同時に阻害されてしまいます。実際に、骨吸収抑制作用のある薬剤を長期間使用すると、結果的に適切な骨形成までもが抑制され、質の低い骨が蓄積されることで、十分な治療効果が得られないケースが知られています。また、骨形成を促進することで骨を増やす薬剤として、最近、副甲状腺ホルモン製剤が使用され始めましたが、長期的な治療効果については統一した見解は得られていない段階です。一方、これまでの骨研究においては、骨吸収を抑制しつつ、同時に骨形成を促進することが可能な分子は見つかっていませんでした。このため、健康な骨が恒常性を維持するメカニズムを詳細に解明し、骨吸収と骨形成とを同調して制御する生体内の分子を明らかにすることで、新しい薬剤の標的を見出し、効果的な骨疾患の治療薬を開発することが切実に望まれています。
<研究の内容>
本研究グループは、マウスの骨芽細胞から分泌され、破骨細胞の分化を抑制する活性を持つ因子を探索し、プロテオーム解析注5)を駆使することで、骨芽細胞から産生されるSema3Aと呼ばれるたんぱく質が強力な破骨細胞の分化抑制活性を持つことを見出しました。Sema3Aはこれまで、発生段階において神経細胞が軸索を伸ばし回路を作る過程に関わることや、免疫細胞であるT細胞の活性化を抑制すること、樹状細胞がリンパ節へ移動する過程に関わることなどで知られていたたんぱく質です。
解析を進めた結果、Sema3Aは破骨細胞および骨芽細胞双方の分化に重要な役割を持つことが明らかになりました(図1)。すなわち、Sema3Aは(1)破骨細胞および骨芽細胞上に発現するたんぱく質(受容体)「Neuropilin-1(ニューロピリン ワン:Nrp1)」を介して「Plexin-A(プレキシン エー)」に作用し、破骨細胞分化を抑制するとともに骨芽細胞分化を促進すること、(2)破骨細胞分化に関わるシグナルの1つ「ITAM(アイタム)」シグナルを抑制すること、(3)破骨細胞の運動能に関わる「RhoA(ロー エー)」シグナルを抑制し、破骨細胞が骨芽細胞に近づこうとする動きを妨げ、骨芽細胞と接することで誘導される破骨細胞の分化を抑制することを明らかにしました(図2)。また、骨芽細胞内では、Sema3Aは骨芽細胞の分化に重要な働きをする古典的Wnt/β-カテニンシグナル伝達系を介して骨芽細胞の分化を誘導し、骨芽細胞と由来を同じくする脂肪細胞への分化注6)は相対的に抑制されていることも明らかにしました (図2)。これらの結果から、骨芽細胞はSema3Aを産生することによって骨吸収の抑制と骨形成の促進の双方を制御し、適切な骨量を維持していることを明らかにしました。
Sema3AやNrp1遺伝子を破壊したマウスを調べたところ、破骨細胞の数と骨吸収が増えている一方、骨芽細胞の数と骨形成率が異常に低下しており、それに伴って骨髄中の脂肪細胞の数が増え、骨量も著しく減少していることが分かりました。これは、Sema3Aの働きが失われたことで破骨細胞の分化抑制が行われず、さらに骨芽細胞の分化が促進されないためだと考えられます。
さらに、Sema3Aを正常なマウスに静脈注射によって投与すると顕著な骨量増加が認められました。また、骨にドリルで穴を開けてその部位の骨の再生を観察するモデルにおいても、Sema3Aを局所投与することで、より早い骨の再生を誘導できることが分かりました。また、卵巣を摘出する手術を行って骨粗しょう症を発症させたマウスにSema3Aを投与すると、骨吸収抑制と骨形成促進がなされ、骨量の減少を食い止めることができることが分かりました。以上の多様な解析の結果から、Sema3Aは、骨吸収と骨形成の共役(カップリング機構)を生じることなく、破骨細胞分化を抑制すると同時に骨芽細胞分化を促進することが分かり、カップリング機構の影響を受けにくい新たな治療薬のターゲットとなりうることを証明しました(図3)。
さらに、老化して骨量が低下傾向にあるマウスでは、老化の進行に伴い血中のSema3Aたんぱく質量が低下していることも観察でき、骨減少疾病の診断バイオマーカーとしても利用できる可能性も示すことができました。
<今後の展開>
本研究成果により、Sema3Aをはじめとして、Sema3A-Nrp1経路を活性化する治療法が、骨粗しょう症などの骨関連疾患に対して強い治療効果を発揮すると期待されます。実際に、マウスだけでなくヒトの細胞でもSema3Aが同様の作用を発揮することを確認しています。また、これまでの報告から、Sema3Aは破骨細胞・骨芽細胞だけでなく、免疫系の細胞にも作用し、免疫抑制活性を持つことが知られています。関節リウマチは免疫系に異常が生じ、自分の関節を攻撃してしまう病気で、悪化すると重篤な骨破壊につながってしまいますが、Sema3Aはこのような免疫系と骨の両方に異常が生じる疾患の治療に対しても効果がある可能性も考えられます。今回の報告は、国内外の骨代謝学研究の先導的な意義を持つと考えられ、日本における骨疾患研究が一層進展することが期待されます。
<参考図>
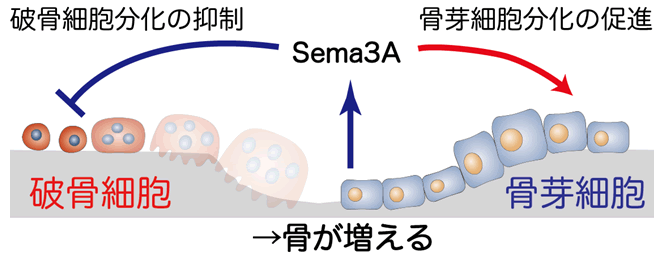
図1 Sema3Aによる骨量増加作用
骨芽細胞が産生するSema3Aが骨芽細胞・破骨細胞の両者に作用して、骨吸収を抑制し、骨形成を促進することで骨が増える。
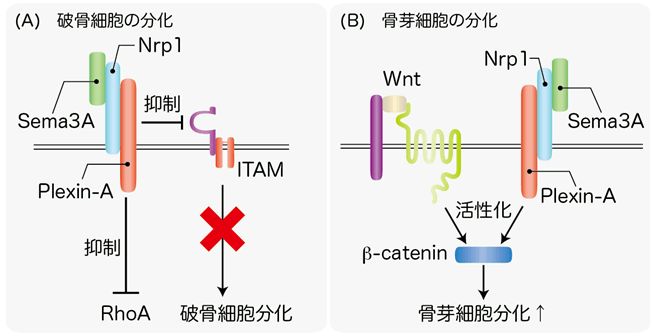
図2 Sema3Aによる骨量増加作用のメカニズム
(A)破骨細胞分化におけるSema3Aシグナル
細胞膜上に発現する受容体Nrp1を介してPlexin-AがSema3Aを認識すると、破骨細胞分化に重要なITAMシグナルを抑制する。また、活性化したPlexin-AはRhoAの活性化を抑制することで、Sema3Aの供給源である骨芽細胞から遠ざけることで間接的にも破骨細胞分化が抑制されると考えられる。
(B)骨芽細胞分化におけるSema3Aシグナル
同様のメカニズムでSema3Aを認識すると、骨芽細胞分化に必須の因子である古典的Wnt/β-カテニンシグナル伝達系の活性化を誘導し、骨芽細胞分化が促進される。
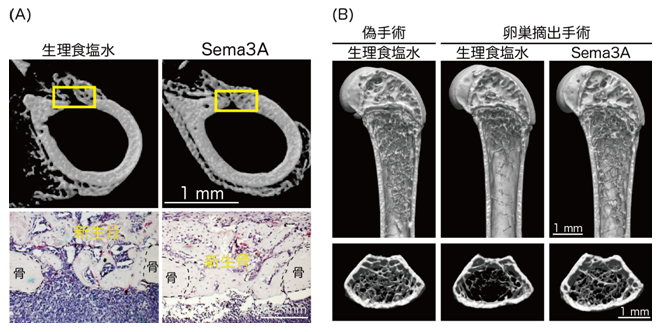
図3 Sema3Aは骨再生を促進する
(A)骨再生モデルにおけるSema3Aの効果
(上段)ドリルによってマウスの骨に穴を開け(写真上段黄色の四角で囲まれた領域)、その部位での骨新生を観察したところ、Sema3Aを局所投与すると著しい骨再生の促進が観察された。(下段)赤く染められた細胞が破骨細胞であるが、Sema3Aを投与したマウスでは骨の再生が促進しており、破骨細胞数が低下していた。
(B)卵巣を摘出したマウスでは、偽手術(卵巣摘出なし/生理食塩水群)を行ったマウスに比べ4週間後に重度の骨粗しょう症を発症する(卵巣摘出術/生理食塩水群)。この骨粗しょう症モデルマウスにSema3Aを投与することにより、骨の減少を抑制した(卵巣摘出術/Sema3A群)。
<用語解説>
- 注1) Semaphorin 3A(セマフォリン スリー エー:Sema3A)
- 「セマフォリン」は、「セマドメイン」と呼ばれる特徴的なアミノ酸配列を持つ分子群のたんぱく質であり、元々は神経細胞軸索の行き先を決める分子として発見された。それぞれのセマフォリンには、特異的に結びつくことができるたんぱく質(受容体)が存在し、細胞と細胞の間での情報伝達因子として働き、神経細胞の軸索が伸びる過程に作用することが知られていた。Sema3Aは分泌型のたんぱく質で、Nrp1を介してPlexin-Aを活性化することで、細胞内に情報を伝達する。これまでの知見で、Sema3Aは免疫系の抑制などにも関与することが分かっている。
- 注2) 骨芽細胞(こつがさいぼう)
- 骨の表面に存在し、新しい骨のもととなるたんぱく質を産生・分泌し、カルシウムなどの沈着を誘導する細胞。この一連の過程を「骨形成」と呼ぶ。
- 注3) 破骨細胞(はこつさいぼう)
- 骨の表面に存在し、古くなった骨基質を溶解して破壊する細胞。複数の細胞が融合したもので多数の核を持つ。骨を溶解する物質を放出して分解し、その分解産物を吸収することで、古い骨を破壊する。この一連の過程を「骨吸収」と呼ぶ。骨吸収がおこった箇所では、骨芽細胞により新しい骨が形成される。
- 注4) カップリング機構
- 吸収した骨と同量の骨を新たに形成するために、骨吸収がきっかけとなって骨形成が開始される仕組み。
- 注5) プロテオーム解析
- プロテオームは、特定の細胞や組織で発現している全てのたんぱく質を指す。プロテオーム解析とは、さまざまな方法によって細胞から採取・分離したたんぱく質の質量を分析し、数理解析することで、どのような構造や機能を持つたんぱく質が含まれるかを網羅的に解析する方法。
- 注6) 骨芽細胞と脂肪細胞の分化
- 骨芽細胞と脂肪細胞は共通の前駆細胞である間葉系幹細胞から分化誘導されることが分かっており、老化や閉経後骨粗しょう症の状態では、骨芽細胞分化や骨形成が低下し、逆に骨髄の脂肪細胞の顕著な増加が見られる。
<論文名>
“ Osteoprotection by Semaphorin 3A ”
(Semaphorin 3Aによる骨保護)
Mikihito Hayashi, Tomoki Nakashima, Masahiko Taniguchi, Tatsuhiko Kodama, Atsushi Kumanogoh and Hiroshi Takayanagi
doi: 10.1038/nature11000
<お問い合わせ先>
<研究に関すること>
高柳 広(タカヤナギ ヒロシ)
東京医科歯科大学 大学院医歯学総合研究科 分子情報伝達学 教授
〒113-8549 東京都文京区湯島1-5-45
Tel:03-5803-5471 Fax:03-5803-0192
E-mail:
研究室ホームページ http://osteoimmunology.com/
高柳オステオネットワークプロジェクトホームページ http://osteonetwork.jp/
<JSTの事業に関すること>
金子 博之(カネコ ヒロユキ)
科学技術振興機構 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町ビル
Tel:03-3512-3528 Fax:03-3222-2068
E-mail: