東京大学 大学院理学系研究科の黒田 真也 教授らは、モデルと実験を用いた解析によって、シグナル伝達注1)分子の分解や不活性化などの負の制御注2)機構が感受性変化負の制御機構が感受性変化を制御していることを見いだした。
抗がん剤などの薬剤の濃度と、これに対する細胞の応答の強さとの関係は「感受性」と呼ばれ、薬剤の作用を知るうえで重要な指標として利用されている。しかし、この感受性がどのような仕組みにより調節されているかについてはこれまで不明であった。例えば、ある濃度の薬剤が標的分子を十分に阻害できても、細胞の応答を十分に阻害するためには、より高い濃度の薬剤が必要になる場合がある。
今回の解析によって、薬剤により、標的分子を十分に阻害できても、最終的な応答は必ずしも十分に抑制できないことが明らかになった。この原理の発見は、薬剤応答の予測や創薬デザインなどに役立つことが期待される。
本研究は、JST 戦略的創造研究推進事業 チーム型研究(CREST)「生命システムの動作原理と基盤技術」研究領域(研究総括:中西 重忠 (財)大阪バイオサイエンス研究所 所長)における研究課題「シグナル伝達機構の情報コーディング」(研究代表者:黒田 真也)の一環として、同校 大学院理学系研究科 生物化学専攻 博士課程の豊島 有 氏、同校 大学院新領域創成科学研究科 情報生命科学専攻 修士課程の角田 裕晶 氏と共に行われた。
本研究成果は、2012年3月13日(英国時間)発行の「Nature Communications」に掲載される予定である。
<研究の内容>
1.これまでの研究で分かっていた点
細胞外のホルモンや成長因子などの刺激の情報は、シグナル伝達経路を介して細胞内へ伝わり、細胞の応答を引き起こす。シグナル伝達経路は多数の分子(シグナル分子)の連鎖的な生化学反応によって構成され、上流分子による下流分子の活性化を通じて、情報を下流へ伝える。
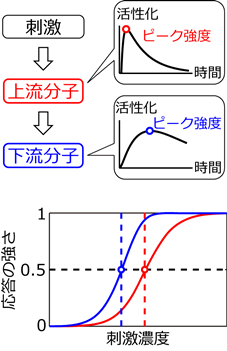
ある刺激に対して特定の分子が応答するとき、分子の活性化時間パターンの最大値(ピーク強度)は応答の強さの指標としてよく用いられる(図1上段)。また一般に、刺激が強いほどシグナル分子の応答も強くなると考えられており、最大応答の50%の応答を引き起こす刺激濃度はその分子の感受性の指標となる(図1下段)。この濃度が小さいことは、より微量の刺激で十分な応答が起きることを意味するので、その分子は刺激感受性が高いといえる。また、シグナル伝達経路の阻害剤は抗がん剤などとして利用されており、阻害剤に対するシグナル分子の感受性は阻害剤の効果の指標の1つとなっている。つまり、感受性が強いほど阻害剤が効果的であることを意味している。しかしこの感受性がどのような仕組みによって決定されているかは不明であった。
また、多くの生化学反応は逐次一次反応注3)という基本的構成要素を含んでおり、逐次一次反応の持つ特性は多くの生化学反応に当てはまることが期待される。黒田教授らは以前の研究において、逐次一次反応を介して信号が伝達されるとき、上流分子のピーク強度が同じ場合でも、上流分子の時間パターンによってピーク強度の伝達効率が異なるために、下流分子のピーク強度が変化するという現象を見いだした(図2)。つまり、上流の信号が強いほど下流分子も強く応答するという、従来信じられていた暗黙的な概念が間違っていることが分かった。しかし、上流分子の時間パターンとピーク強度の伝達効率の定量的な関係や、その関係の一般性については不明のままであった。
2.この研究が新しく明らかにしようとした点
刺激濃度を変えると上流分子の時間パターンが変わる場合には、下流分子へのピーク強度の伝達効率も刺激濃度に応じて変化し、上流分子と下流分子とで感受性に違いが生じる可能性がある。まず、上流分子の時間パターンや逐次一次反応の特性とピーク強度の伝達効率との定量的な関係を詳しく調べることにした。次に、この定量的な関係に対する刺激濃度の影響を調べることで、刺激感受性の変化やその仕組みを明らかにすることを目指した。さらに、刺激のかわりに阻害剤を用いて、阻害剤感受性の変化についても調べた。
3.方法、およびこの研究で得られた結果、知見
①負の制御によるピーク強度の伝達効率の減衰
まず、逐次一次反応を含むシグナル伝達経路の簡単な数理モデルを作成してシミュレーションを行った。その結果、上流信号の時間パターンの時定数注4)が経路の時定数より小さいとき、ピーク強度の伝達効率が減衰することを見いだし、その関係式を導いた(図3実線)。経路の時定数は経路の負の制御の強さによって決まるため、経路の負の制御がピーク強度の伝達効率に影響していることが分かった。
この減衰特性の理論的予測を実証するため、複数種類の培養細胞に対し、刺激を様々な濃度で投与して、多数のシグナル伝達経路の分子の活性化の時間パターンを測定した。これらの実験データから、測定した110経路のうち49経路では逐次一次反応の特性が強く表れていることが分かった。さらに、これらの経路では伝達効率の実測値と理論値が一致していた(図3)。このようにして、減衰特性の実証とともに、この減衰特性が細胞の種類や刺激の種類によらず、多くのシグナル伝達経路で生じていること(一般性)を示すことができた。
②負の制御による刺激感受性の向上
刺激濃度を変えたシミュレーションの結果、刺激濃度が高くなると上流信号の時間パターンの時定数が小さくなり、ピーク強度の伝達効率が減衰することが分かった。つまり、上流分子が最大応答を示すような高い刺激濃度のときよりも、50%の応答を示す刺激濃度のときの方が伝達効率は高くなっていた(図4中段)。その結果、上流分子が50%の応答を示す刺激濃度でも、下流分子は50%以上の応答を示し、下流分子が50%の応答を示す刺激濃度(図4下段、青点)は上流分子が50%の応答を示す刺激濃度(赤点)よりも低くなって、感受性が向上した。
またシグナル伝達経路の負の制御(逐次一次反応の分解反応)が弱いほど経路の時定数が大きくなるため、伝達効率の減衰が強まり、刺激感受性の向上の度合いが強くなることが分かった。シグナル伝達経路は最終的に遺伝子発現へつながるが、遺伝子発現過程では逐次一次反応の特性が強く表れる場合が多いことや、シグナル伝達経路と比べて負の制御が弱いことから、細胞は遺伝子発現の過程を介することで自身の刺激感受性を向上させている可能性が示唆された。
③負の制御による阻害剤感受性の低下
このメカニズムが抗がん剤などの感受性に対してどのように作用しうるかを明らかにするために、上記の数理モデルに阻害剤の効果を組み込んでシミュレーションを行ったところ、刺激濃度を変えたときとは逆に、阻害剤濃度が低いほど、上流信号の時間パターンの時定数が小さくなった。その結果、ピーク強度の伝達効率の減衰のため、阻害剤感受性は経路の下流で低下することが分かった(図5)。つまり、阻害剤が下流分子ほど効きづらくなることが分かった。またシグナル伝達経路の負の制御が弱いほど感受性の変化の度合いが強くなることや、不可逆的阻害剤を用いると感受性が低下しないことが分かった。
この阻害剤感受性の低下を実証するため、細胞のがん化に関与するAkt経路に注目した。Akt経路はEGFという成長因子を受けて活性化し、EGF受容体からAktというシグナル伝達分子を介して、S6という分子まで信号が伝わることが知られている。EGF受容体に対する阻害剤は抗がん剤としても用いられている。この阻害剤をPC12という培養細胞に与え、AktとS6の活性化の様子を測定した。その結果、Aktの下流分子にあたるS6ではAktよりも阻害剤感受性が低くなっていた(図6)。つまり、実際に阻害剤が下流分子ほど効きづらくなることが分かった。こうして、実際の細胞内でも阻害剤感受性の低下が生じていることを実証できた。
4.研究の波及効果
本研究により、シグナル伝達経路の負の制御(図7上)が、ピーク強度の伝達効率の減衰(図7中)を介して、刺激や阻害剤に対する感受性を制御する(図7下)ことが分かった。この刺激感受性や阻害剤感受性を決める基本的な仕組みを考慮することで、薬剤に対する感受性をより正確に予測することが可能になると考えられる。また本研究により、阻害剤の効果は下流へ行くほど弱まることが分かった。新しい抗がん剤を開発する際には、シグナル伝達のもっとも上流にあたる受容体に対する阻害剤が候補となることが多いが、本研究の結果は、このような阻害剤は本質的に細胞の応答を効率よく阻害できない可能性があることを示唆している。また本研究では標的分子に一度結合するとほとんど離れないような不可逆性の強い阻害剤を用いることで、下流における阻害剤感受性の減弱を抑止できる可能性も示唆された。このように本研究の成果は薬剤開発などの分野における活用が期待できる。
5.今後の課題
本研究により、遺伝子発現の過程を介することで、細胞は刺激に対する自身の感受性を増強している可能性が示唆された。また負の制御の強さはたんぱく質分解酵素などの負の調節因子の活性・発現量を反映すると考えられるので、細胞はこのような分子の活性調節を介して、刺激や阻害剤に対する自身の感受性を制御できる可能性がある。これらの知見は今後の研究で検証される必要がある。
6.先行研究との関係について
本研究は、2010年7月28日に黒田教授らが発表した先行研究「細胞内シグナル伝達経路の信号処理特性を解明-薬剤が意図したものと逆の応答を引き起こし得るメカニズムを解明-」の後続研究にあたる。先行研究では、(本研究でも用いた)PC12細胞のAkt経路のみを対象としたが、本研究ではこれに限らず、複数種の培養細胞における多数のシグナル伝達経路(遺伝子発現を介するものも含む)を対象として、伝達効率の減衰特性が細胞内で広くみられる一般的な特性であることを明らかにした。この減衰特性を定量的に扱った点も先行研究と異なる点である。さらに本研究で解析したような刺激感受性や阻害剤感受性は薬剤開発の現場で実際に使われているが、先行研究には含まれていなかった。これらの点で本研究は先行研究から進歩しており、高いインパクトを持っている。
<参考図>
-
図1 (上)シグナル伝達経路と活性化の強さ。
- (下)感受性の定義。青線は赤線より微量の刺激で十分に応答しているので、刺激感受性が高いといえる。
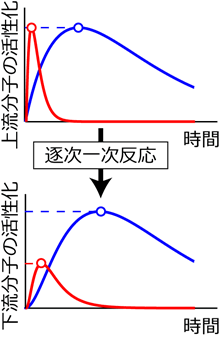
図2 逐次一次反応を介した、上流分子から下流分子への信号の伝達。
赤と青の2つのシグナルについて、上流分子の活性化のピーク強度は同じだが、下流分子の活性化のピーク強度は異なっている。
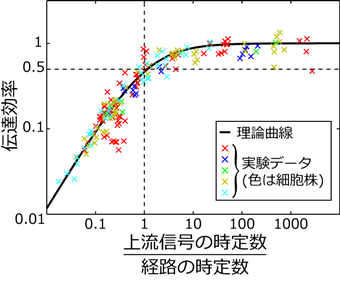
図3 上流信号の時定数が経路の時定数より小さいとき、信号の伝達効率は減衰する。
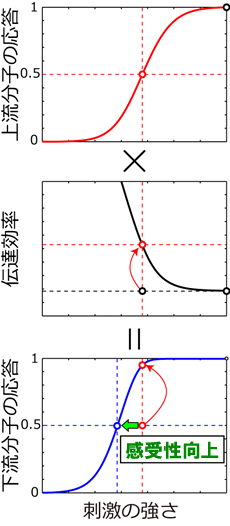
- 図4 (上) 刺激濃度に対する上流分子の応答(実線)と最大の50%の応答を示す刺激濃度(点線)。
- (中) 刺激濃度が高いほど信号の伝達効率は低下する。
-
(下) 下流分子の応答は上流分子の応答と伝達効率のかけ算で表されるため、下流分子が50%の応答を示す刺激濃度(青点線)は小さくなる。このように伝達効率の変化のため下流分子の刺激感受性が向上する。
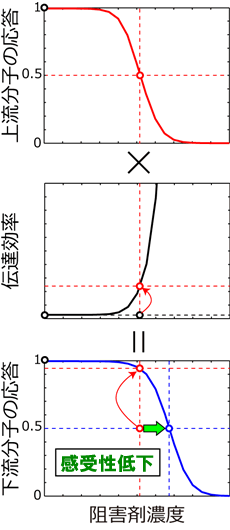
図5 図4とは逆に、阻害剤濃度が高いほど信号の伝達効率が向上するため、下流分子の阻害剤感受性が低下する。
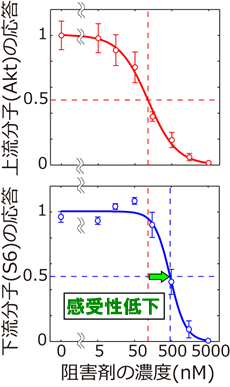
図6 実験によって阻害剤感受性の低下を実証した。
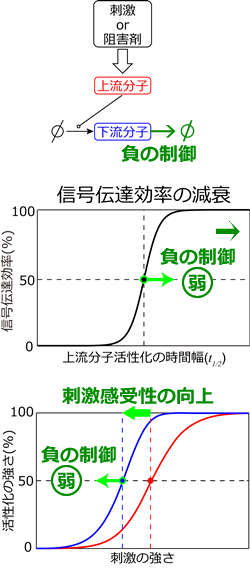
- 図7 (上) シグナル伝達経路の概要。下流分子の分解や不活性化の反応は経路の負の制御に相当する。
- (中) 信号伝達効率は上流分子の活性化の時間幅が小さいほど減衰する。この傾向は経路の負の制御が弱いほど強まる。
-
(下) 経路の負の制御は、信号伝達効率の減衰を介して、刺激や阻害剤に対する感受性を制御する。
<用語解説>
- 注1) シグナル伝達(Signal transduction)
- 細胞外のホルモンや成長因子、栄養などの環境変化の情報は受容体などを介して細胞内に伝わっていき、最終的に細胞の応答を導く。細胞内に情報を伝える経路はシグナル伝達経路と呼ばれ、一般に多数の分子からなる連鎖的な生化学反応によって構成されている。
- 注2) 負の制御(Negative regulation)
- シグナル伝達分子を分解したり不活性化する反応のこと。シグナル伝達分子の合成や活性化(アクセル)とは逆に、信号を抑制するブレーキの役割を果たす。シグナル伝達分子は上流分子により活性化されることで信号を下流へと伝えていくが、正しい信号伝達のためには、負の制御によりシグナル伝達分子を適切に不活性化して、信号強度を適切な範囲に調節することが必要である。実際、負の制御に関わる遺伝子が欠けると細胞ががん化しやすくなることが知られている。また、負の制御が弱いほど経路の時定数が大きくなるので、上流分子の早い変化に対して下流分子が十分追随できなくなり、信号がうまく伝わらなくなる。
- 注3) 逐次一次反応(Consecutive first-order reaction)
- 経路の下流分子が上流分子の量に従って活性化(合成)され、自分自身の量に従って不活性化(分解)されるという、連続した2つの一次反応からなる生化学反応の基本的枠組みのこと。
- 注4) 時定数(Time constant)
- 特徴的な時間のスケールのこと。上流信号の時定数はここでは一過的な信号の時間幅を指す。シグナル伝達経路の時定数は、経路下流の分子が追従できる上流分子の時間変化の早さの上限に相当する。経路の時定数より早く変化する信号に対して、経路の下流分子は十分に追随できず、信号がうまく伝わらなくなる。
<お問い合わせ先>
<研究に関すること>
黒田 真也(クロダ シンヤ)
東京大学 大学院理学系研究科 生物化学専攻 教授
Tel:03-5841-4697 Fax:03-5841-4697
E-mail:
<JSTの事業に関すること>
石井 哲也(イシイ テツヤ)
科学技術振興機構 イノベーション推進本部 研究領域総合運営部
〒102-0076 東京都千代田区五番町7 K’s五番町ビル
Tel:03-3512-3524 Fax:03-3222-2064
E-mail: