JST 課題達成型基礎研究の一環として、大阪大学 大学院医学系研究科の竹田 潔 教授と香山 尚子 助教らは、腸の粘膜に存在する自然免疫細胞注1)の一部が炎症を抑制する仕組みと、その自然免疫細胞の異常により炎症性腸疾患(IBD)注2)が発症することを明らかにしました。
IBDの主な原因は、炎症を誘導する獲得免疫細胞注3)の異常によるものと考えられ、これまでの研究の中心も獲得免疫細胞でした。一方で、自然免疫細胞が獲得免疫細胞の働きを制御することが分かってきていましたが、IBDの発症における自然免疫細胞の役割には不明な点が多くありました。
本研究グループは、自然免疫細胞の一部が獲得免疫細胞に結合してその働きを抑制することを明らかにし、この自然免疫細胞を、「制御性ミエロイド細胞(Mreg(エムレグ)細胞)」と名付けました。IBDを発症するモデルマウスに、正常なMreg細胞を与えると腸炎の症状が改善することを明らかにしました。本研究成果は、自然免疫細胞が腸炎を直接抑制する仕組みを明らかにしたもので、IBDの治療法開発に新たな可能性を与えると期待されます。
本研究は、大阪大学 大学院生命機能研究科の村上 正晃 准教授、大阪大学 免疫学フロンティア研究センターの石井 優 教授、徳島大学 疾患ゲノム研究センターの岡崎 拓 教授、順天堂大学 医学部の八木田 秀雄 専任准教授の協力を得て行われました。
本研究成果は、2012年3月5日の週(米国東部時間)に米国科学雑誌「米国科学アカデミー紀要(PNAS)」のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域 |
「アレルギー疾患・自己免疫疾患などの発症機構と治療技術」
(研究総括:菅村 和夫 宮城県立病院機構 理事長)
|
| 研究課題名 |
「自然免疫系を標的とした腸管免疫疾患の制御技術の開発」 |
| 研究代表者 |
竹田 潔(大阪大学 大学院医学系研究科 教授) |
| 研究期間 |
平成22年10月~平成28年3月 |
JSTはこの領域で、アレルギー疾患や自己免疫疾患を中心とするヒトの免疫疾患を予防・診断・治療することを目的に、免疫システムを適正に機能させる基盤技術の構築を目指しています。上記研究課題では、自然免疫系による腸管粘膜免疫制御機構を明らかにすることにより、腸管免疫疾患の治療技術の開発を目指します。
<研究の背景と経緯>>
免疫細胞注4)は、細菌やウイルスといった異物を認識して攻撃・排除することによって、生体を防御する仕組みにおいて重要な役割を担っています。自然免疫細胞は体内に侵入してきた病原体を消化して、その構造の特徴を獲得免疫細胞であるT細胞に伝えることで獲得免疫系を活性化します。しかし、腸管内には100兆個の腸内常在細菌や食べ物由来の抗原といった異物が常時存在するため、腸管の粘膜において免疫細胞が過剰に活性化すると、腸管の組織を破壊し、腸炎の発症につながる恐れがあります。そこで、腸管粘膜に存在する免疫細胞は腸内の異物に対して普段は反応しない免疫寛容注5)の状態である必要があります。
腸管組織における免疫寛容の破綻は、日本で急激な増加傾向にある炎症性腸疾患(IBD)の原因となることが報告されています。IBDの病因および発症機序は未解明な部分が多く、病態を根本的に改善する方法は確立されていません。IBDの特徴として炎症を導くT細胞が異常に増加していることが挙げられるため、今までのIBDの病因や発症機序の解明への取り組みはT細胞が主体である獲得免疫系を中心としたものでした。しかし、近年、自然免疫細胞に異常があると、獲得免疫系の活性化を抑制する仕組みが破綻することが明らかとなり、腸組織の恒常性維持における自然免疫細胞の役割に注目が集まっています。
腸内での免疫寛容状態の維持や、腸炎の抑制に重要な役割を果たす獲得免疫細胞としては、制御性T細胞(Treg(ティーレグ)細胞)が知られています。Treg細胞は、炎症を誘導するT細胞(炎症性T細胞)の活性化を抑制しています。これまでに、腸管粘膜に存在する自然免疫細胞の中にTreg細胞を誘導することによって、間接的に炎症を抑制しているものがいくつか報告されていました。しかし、炎症性T細胞を直接的に抑制する自然免疫細胞は報告されていませんでした。
そこで本研究グループは、Treg細胞を介さず直接的に腸炎を改善することができる自然免疫細胞が存在するのかを調べることにしました。
<研究の内容>
研究グループは、T細胞の増殖を抑制する自然免疫細胞を探すために、マウスの大腸粘膜から回収した自然免疫細胞のうち最も大きな細胞集団に着目しました。この細胞を調べたところ、3つのグループがあることが確認され(図1A)、そのうちの1つの細胞が、T細胞の増殖を抑制することが分かりました(図1B)。さらに調べると、この細胞は細胞接着分子注6)を多く発現するほか、炎症性のT細胞に良く結合することも明らかになりました。
次に、この細胞の生体内での機能を解析するために、IBDモデルマウスの腹腔にこの細胞を投与しました。その結果、この細胞が腸管組織で炎症性T細胞の増殖を抑制して腸炎を抑えていることが明らかとなりました(図1C)。本研究グループは、この細胞を、Treg細胞を誘導するのではなく細胞上にある細胞接着分子によって、炎症性T細胞と直接結合して増殖を抑制することから、新規の自然免疫細胞集団として、「制御性ミエロイド細胞(regulatory myeloid cell;Mreg細胞)」と名付けました。
Mreg細胞による腸炎の抑制に関与する分子機構をさらに明らかにするため、遺伝子発現解析を行った結果、Mreg細胞では腸管粘膜にたくさん存在する抗炎症性サイトカインのIL-10や、Stat3という転写因子注7)によって発現が誘導される遺伝子が多数存在していることが分かりました。そこで、Mreg細胞による炎症性T細胞の増殖抑制にはIL-10やStat3が必要であるという仮説を立てました。
この仮説を実証するため、IL-10またはStat3の機能を破壊したMreg細胞を炎症性T細胞と一緒に培養したところ、炎症性T細胞の増殖は抑制されませんでした。さらに、Stat3の機能を破壊したMreg細胞をIBDモデルマウスの腹腔に投与しても腸炎が抑制されないことから、Mreg細胞の炎症性T細胞の増殖抑制や腸炎抑制には、IL-10やStat3が必要であると考えられました(図2A)。さらに詳細に解析した結果、T細胞の活性化に必須のCD80やCD86というたんぱく質の発現が、Mreg細胞ではIL-10やStat3によって抑制されていることが明らかとなりました。IBDモデルマウスの腹腔に正常なMreg細胞を注射によって投与したところ、腸炎の症状が改善されました(図2B)。これらの結果により、Mreg細胞はIL-10やStat3に依存して腸炎の発症抑制に重要な役割を果たすことが分かりました。
本研究の結果より、①大腸に存在するMreg細胞は、細胞接着分子を高発現し炎症性T細胞と優位に結合する、②Mreg細胞では、IL-10やStat3が炎症性T細胞の活性化に必要なCD80やCD86の発現を抑制しているため、炎症性T細胞の増殖を誘導できない、という2段階の方法で炎症性T細胞の活性化を抑制し、腸管免疫系の恒常性維持に重要な役割を果たすことが推測されました。
<今後の展開>
本研究では、マウスの大腸に存在する自然免疫細胞のうちMreg細胞が、腸炎の発症を抑制していること、さらに、腸炎モデルマウスにおいてMreg細胞の腹腔への投与が治療効果を示すことを明らかにしました。今後、ヒトのMreg細胞の同定および作用機序の解明が進むことにより、IBDの効果的な治療法開発につながることが期待されます。
近年、腸内細菌叢注8)の変化に伴う腸管免疫寛容の破綻が、IBDだけでなく多発性硬化症などの自己免疫疾患の発症に深く関与することが報告されています。いずれも、欧米化された食生活をはじめとするライフスタイルの変化に伴い急激に日本で増加している難病です。ヒトMreg細胞が発見され細胞培養により多量のMreg細胞を作ることが可能となれば、IBDだけではなく多くの自己免疫疾患の治療法開発に結びつくことが期待されます。
<参考図>
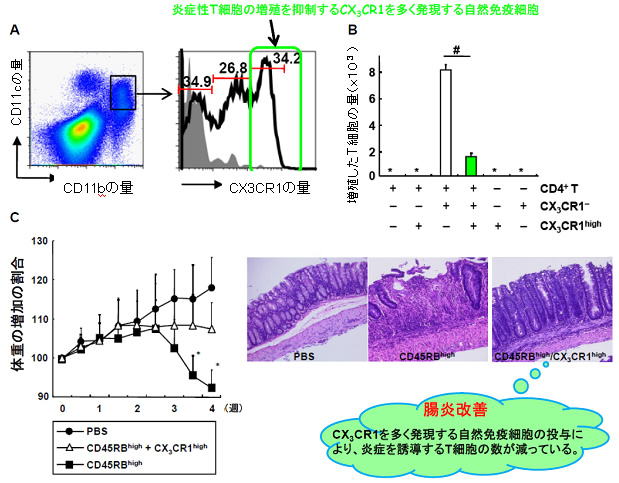
図1 大腸に存在するCX3CR1high CD11b+ CD11c+ 細胞は腸炎抑制能を示す
-
A 野生型マウス(C57BL/6Jマウス)より回収した大腸粘膜固有層細胞をCD11c、CD11b、CX3CR1で染色すると、CD11b+ CD11c+ 細胞にはCX3CR1の発現量が異なる3つの集団が存在する。左図の黒枠内はCD11b+ CD11c+ 細胞を示す。
-
B CX3CR1・ CD11b+ CD11c+ 細胞により誘導されるT細胞の増殖は、CX3CR1high CD11b+ CD11c+ 細胞を添加すると抑制される。
-
C IBDモデルとして、SCIDマウスにCD4+ CD45high T細胞を3x105個移入。同時に、大腸のCX3CR1high CD11b+ CD11c+ 細胞を3x105個投与すると腸炎が抑制される。PBSは緩衝液で、コントロール実験として用いた。
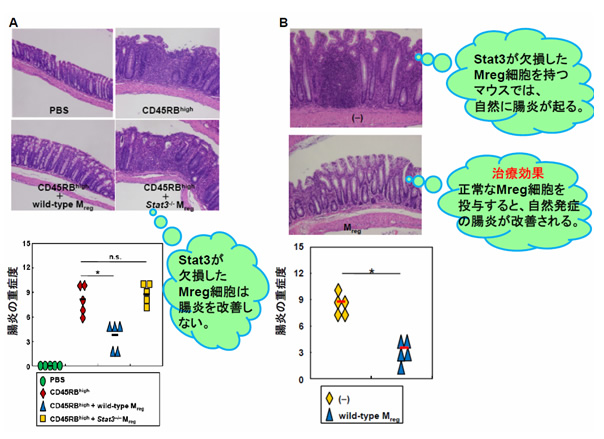
図2 Stat3欠損Mreg細胞は腸炎抑制能を持たない
-
A IBDモデルとしてRag2 -/-マウスにCD4+ CD45high T細胞を3x105個移入。同時に、PBS、野生型Mreg細胞(3x105個)、Stat3-/-Mreg細胞(3x105個)を投与。
-
B Stat3を欠損したMreg細胞を持つLysM-cre;Stat3 F/Fマウスは、腸炎を自然に発症する。正常なMreg細胞を投与すると腸炎の発症が抑制される。コントロール群にはPBS投与を行った。
<用語解説>
- 注1) 自然免疫細胞
- 体内に病原体が侵入した際に、最初の生体防御反応として機能する免疫細胞。異物の構成成分を認識することで活性化し、病原体を貪食する。マクロファージや樹状細胞などが含まれる。
- 注2) 炎症性腸疾患(IBD)
- 免疫細胞により腸の粘膜が攻撃され炎症を起こす自己免疫疾患で、発症の原因は分かっていない。潰瘍性大腸炎やクローン病などがある。
- 注3) 獲得免疫細胞
- 自然免疫細胞が貪食し、提示した病原体の特徴的分子に対してT細胞が抗体(B細胞)を作ることで病原体に対抗する獲得免疫反応を担当する細胞で、T細胞とB細胞が主体となる。
- 注4) 免疫細胞
- 生体内で病原体やがん細胞を排除するために働く細胞。元来生体に備わっている自然免疫を担当する細胞(自然免疫細胞)と決まった抗原による刺激で誘導される獲得免疫を担当する細胞(獲得免疫細胞)に大別される。また、免疫細胞はもともと共通の造血幹細胞から分化するが、その後の分化する器官により、骨髄中で分化する細胞(ミエロイド細胞)と胸腺中で分化する細胞(リンパ球系細胞)に分類することもできる。
- 注5) 免疫寛容
- 病原性のない微生物や自己の細胞に対して免疫細胞が反応を示さない状態。
- 注6) 細胞接着分子
- 細胞膜に存在して細胞同士の結合に関与するたんぱく質。
- 注7) 転写因子
- 遺伝子に結合して、遺伝子の発現を調節するたんぱく質。
- 注8) 腸内細菌叢
- 腸内には100種類以上、100兆個以上の腸内細菌が生息しており、宿主であるヒトや動物の栄養分の一部を利用しながら、他の腸内細菌とバランスを取って一種の生態系を形成しており、この生態系を腸内細菌叢(腸内フローラ)と呼ぶ。
<論文名>
“Intestinal CX3C chemokine receptor 1high (CX3CR31high) myeloid cells prevent T-cell-dependent colitis”
(腸管粘膜固有層に存在するCX3CR1highミエロイド細胞はT細胞依存的な腸炎を抑える)
doi: 10.1073/pnas.1114931109
<お問い合わせ先>
<研究に関すること>
竹田 潔(タケダ キヨシ)
大阪大学 大学院医学系研究科 免疫制御学教室
〒565-0871 大阪府吹田市山田丘2-2
Tel:06-6879-3980 Fax:06-6879-3989
E-mail:
<JSTの事業に関すること>
石井 哲也(イシイ テツヤ)
科学技術振興機構 イノベーション推進本部 研究領域総合運営部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail: