本研究成果のポイント
- 気道過敏性を引き起こすIL-17RB陽性NKT細胞の独自分化経路を発見
- IL-17RB陽性NKT細胞がさまざまなサイトカインを産生し、多くの炎症誘導に関与
- 機能解明を進め小児ぜんそくなどの新しい治療法開発へ
独立行政法人 理化学研究所(野依 良治 理事長)は、気道過敏性注1)発症に中心的な役割をするIL-17RB陽性NKT細胞注2)が、胸腺注3)という臓器で独立に分化することを突き止め、小児ぜんそく発症の鍵を握る細胞であることを明らかにしました。これは、理研 免疫・アレルギー科学総合研究センター(谷口 克 センター長)免疫制御研究グループの谷口 克 グループディレクターと渡会 浩志 上級研究員(独立行政法人 科学技術振興機構(JST) さきがけ研究者兼任)らによる研究成果です。
花粉症や食物アレルギーなどのアレルギー疾患は、日本人の約30%がかかっている国民的な病気です。中でも小児ぜんそくは、小学校入学前の子どもの約6%が発症し、1980年代に比べると6倍にも増えています(平成20年度厚生労働省患者調査)。
2008年に研究チームは、免疫細胞であるナチュラルキラーT(NKT)細胞の一タイプとして、インターロイキン17受容体B(IL-17RB)という分子が特異的に発現するIL-17RB陽性NKT細胞を発見し、ぜんそく患者のほとんどに認められる気道過敏性を起こす悪玉であることを明らかにしました。さらに、アレルギー性気道炎症のモデルマウスに抗IL-17RB抗体を投与すると、発症を抑制できることも見いだしました(2008年11月17日プレスリリース:http://www.riken.jp/r-world/info/release/press/2008/081117/detail.html)。しかし、この細胞の発生起源や機能は不明のままでした。
研究グループは今回、マウス体内のIL-17RB陽性NKT細胞の発生を解析した結果、他のNKT細胞とは違い、胸腺内で特別な分化経路をたどることを明らかにしました。さらに、アレルギーやぜんそくにかかりやすい体質とIL-17RB陽性NKT細胞の間に強い関連を見いだしました。また、冬季に流行するRSウイルスに小児ぜんそく患者が感染すると重篤化しますが、マウスではIL-17RB陽性NKT細胞が引き金を引くことも突き止めました。今後、人の乳幼児における解析が必要であるものの、気道過敏性の発症機序解明や新しい治療法開発に繋がる可能性があります。
本研究成果は、JST 戦略的創造研究推進事業 個人型研究(さきがけ)「炎症の慢性化機構の解明と制御」研究領域(研究総括:高津 聖志 富山県薬事研究所 所長)における研究課題「ナチュラルキラーT細胞による炎症慢性化機構の解明と制御」(研究者:渡会 浩志)の一環として行われ、米国の科学雑誌『PLoS Biology 』のオンライン版(2月7日付け:日本時間2月8日)に掲載されます。
<背 景>
アレルギー疾患は日本人の約30%がかかっており、国民的な病気の1つとなっています。中でもアレルギー性ぜんそくの患者数は世界で3億人、日本で約300万人と報告され、死亡者数は世界で年間25万人超、日本でも3,000人超にもおよび、年々増加の一途をたどっています(世界保健機関の疾病及び関連保健問題の国際統計分類:International Statistical Classification of Diseases and Related Health Problems)。特に小児ぜんそくは、小学校入学前の約6%の子どもが発症し、その数は1980年代に比べて6倍に増加しており、治療法の確立が強く求められています。
アレルギーは、外来性の物質(抗原)に対して免疫系が過剰に反応して起こる炎症性反応です。多くのぜんそく患者では、気管支が収縮して呼吸困難となる発作である気道過敏性がみられます。その発症には、気道から侵入した抗原に対して免疫系細胞であるヘルパーT(Th)細胞がIL-4、 IL-5、 IL-13といったサイトカイン注4)を産生し、気道の炎症を引き起こすことが重要であることが知られています。抗原刺激のたびにこの反応が繰り返され、気道組織の損傷とそれを修復しようという反応がたび重なる結果、炎症が慢性化して組織の構造が変化し、さらに気道過敏性が悪化して少量の抗原にも発作が起こるようになります。2008年に研究チームは、ヘルパーT細胞の分化の誘導・活性化や気道壁の肥厚に関与すると考えられ、このような病態形成に至る引き金を引く細胞の1つがNKT細胞の内でもIL-17RBを細胞表面に有する特定の細胞集団(IL-17RB陽性NKT細胞)であることを突き止めました(図1)。その結果から、この細胞集団の発生起源や機能の詳細を明らかにしてその作用を押さえることができれば、新たなぜんそく治療法の開発につながると考えられました。しかし、IL-17RB陽性NKT細胞が体内でどのような経路をたどって分化するのか、詳細な機能については不明なままでした。
これまでNKT細胞の分化経路として、ヘルパーT細胞のマーカーであるCD4とキラーT細胞のマーカーであるCD8の両方が陽性のCD4+CD8+細胞を起源として、胸腺内でステージ1(CD44陰性NK1.1 陰性)、ステージ2(CD44陽性NK1.1 陰性)、ステージ3(CD44陽性NK1.1 陽性)の順に分化し、末梢へと移動することが知られていました(図2A)。そこで研究グループは、IL-17RB陽性NKT細胞の発生起源を特定するため、胸腺に存在するNKT細胞を詳細に解析しました。
<研究手法と成果>
まず、IL-17RBを特異的に認識するモノクローナル抗体注5)を用いて、生後4~6週(乳幼児相当)のマウス胸腺内のNKT細胞のIL-17RBの発現を調べました。その結果、胸線内のNKT細胞の10%程度に、IL-17RBが発現することが分かりました。さらに、IL-17RB陽性NKT細胞の大半がステージ1とステージ2に存在することに加え、これまでNKT細胞の形成維持と数の増加に必須と考えられていたIL-15を必要としないことも見いだしました。そして、このIL-17RB陽性NKT細胞は、ステージ1からステージ2へと分化発生した後末梢へと移動することを突き止め、これまで考えられてきたNKT細胞とは違う独自の分化経路で発生する細胞集団であることが明らかとなりました(図2B)。
また、胸腺内のIL-17RB陽性NKT細胞の数はマウスの系統によって異なり、アレルギーを発症しやすい系統のマウスでは、発症しにくい系統のマウスより3~4倍多く発現することが分かりました。これは、アレルギーやぜんそくになりやすい体質であるかどうかは、IL-17RB陽性NKT細胞の存在数に関わることを示しています。
これまでに研究チームは、IL-17RB陽性NKT細胞がTh2サイトカインを大量に産生することを確認しています。今回、IL-17RB陽性NKT細胞の機能を確かめるため、IL-17RBをコードするIl17rb 遺伝子を欠損させたIl17rb ノックアウトマウス注6)を作製し、サイトカイン産生能力を調べました。その結果、Th2サイトカインだけでなく、Th9サイトカイン(IL-9、IL-10)やTh17サイトカイン(IL-17A、IL-22)の生産能力が低下したため、IL-17RB陽性NKT細胞はTh2サイトカインだけでなく、Th9サイトカインやTh17サイトカインも産生する能力を有していることが分かりました。
これらサイトカインの産生を詳細に調べたところ、IL-17RB陽性NKT細胞は、CD4の有無によって陽性と陰性に分かれることを発見し、IL-17RB陽性CD4陰性NKT細胞はTh17サイトカインを、IL-17RB陽性CD4陽性NKT細胞はTh2、Th9、Th17サイトカインを産生することが分かりました(図2B)。これらのサイトカインは、直接アレルギー反応を誘導するサイトカイン群として知られる一方、他の免疫細胞や多形核白血球に作用して炎症を誘導することが知られています。従って、IL-17RB陽性NKT細胞の活性化が引き金となって、免疫反応の経路のあらゆるところで炎症誘導を引き起こすことを示しています。
IL-17RB陽性NKT細胞は、マウスでは肺などの限られた場所に集積し、幼少期に多く存在します。小児ぜんそく患者は、冬季に流行するRSウイルスに感染すると、重篤な細気管支炎や肺炎を引き起こすことが知られています。そこで、RSウイルスに感染したモデルマウスを解析したところ、NKT細胞ノックアウトマウスやIl17rb ノックアウトマウスでは、アレルギー気道炎症が誘導されませんでした(図3)。しかし、NKT細胞ノックアウトマウスにIL-17RB陽性NKT細胞を移入すると、RSウイルスによって誘発されるアレルギー気道炎症が細胞数の増加とともに悪化することが分かりました。従って、IL-17RB陽性NKT細胞がRSウイルスによる炎症誘導の中心を担っていると考えられます。
<今後の期待>
今回研究グループは、IL-17RB陽性NKT細胞が胸腺で、独自の経路をたどって分化すること、および、この細胞がさまざまな炎症の誘導に関わるサイトカインの産生に関与していることを明らかにしました。本研究はマウスを用いて行いましたが、今後、乳児や小児におけるIL-17RB陽性NKT細胞の役割を詳細に解析することが重要となります。この細胞の機能を抗体治療などで人為的に抑制することで、気道過敏性の悪化を抑えることができ、社会的要請の高い小児ぜんそくの効果的な治療法の開発につながるものと期待できます。
<参考図>
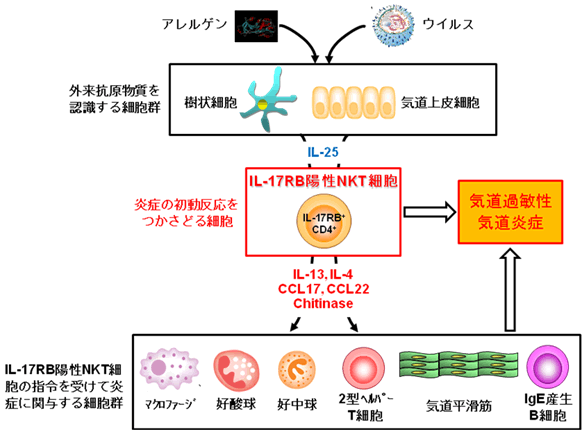
図1 気道過敏性の発症
気道過敏性の発症には、気道から侵入した抗原を提示した樹状細胞などによって主に2型ヘルパーT細胞がサイトカインを産生し、気道の炎症を引き起こすことが重要であることが知られている。気道過敏性はこの炎症が慢性化し、起こり続けている状態だと考えられる。渡会研究者らは2008年、2型ヘルパーT細胞などを誘導・活性化し、気道過敏性へと至る引き金を引く細胞として新しくIL-17RB陽性NKT細胞を明らかにした。
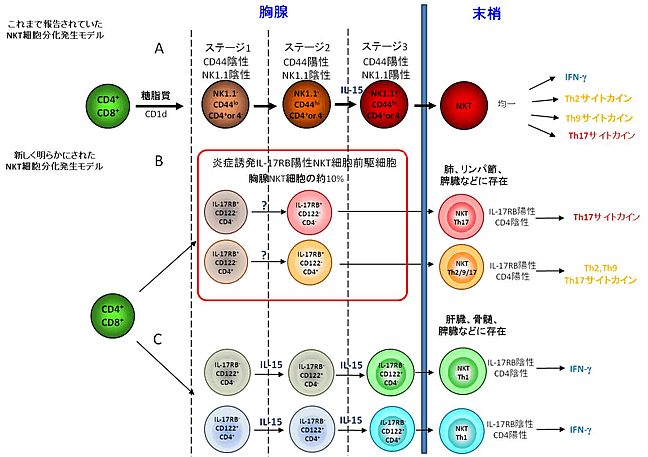
図2 胸腺内でのNKT細胞分化発生様式
- A:これまで報告されていたNKT細胞分化発生モデル
NKT細胞は、胸腺内でCD4とCD8がともに陽性であるCD4+CD8+細胞よりステージ1、2、3を経て分化し末梢へと移行する、と考えられていた。
- B:IL-17RB陽性NKT細胞の発生モデル
IL-17RB陽性NKT細胞は、初期の分化段階から別個に存在し、胸腺NKT前駆細胞を経てステージ1から2をたどり、末梢(肺、リンパ節、脾臓など)に移行する(赤線囲み)。さらに、このIL-17RB陽性NKT細胞は、CD4陰性とCD4陽性に別れ、CD4陰性からはTh17サイトカインを、CD4陽性からはTh2、9、17サイトカインを産生し、炎症誘導反応の中心を担う。
- C:IL-17RB陰性NKT細胞の発生モデル
IL-17RB陰性NKT細胞は、CD4陽性/陰性ともに肝臓、骨髄、脾臓などに存在し、IFN-γ(インターフェロンガンマ)を産出する。
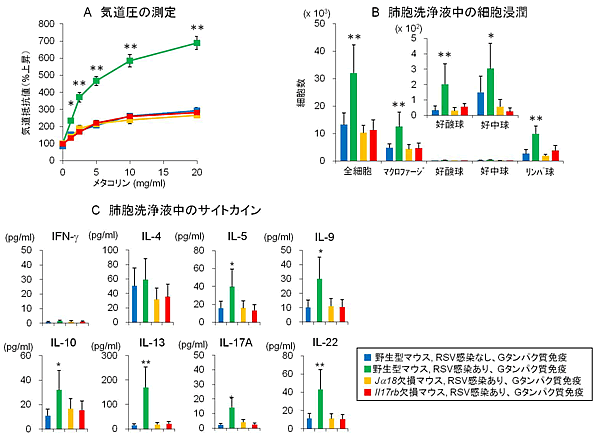
図3 RSウイルス感染小児ぜんそくマウスモデルにおけるIL-17RB陽性NKT細胞の役割
RSウイルスを感染、RSウイルスGタンパク質を免疫した野生型マウス(緑色)では、炎症に関与する細胞浸潤(B)やサイトカイン量(C)が多く、気道抵抗値が上昇して気道炎症を発症する(A)のに対して、NKT細胞ノックアウトマウス(黄色)あるいはIl17rb ノックアウトマウス(赤色)では気道炎症を発症しない。従って、IL-17RB陽性NKT細胞がRSウイルス感染による炎症誘導の中心を担っていると考えられる。
<用語解説>
- 注1) 気道過敏性
- 種々の刺激に対して気道が収縮しやすいこと。ぜんそく患者のほとんどすべてに認められる。ぜんそくの人は健康な人にとって無害な刺激(冷気、タバコの煙、線香の煙、香水の匂いなど)にも敏感に反応して発作を起こす。アレルギー性ぜんそくは、気道の慢性炎症性疾患を指す。
- 注2) IL-17RB陽性NKT細胞
- T細胞、B細胞、NK細胞に続く第4のリンパ球決定系列で、免疫の制御や、がんの免疫学的監視などさまざまな役割を担うNKT細胞のうち、受容体IL-17RBを発現する細胞。IL(インターロイキン)は、白血球によって分泌され細胞間コミュニケーションの機能を果たす細胞伝達物質。2008年に免疫制御研究グループが炎症の誘導反応に関わることを明らかにした。
- 注3) 胸腺
- T細胞の分化や成熟など免疫系に関与する臓器。胸小葉とよばれる二葉からなり、胸骨の後ろ、心臓の前に位置し、心臓に乗るように存在する。
- 注4) サイトカイン
- 細胞同士の情報伝達に関わるさまざまな生理活性を持つタンパク質の総称。
- 注5) モノクローナル抗体
- 1つのクローン細胞群がつくる1種類の抗体。動物に抗原を注入しても得られないが、抗体産生細胞と分裂能力を持つ腫瘍細胞との雑種細胞を培養して増殖させることで多量に得られる。体内や細胞に微量に存在する物質の検定や精製・局在性を調べるのに有効。病気の診断・治療にも利用される。
- 注6) ノックアウトマウス
- 目的の遺伝子を人為的に欠損させたマウス。
<原論文情報>
Watarai H, Sekine-Kondo E, Shigeura T, Motomura Y, Yasuda T, Satoh R, Yoshida H, Kubo M, Kawamoto H, Koseki H, Taniguchi M. (2012)
Development and Function of Invariant Natural Killer T Cells Producing TH2- and TH17-Cytokines. PLoS Biology 10(2): e1001255.
doi: 10.1371/journal.pbio.1001255
<報道担当・問い合わせ先>
<研究内容に関すること>
渡会 浩志(ワタライ ヒロシ)
理化学研究所
免疫アレルギー科学総合研究センター 免疫制御研究グループ 上級研究員
Tel:045-503-7008 Fax:048-503-7006
横浜研究推進部 企画課
Tel:045-503-9117 Fax:045-503-9113
<報道担当>
理化学研究所 広報室 報道担当
Tel:048-467-9272 Fax:048-462-4715
科学技術振興機構 広報ポータル部
Tel:03-5214-8404 Fax:03-5214-8432
<JSTの事業に関すること>
科学技術振興機構 イノベーション推進本部 研究推進部(研究推進担当)
Tel:03-3512-3525 Fax:03-3222-2063
E-mail: