JST 課題達成型基礎研究の一環として、慶應義塾大学 医学部の末松 誠 教授と、梶村 眞弓 専任講師らのグループは、マウスの脳内で生成されている一酸化炭素(CO)が、脳梗塞などの低酸素時の脳血管拡張反応と脳のエネルギー代謝の維持に重要な働きをしていることを発見しました。
私たちの体の中では、さまざまなガスが作られており、血流を増やしたり、炎症を抑えたりと生体内で重要な働きをしています。これらのガスは「ガスメディエータ」と呼ばれ、一酸化窒素(NO)やCO、硫化水素(H2S)が代表分子です。脳や肝臓は、COを最も多く生成する臓器ですが、脳で生成される大量のCOの生理的な役割は不明でした。
今回の研究では、COと結合するたんぱく質として「シスタチオニンβ合成酵素(CBS)注1)」に着目し、マウスを用いてCOやH2Sの量の変化と連動して、血管の口径や、脳のエネルギー代謝がどのように変化するかを検証しました。その結果、脳では、CBSが血管拡張作用のあるガス分子H2Sを生成しており、正常時の脳では、COがCBSの働きを阻害してH2Sの量を抑えているため、血管が少し収縮した状態にあることが分かりました。そして、低酸素時にはCO濃度が低下し、CBSへの抑制が解除され、H2Sが増加することによって血管が拡張することを明らかにしました。さらに、COを生成する酵素のないマウスでは、低酸素時に脳の微小血管がうまく拡張しないため、脳のエネルギー代謝の要になるアデノシン3リン酸(ATP)注2)の維持ができなくなることが、質量顕微鏡の技術によりエネルギー代謝物の分布と局所濃度を測定することで分かりました。このことから、COは、急激な酸素(O2)の供給低下にうまく対応できるように、血管拡張性や脳のエネルギー産生の「予備能」(正常時は少し抑え気味、しかし、一度ピンチになった時は、より効果的に血流を増加させたり、エネルギーを産生したりする能力)を与えるガスメディエータであることが明らかになりました。
今回の「O2濃度が低下するとCO濃度が低下し、さらにH2S濃度が増加して、血管が拡張する」という情報伝達経路の発見は、低酸素時のリスクマネジメントを、複数のガス分子が代謝システムを精妙に制御することによって実行している証明となります。さらにこの発見は、脳梗塞などの病態の制御や、治療の開発へとつながると期待されます。
本研究は、慶應義塾大学 医学部と米国のジョンズ・ホプキンス大学との共同研究で行われ、本研究成果は、米国科学雑誌「米国科学アカデミー紀要(PNAS)」のオンライン速報版で2012年1月9日の週(米国東部時間)に公開されます。
本成果は、以下の事業・研究プロジェクトによって得られました。
戦略的創造研究推進事業 ERATO型研究
| 研究プロジェクト |
「末松ガスバイオロジープロジェクト」 |
| 研究総括 |
末松 誠(慶應義塾大学 医学部 医化学研究室 教授) |
| 研究実施期間 |
平成21年10月~平成27年3月 |
JSTはこのプロジェクトで、生体内にあるガス分子がどのようなメカニズムで生理的な役割を持つのかを解明し、病気の治療に役立てることを目指しています。
<研究の背景>
ガス分子は究極の極小分子で、たんぱく質を始めとする生体高分子のすき間に入り込み、結合することによってその機能を変化させます。例えば、ヘム注3)の鉄原子部分にガスが結合することによって、ヘモグロビンのようなヘムたんぱく質の機能を変えるのはその典型例です。本プロジェクトでは、このようなガス応答性のナノスイッチ分子が、私たちの体の中で「いつ、どこで、どのように」して作られ、どのような「未知の働き」をしているのかを探究しています。「私たちの生存に不可欠なガスは?」というと、多くの人は「酸素(O2)」と答えるはずです。一方、一酸化炭素(CO)や硫化水素(H2S)は、大量に取り込むと毒ガスとして働きますが、COもH2Sも肝臓や脳の細胞の中で恒常的に作られている「ガスメディエータ」です。COやH2Sは、生体内で血管を収縮あるいは拡張させることで血流を制御したり、抗炎症など有用な生理作用を発揮することが判明しつつありますが、そのメカニズムは不明な点が多いのが現状です。
現在までに、脳では多量のCOが恒常的に作られていることは分かっていましたが、COの生理学的役割に関しては不明でした。本研究では、脳組織が脳梗塞などの低酸素状態になると、酸素(O2)を原料にしてできるCOの濃度が低下することが、低酸素時のリスクマネジメントの根本機構なのではないかと考えました。そこで、O2(第1のガス)を利用してCO(第2のガス)を生成しているヘムオキシゲナーゼ(HO)注4)、さらにそのCOと結合するたんぱく質としてH2S(第3のガス)の産生酵素であるシスタチオニンβ合成酵素(CBS)に着目しました。H2Sは、脳では血管を拡張させる働きがあることから、低酸素時に起こるCOやH2Sの量的変動が、脳実質内の微小血管の口径や、脳のエネルギー代謝をどのように制御しているのかを検証しました。
<研究の内容>
脳神経は数分の虚血状態でも死に陥ることが知られています。脳がこのような緊急事態に対応するためには、ゆるやかなメカニズムによる応答では間に合わず、別のメカニズムがあると考えられています。しかし、低酸素になって数分以内に起こる非常に速い応答の仕組みは不明でした。本プロジェクトでは、数分という短時間の低酸素状態にも即時に応答し、エネルギー代謝を維持する仕組みを解明するため、「CO-CBS-H2S」の関係に着目して研究を進めてきました。
正常な脳組織においては、神経細胞や血管内皮細胞で豊富に生成されているCOは、CBSの働きを阻害し、血管拡張性ガスとして知られているH2Sの生成量を抑えていることを世界で初めて発見しました。この仕組みによって、正常時には微小血管が恒常的に少しだけ収縮していることを、マウスを用いた実験で確認しました。ところが、低酸素状態に陥ると、O2(CO産生の原料)の不足によって、COの産生量がただちに低下することが分かりました。これは、神経細胞(ニューロン)や血管内皮細胞に発現している酵素「構成型ヘムオキシゲナーゼ(HO-2)」が、酸素が足りないことでCOを生成できなかったためです。つまり、HO-2は脳組織での「酸素センサー」として機能することを示したことになります。
さらに、島津製作所の協力により、精密質量分析技術を利用した新規のH2S測定法を構築して実験を行った結果、低酸素下の脳組織では、COによる恒常的なCBSの活性阻害はCOの低下により速やかに解除され、H2Sが増加することも突き止めました(図1)。これは、低酸素に対する生体防御機構として「ガスが代謝酵素を制御し、別のガスを調節する新しい機構」が存在すること意味しています。
また、「HO-2の欠損マウス」(COの基礎産生量が低下している動物)を用いて、ATPなどのエネルギー代謝物の分布と局所濃度を質量分析イメージングによって検証したところ、正常酸素の状態では、HO-2欠損マウスの脳は、野生型(COの基礎生産量を低下させていない動物)と比べて、ATPのレベルが増加していることが分かりました。ところが、一度低酸素になるとHO-2欠損マウスのATPレベルは極端に低下するのに対し、野生型のマウスではATPは若干減少するものの、比較的維持されているという対照的な結果を得ました(図2)。これらの結果から、中枢神経系で生成されるCOは、急激な酸素の供給低下にうまく対応できるように、血管拡張性や脳のエネルギー産生の「予備能」(正常時は少し抑え気味、しかし、一度ピンチになった時は、より効果的に血流を増加させたり、エネルギーを産生したりする能力)を与えるガスメディエータであることが明らかになりました。
<今後の展開>
近年、脳の局所で神経機能が活発になった時に起こる局所血流の増加「ファンクショナルーハイパーエミア」のメカニズムの解明が盛んに行われています。ところが、秒単位という非常に早い速度で起こるファンクショナルーハイパーエミアの生化学的な仕組みは不明です。局所の神経機能活動が活発な時はその部位の代謝が活発化し、細胞内外のガス環境も瞬時に変化すると予想できることから、今回発見された複数のガスが織りなす情報伝達機構が、ファンクショナルーハイパーエミアを引き起こす仕組みに寄与しているか否かの検討も、今後の研究の視野に入れていきたいと考えています。
さらに、「ガス分子の生体内作用点の実態」を解明することにより、脳循環障害や神経疾患の病態を理解し、治療のターゲットを絞りこむための布石としたいと考えています。なぜならば、脳で消費されるO2はATPを産生するためだけでなく、さまざまな血管作動性物質を産生する原料となるからです。従って、虚血に起因する組織低酸素により起こる組織内ガス分布のリモデリング(再構築)や、ガスシグナリング(ガスによる情報伝達)の変化のメカニズムに対する理解を深めることは、治療の第一歩であると言えます。転写・翻訳による制御は、新たにたんぱく質を合成するため、時間のかかる仕組みです。今回発見されたガス分子による制御は、数分以内の応答が可能な低酸素病態の防御機構の一端です。この研究成果は、脳梗塞などの脳循環疾患の制御や救急蘇生学の最適化などの臨床医学研究への展開が期待されます。
<参考図>
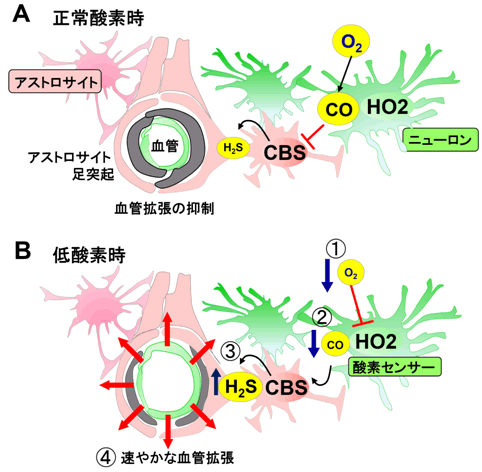
図1 低酸素性血管拡張の仕組みとして発見されたCO-感知性H2S情報伝達経路
- A.正常酸素時
O2が十分供給されている状態では、ヘムオキジゲナーゼ(HO-2)によってマイクロモルレベルのCOが産生される。この濃度のCOは中枢神経のアストロサイト注5)でH2Sを作っているCBSという酵素を阻害する。その結果、血管を拡張させる能力のあるH2S の産生量を低下させるため、正常酸素状態では、脳の微小血管は、少しだけ収縮する。
- B.低酸素時
一度、組織に供給されるO2の量が下がると、HO-2が低酸素を感知することを起点として、図中に番号で示したような、ガスメディエータの変動が起こり、結果として血管が拡張する。脳組織では、このような「ガスが代謝酵素を制御し、別のガスを調節する機構」があることが判明した。
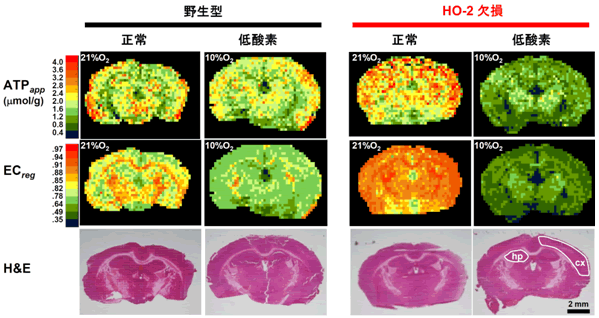
図2 質量分析イメージングによるATPの脳内分布
正常酸素の状態(21% O2)では、HO-2欠損マウスの脳は野生型に比べて、ATPのレベルが増加していることが見てとれる。ところが、一度低酸素(10% O2)になると、HO-2欠損マウスのATPレベルは極端に低下するのに対し、野生型のマウスではATPは若干減少するものの、比較的維持されているという対照的な結果が示されている。このことから、COが精妙な代謝システム制御ガスとして機能していることが明らかになった。
<用語解説>
- 注1) シスタチオニンβ合成酵素(CBS:cystathionine β-synthase)
- ホモシステインとシステインの縮合により、シスタチオニンと硫化水素を生成する反応を触媒する酵素。
- 注2) アデノシン3リン酸(ATP:adenosine triphosphate)
- 「生体のエネルギー通貨」と称される、真核生物におけるエネルギー源。生物がたんぱく質合成やDNA合成、神経細胞の活動、筋肉の伸縮などを行う際には、ATPを分解することでそれらのエネルギーを得る。
- 注3) ヘム(heme)
- 2価の鉄原子とポルフィリンからなる錯体で、ヘモグロビン、ミオグロビン、薬物代謝酵素(P450)、カタラーゼ、一酸化窒素合成酵素、ペルオキシダーゼなどのヘムたんぱく質の補欠分子族。ガスはヘムの鉄原子の部分に結合する能力が高く、そうすることでヘムたんぱく質の機能を変化させることが知られている。つまり、ヘムの鉄原子は「ガスのセンサー」として機能する能力が保持されている。
- 注4) ヘムオキシゲナーゼ(HO:heme oxygenase)
- ヘムを一酸化炭素(CO)と、ビリベルジン(biliverdin)、遊離鉄(Fe2+)に分解する酵素。ヘムオキシゲナーゼの反応には、ヘムの分子骨格であるポルフィリン環を開裂するために「分子状酸素」(O2)を必要とする点が今回の実験の1つの重要なポイントである。ヘムオキシゲナーゼには、構成型のヘムオキシゲナーゼ-2(HO-2)と誘導型ヘムオキシゲナーゼ-1(HO-1)が存在する。
- 注5) アストロサイト(astrocyte)
- 中枢神経系に存在するグリア細胞の一種で、神経活動が円滑に行われるために重要な役割を担う細胞群。アストロサイトが脳代謝においてエネルギー基質の受け渡しの過程に重要な役割を果たしていることが実験的に証明されつつある。また血管内皮細胞とともに、危険な分子の脳実質への侵入を妨げる「血液脳関門」を形成している。
<掲載論文名>
“Hypoxic regulation of the cerebral microcirculation is mediated by a carbon monoxide-sensitive hydrogen sulfide pathway”
(中枢神経系における一酸化炭素の役割;一酸化炭素―硫化水素経路を介した急性低酸素による脳微小循環代謝制御)
doi: 10.1073/pnas.1119658109
<お問い合わせ先>
<研究内容に関すること>
末松 誠(スエマツ マコト)
慶應義塾大学 医学部 医化学教室 教授
〒160-8582 東京都新宿区信濃町35番地
Tel:03-5363-3753 Fax:03-5363-3466
E-mail:
梶村 眞弓(カジムラ マユミ)
慶應義塾大学 医学部 医化学教室 専任講師
〒160-8582 東京都新宿区信濃町35番地
Tel:03-5363-3461 Fax:03-5363-3466
E-mail:
<JSTの事業に関すること>
金子 博之(カネコ ヒロユキ)
科学技術振興機構 イノベーション推進本部 研究プロジェクト推進部
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528 Fax:03-3222-2068
E-mail: