JST 課題達成型基礎研究の一環として、大阪バイオサイエンス研究所の古川 貴久 研究部長と佐貫 理佳子 研究員らは、マイクロRNAと呼ばれる短いRNAの一種、miR-124aが脳や網膜注1)といった神経回路の形成と神経細胞の生存に重要であることを明らかにしました。
マイクロRNAは18~25個の核酸でできている小さなRNAで、アミノ酸(たんぱく質)へと翻訳されず、機能が不明でした。しかし、近年の研究によってマイクロRNAには、さまざまな種類が存在し、その中には遺伝子に結合してその発現を抑制するなど、生体にとって重要な働きをすることが分かってきました。そのマイクロRNAの1つであるmiR-124aは中枢神経系注2)で最も多く存在しており、脳に発現する全マイクロRNA量の25~48%にも達します。そのため、miR-124aの、中枢神経系での重要な機能が想定されていましたが、これまで複数のグループからいくつもの相反する結果が報告され、その機能は謎のままでした。
本研究グループは、miR-124aの機能を生体で明らかにするため、miR-124aが機能しないマウス(miR-124a欠損マウス)を世界で初めて作ることに成功しました。このmiR-124a欠損マウスでは、脳全体が小さく脳の発達障害を起こしていました。さらに調べると、「記憶」に重要な海馬注3)の神経回路形成の異常が認められました。また網膜では、「視力と色覚」を司る神経細胞が死んでいることも発見しました。この異常は、miR-124aがないと、その標的となっている遺伝子Lhx2の発現が抑制されず、Lhx2が過剰に機能し続けていることが原因であることを突き止めました。これは脳や網膜といった中枢神経系の神経回路の形成や、神経細胞の生存にマイクロRNAが重要な役割を担うことを生体レベルで初めて証明したものです。
ヒトでは、miR-124aの遺伝情報を含む染色体領域の欠損あるいは重複によって、てんかんや自閉症などの精神神経疾患が起こると知られています。この研究成果から、精神神経疾患の原因究明や神経系の再生医療に貢献することが期待されます。
本研究成果は、2011年8月21日(英国時間)に英国科学誌「Nature Neuroscience」のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域 |
「脳神経回路の形成・動作原理の解明と制御技術の創出」
(研究総括:小澤 瀞司 高崎健康福祉大学 健康福祉学部 教授) |
| 研究課題名 |
「網膜神経回路のシナプス形成と生理機能発現の解析」 |
| 研究代表者 |
古川 貴久(大阪バイオサイエンス研究所 発生生物学部門 研究部長) |
| 研究期間 |
平成21年11月~平成27年3月 |
JSTはこの領域で、脳神経回路の発生・発達・再生の分子・細胞メカニズムを解明し、さらに個々の脳領域で多様な構成要素により組み立てられた神経回路がどのように動作してそれぞれに特有な機能を発現するのか、それらの局所神経回路の活動の統合により、脳が極めて全体性の高いシステムをどのようにして実現するのかを追求します。またこれらの研究を基盤として、脳神経回路の形成過程と動作を制御する技術の創出を目指します。
上記研究課題では、網膜に注目してシナプスが特異的に結合する分子メカニズムおよび網膜神経回路の生理機能と動作メカニズムの解明を目的とし、網膜神経回路がどのようなメカニズムと機能原理に基づき視覚情報処理を行っているかを明らかにします。
<研究の背景と経緯>
DNAからメッセンジャーRNA(mRNA)が転写され、アミノ酸(たんぱく質)へと翻訳されるという一連の機構は「セントラルドグマ」と呼ばれ、高等生物の遺伝情報の伝達において中心的な役割を果たしていると考えられてきました。一方で、たんぱく質へと翻訳されない、つまり古典的セントラルドグマに属さない「小さなRNA」が、さまざまな遺伝子の制御に関わっていることが近年明らかになってきました。こうした小さなRNAの役割を利用した例の1つが、2006年にノーベル医学生理学賞を受賞したRNA干渉法(RNAi)です。生物の生体内で作られる、RNA干渉作用(二本鎖RNAと相補的な塩基配列を持つmRNAが分解される現象)を持つ小さなRNAを「マイクロRNA」といいます。マイクロRNAはさまざまな生物に存在しており、ウイルスや細菌からヒトまでの153生物種の中で19,724種類がこれまでに登録されています(2011年4月時点)。それぞれのマイクロRNAには標的とするmRNAがあり、マイクロRNA自身の核酸配列と相補的な配列を持つmRNAに結合します。マイクロRNAに結合されたmRNAは翻訳阻害もしくは分解によってそのmRNAとしての機能が失われ、発現抑制されます。近年、このようなマイクロRNAの機能が、「生命現象」や「人の病気」に深く関わることが次第に明らかになってきています。マイクロRNAが発症や進行に関わる疾患として、がんや心臓病、精神疾患などが知られています。
数多くあるマイクロRNAの中で、本研究チームが注目したのはmiR-124aです。miR-124aは中枢神経系で最も高発現するマイクロRNAです。しかし、miR-124aの機能に関しては相反する矛盾した報告が複数あり、実際の生体での機能はほとんど分かっていませんでした。
<研究の内容>
本研究チームは、miR-124aの機能を生体で明らかにするため、miR-124aを欠損させたノックアウトマウスを世界で初めて作ることに成功しました。miR-124a欠損マウスは欠損していないマウス(野生型)に比べて脳全体が小さく、脳の発達障害を起こしていました。そこで、中枢神経系の中でも記憶の入り口である「海馬」と視覚情報の入り口である「網膜」に注目して観察を行いました。
海馬は大まかに分けると、歯状回、CA3、CA1といった神経細胞が密集して存在する領域で構成されています。これら3つの領域は回路を形成してつながっています。これらのうち、歯状回にある神経細胞(顆粒細胞注4))とCA3領域にある神経細胞(錐体細胞注5))は、「苔状線維注6)」と呼ばれる軸索を伸ばして錐体細胞と神経回路を形成します。しかし、miR-124a欠損マウスの海馬では、苔状線維とCA3錐体細胞の回路形成が正しい位置で形成されず、苔状線維がCA3領域内へ異常に侵入していることを発見しました(図1)。すなわち、miR-124a欠損マウスは本来とは異なる場所で回路を形成してしまったのです。このような海馬の回路形成異常は、側頭葉てんかん発作のモデル動物でも観察されています。さらに網膜では、視力と色覚を司る神経細胞(錐体視細胞注7))が細胞死を起こしていました。その結果、miR-124a欠損マウスでは錐体視細胞が光を感受することで始まる神経回路の情報伝達能力が低下していることを見いだしました(図2)。
また、miR-124a欠損マウスにおける海馬の神経回路異常と網膜の錐体視細胞の細胞死は、miR-124aがないために、脳の初期発生期に機能する遺伝子Lhx2の働きを抑制できないことが原因であることを明らかにしました。これらの知見は、脳や網膜といった中枢神経系の神経回路の形成や神経細胞の生存に特定のマイクロRNAが重要な役割を担うことや、そのメカニズムを生体レベルで初めて証明したものです(図3)。
<今後の展開>
マイクロRNAによる中枢神経系の機能制御に関する研究は始まったばかりです。このようなマイクロRNA、特に最も発現量の多いmiR-124aの神経回路形成や精神神経機能に果たす役割と、その機構の解明が今後の重要な課題になります。近年では、精神疾患は神経回路の病気であると考えられています。ヒトでは、miR-124aを含む染色体領域の欠損あるいは重複によって、てんかんや自閉症などの精神神経疾患が起こると知られています。そのため、この研究から精神神経疾患の原因究明や神経系の再生医療への貢献が期待されます。
<参考図>
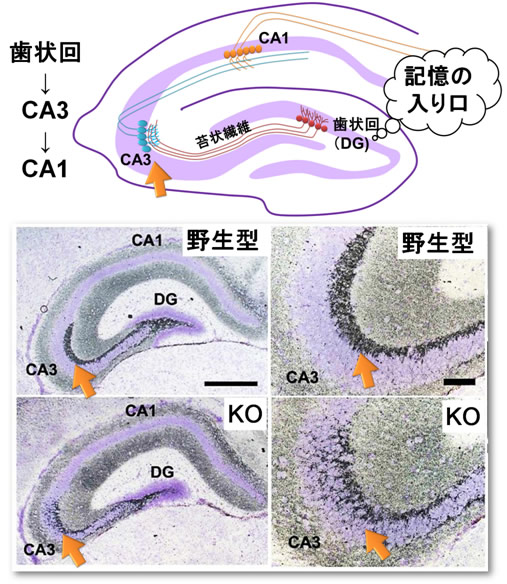
図1 miR-124a欠損による海馬の神経回路異常
海馬の歯状回の顆粒細胞(赤)に入った情報は苔状線維を介してCA3の錐体細胞(青)へと伝達され、さらにCA1へと伝わる(上図)。miR-124a欠損マウス(KO)では、苔状線維とCA3錐体細胞の回路形成が正しい位置で形成されず、苔状線維のCA3領域への異常侵入が認められた(下図、橙矢印)。
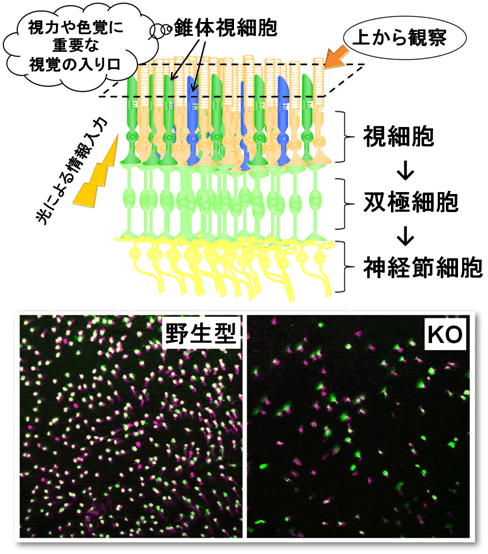
図2 miR-124a欠損による錐体視細胞の脱落
視覚情報の入り口である視細胞によって光信号は受容され、電気信号へと変換される。その信号は双極細胞を介して神経節細胞へと伝達され、脳に情報が伝わる。この視覚情報入力系のうち錐体視細胞は視力と色覚にとって重要な働きをする(上図)。miR-124a欠損マウス(KO)では錐体視細胞が細胞死によって脱落し、その結果、野生型に比べて錐体視細胞が減少する。錐体視細胞を蛍光色素で標識し、網膜を上から観察した(下図)。
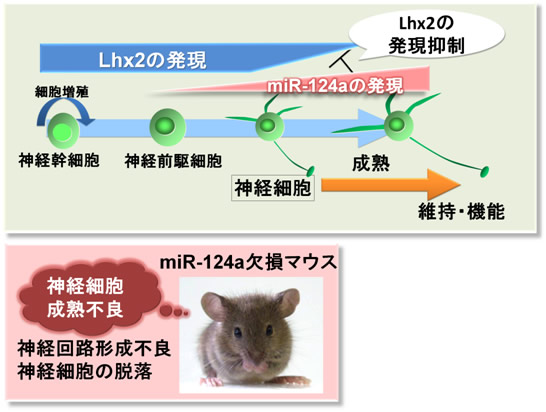
図3 miR-124aの機能メカニズム
miR-124aは分化した神経細胞から発現し始め、成熟が進むにつれてその発現量が多くなる。この時、miR-124aは標的遺伝子であるLhx2の発現を抑えることによって、神経細胞の発達・成熟と維持を制御して正常な神経機能を発揮する。miR-124a欠損マウスは神経細胞の成熟不良により、神経回路形成の異常や神経細胞死が起こる。
<用語解説>
- 注1) 網膜
- 視覚系の入り口となる器官。眼球内の後部にあり、光信号を電気情報に変換して、さらにその情報を統合して脳へ伝達する。
- 注2) 中枢神経系
- 脳や網膜、および脊髄を指す。情報伝達の際にその情報の統合処理を行うことが特徴である。
- 注3) 海馬
- 記憶を司る脳の器官。海馬の異常はてんかん発作やアルツハイマー病の原因となる。
- 注4) 顆粒細胞
- 海馬を構成する細胞のうち、歯状回に存在する顆粒状の神経細胞で、記憶情報処理の入り口となる細胞。
- 注5) 錐体細胞
- 海馬と大脳皮質に見られるピラミッド型の神経細胞。錐体細胞は長い軸索を持ち、処理した情報を脳のほかの部分へと伝達している。ほかの神経細胞からの情報を受け取る樹状突起の部分には「スパイン」と呼ばれる棘状の突起からなるシナプスをたくさん持ち、情報入力アンテナとして機能する。
- 注6) 苔状線維
- 顆粒細胞から伸びる軸索のことで、CA3の錐体細胞へと向かって伸長する。
- 注7) 錐体視細胞
- 網膜の中でも特に視力と色覚を司る、光信号を電気信号に変換できる細胞。錐体視細胞の異常は、黄斑変性症や錐体ジストロフィーなどの原因となる。
<論文名>
“MiR-124a is required for hippocampal axogenesis and retinal cone survival through Lhx2 suppression”
(miR-124aは海馬の軸索形成と網膜錐体視細胞の生存におけるLhx2の抑制に必須である)
doi: 10.1038/nn.2897
<お問い合わせ先>
<研究に関すること>
古川 貴久(フルカワ タカヒサ)
大阪バイオサイエンス研究所 発生生物学部門 研究部長
〒565-0874 大阪府吹田市古江台6-2-4
Tel:06-6872-4853 Fax:06-6872-3933
E-mail:
<JSTの事業に関すること>
河村 昌哉(カワムラ マサヤ)
科学技術振興機構 イノベーション推進本部 研究領域総合運営部
〒102-0075 東京都千代田区三番町5 三番町ビル
Tel:03-3512-3531 Fax:03-3222-2066
E-mail: