京都大学 大学院生命科学研究科の井上 丹 教授、次世代研究者育成センター(白眉プロジェクト)の齊藤 博英 特定准教授らの研究グループは、RNAとたんぱく質の特性を生かしたナノサイズ構造体(正三角形)の分子設計の手法の確立と構築に世界で初めて成功しました。
現在、DNAのような生体分子を使ったナノ構造体創製に関する研究が盛んに行なわれています。DNAは設計が容易で、化学的に安定した性質を持っているため、使いやすく多くの研究がなされてきました。しかし、DNAは構造上の柔軟性が低いため、構造変換が可能な、微細で動的な構造物を構築することが困難でした。
本研究グループは、RNAの柔軟でありながら設計が容易で微細な構造をデザインしやすい性質を利用して、RNAを骨格としたナノサイズ構造体の作成技術の開発を行ない、RNAに結合してRNAを60度に曲げるたんぱく質を用いることで、動的にナノサイズの三角形構造体を創製することに成功しました。また、三角形の各頂点に機能性たんぱく質を自在に結合する技術の開発にも成功しました。
本研究で開発されたナノ構造体作成技術は、ナノバイオテクノロジー分野にRNAとたんぱく質という新しい材料を提供するものであり、特定のたんぱく質の存在下でのみ三角形構造体の構造形成が起こるといった構造制御を可能にした技術です。生体内においても、複数の分子が自己集合することで複雑な構造体を形成し、多彩な機能を発現していますが、本技術の発展により、そのような機能性構造体の創出が可能になるものと期待されます。
また本技術は、細胞機能を制御する技術へも展開できます。三角形の頂点に、例えばがんを認識するたんぱく質とがん細胞を殺傷するたんぱく質などを結合させることで、選択的に特定の細胞のみをターゲットとし、無差別に他の細胞を殺傷しない新しいがん治療法の開発につながります。
さらにナノ構造体の構造が変わることにより、はじめて機能が発揮できる仕組みを作れば、例えばがん細胞に入った時のみ構造変換が起こり、がん細胞を殺傷するといった細胞内で機能する「ナノロボット」構築技術に発展することも期待されます。
本研究は、JST 戦略的創造研究推進事業 国際共同研究事業(ICORP)「RNAシンセティックバイオロジープロジェクト」(代表研究者:井上 丹)の一環として行われ、本研究成果は、2011年1月16日(英国時間)に英国科学雑誌「Nature Nanotechnology」のオンライン速報版で公開されます。
<研究背景と目的>
生体分子の中で、DNA、RNAおよびたんぱく質については、分子レベル、原子レベルでの研究が進んでいます。DNAの場合は、DNAのもつ単純な二重らせん構造を基本として分子デザインが行われており、DNAオリガミ注1)という高度に複雑な構造体などの大きなサイズの分子の構築が報告されています。しかしDNAは、あくまでも二重らせん構造を基本とする制約があり、構造体形成のための材料としての構造単位に限界があると考えられます。特に、生体内で作用する小さなサイズ(例えば通常の酵素以下の大きさ)で複雑な機能と構造を持つ分子の作成には適しません。また、生体内で酵素などの機能性分子として働くものはなく、機能的にも構造的にも自由度が少ないのが現状です。一方、RNAは二重らせん構造に加えて、さまざまな分子内および分子間相互作用が可能であるため、この性質を利用して生体内で多様な立体構造を形成し、酵素機能などの高度な機能を発揮することが知られています。また、たんぱく質はRNAよりはるかに多彩かつ複雑な立体構造と機能を有しますが、その複雑さのため、分子設計は非常に困難です。そこで、RNAは設計により作成し、たんぱく質は天然のものを利用するといった戦略で、設計の柔軟性が高くかつ複雑な立体構造や機能を持つ分子を設計するのが合理的と考えられます。しかし、これまでの国内外の研究においてRNAとたんぱく質の複合体(RNP)注2)を利用したナノ構造体の構築や、たんぱく質により構造を制御できる人工ナノ構造体の構築は達成されておらず、そのため複雑な構造や、微細な構造の作成技術の開発はほとんど進んでいませんでした。
<研究の内容>
本研究では、RNA分子上に複数の機能性たんぱく質の結合を可能にする、RNP分子デザイン技術を開発しました(図1)。特定のたんぱく質にだけ結合しやすいRNPモチーフ注3)が必須なため、リボソームたんぱく質L7Ae注4)と、それに特異的に相互作用するキンクターンRNA注5)を選択しました。このキンクターンRNAはL7Aeと結合する(図2の黄色の部分)と約60度の角度に折れ曲がります(図2の赤い部分)。この特徴的なRNPは、ナノサイズの構造体を作成するための新しいパーツとして有用である可能性があります。このRNPを利用して、人工のRNPから成るナノ正三角形(Triangle-RNP)を作成しました。具体的には、一辺が10-30nmというナノ(10億分の1)メートルサイズの三角形を構築するため、キンクターンRNAのモチーフを3ヵ所に持つ環状の二本鎖RNAを設計して、これにL7Aeを結合させる実験を行ないました(図3・左)。
その構造体形成を原子間力顕微鏡(AFM)により観察すると、3つのL7Ae-キンクターンRNAがそれぞれの頂点部分を形成する一辺が約17nmの三角形構造体が完成していました(図3・右)。たんぱく質の存在下でのみ、三角形様の構造体が観察されたことから、たんぱく質によりRNAの構造を人工的に制御する世界初の構造制御に成功したことが分かりました。また、辺にあたる部分のRNAの塩基数(長さ)を26bpから48bpに増やすことで一辺が23nmのよりサイズの大きな三角形をデザインし、同様にこのRNAとL7Aeを結合させたところ、予想通り大きな三角形が観察されました。 これらの結果は、RNPモチーフを切り貼りすることで、ナノ構造を容易に設計できることを示しています。
さらに、3つの頂点に目的の機能性たんぱく質を配置するため、L7Aeとの融合たんぱく質として、緑に光るEGFP蛍光たんぱく質を同様の方法で結合させ、AFMにより観察してみました。その結果、3つの機能性たんぱく質を頂点に持つ三角形が構築できていることが分かりました(図4)。 また、細胞内の環境に類似した生理条件下でも、この構造体は安定に保持できることが明らかになりました。
<今後の展望>
本研究の成果より、三角形の頂点それぞれに例えばがん細胞を認識する2種類のたんぱく質と細胞を殺傷する1つのたんぱく質を結合すれば、特定のがん細胞を間違いなく認識し、これにより検出されたがん細胞のみを殺傷するといった複数の機能を持つ有用な高機能RNP分子の創製が期待できます。また、ナノバイオテクノロジー分野にRNA-たんぱく質複合体が活用できることを初めて示すものであり、細胞内で目的の機能をもつ構造体を自在に作り出せるため、必要なときに必要な「分子機械」を構築する基盤技術としても期待されます。
細胞内のたんぱく質合成工場であるリボソーム注6)に代表される天然の超機能性分子は、複数のRNAとたんぱく質が自己集合することで複雑な構造体を形成し、高度な機能を発現しています。近年、生体分子を活用してナノサイズの構造体を作成する研究が注目されていますが、このような複数の分子から成る機能性ナノ構造体の作成は、これまで実現できておりませんでした。本技術の発展により、そのような機能性構造体の創出が可能になることが期待できます。さらに、機能や構造を環境に応答して変換できる、インテリジェントな人工分子を創出するには至っていませんでしたが、本研究の基盤技術である「RNP分子デザイン」は、より複雑な構成を持つナノサイズの構造体を作成できるとともに、さらにはその構造をも動的に制御できるインテリジェントな分子作成技術です。将来的には構造変換によりRNP分子機械の機能を制御できる可能性も十分にあると考えられ、リボソームに匹敵する、高度に複雑で洗練された機能性分子複合体やナノロボットを創出する可能性を秘めています。
本技術で創製した分子は、あらゆる生物に適用可能であるため、生物学研究や医療、検査などに用いる新しい機能性複合体分子の開発が可能になると考えられます。
<参考図>
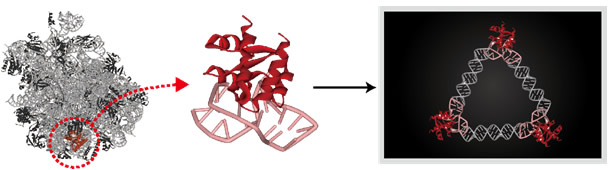
図1 RNPの分子デザイン
天然のRNPからパーツとなるたんぱく質とRNAを取り出し、それらを組み合わせて新たなナノサイズの構造体を作製する。
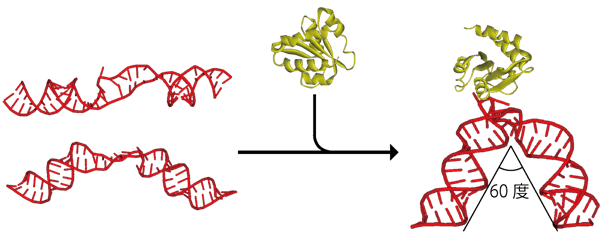
図2 使用したRNP
赤色で示したキンクターンRNAは単独では特定の構造を形成しない(左)。リボソームたんぱく質L7Ae(黄色)を加えると、このたんぱく質がキンクターンRNAに結合しRNAが60度に折り曲がる(右)。
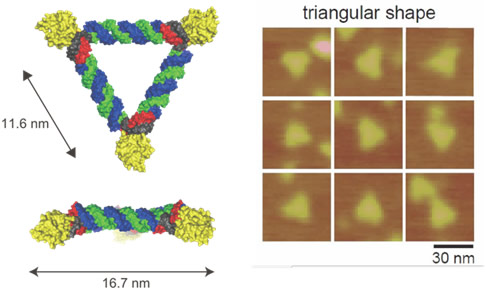
図3 RNPによるナノメートルサイズの三角形構造
黄色部分がL7Aeであり、このたんぱく質がRNAを60度に折り曲げている。二本鎖RNAは直線のため、全体としては正三角形の形状となる(左図)。作成したナノ三角形構造をAFMにより観察した写真(右図)。一つひとつの三角形がRNPによる形作られた構造体となっている。
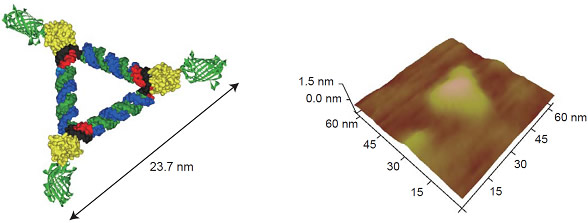
図4 3つの機能性たんぱく質を頂点に持つ三角形
L7Ae(黄色)にEGFP(緑色)を融合させ、三角形上に配置させた(左図)。AFMで観察すると、L7Aeの時(図3)よりも大きな三角形が見られた(右図)。
<用語解説>
- 注1) DNAオリガミ
- 2006年にカリフォルニア工科大学のPaul Rothemund博士により初めて報告された、約7000塩基の長い1つのDNAと、その構造を規定する数百本の短い留め金DNAを用いてナノ構造体を設計し、作成する技術のこと。DNAオリガミでこれまでに作成された構造体に対し、本研究成果で作成したナノ構造体は約10-30nmスケールと比較的小さい。
- 注2) RNAとたんぱく質の複合体(RNP)
- 細胞内に存在するRNAの多くは、単独で機能を発現することはなく、たんぱく質との複合体(RNA-protein complex;RNP)として、存在している。このように生体内で重要な役割を果たすRNPを人工的に設計し、構築する技術は、これまでに達成されていなかった。
- 注3) RNPモチーフ
- RNA-たんぱく質の相互作用の基盤となる、生物種又は分子を超えて保存された配列と構造を持つRNPの構成ユニットのこと。このRNP相互作用モチーフは、比較的単純で短い配列をもち、それ自身独立かつ安定な立体構造を形成できる場合が多い。
- 注4) L7Ae
- 古細菌リボソーム大サブユニットに存在するたんぱく質の1つであり、リボソーム構築に必須の因子であるとともに、RNA塩基の修飾や、RNAを基盤とする遺伝子発現システムであるリボスイッチへの結合など、複数の機能を担う。本研究で用いたキンクターンRNAと強固に結合し、RNAの構造変化を誘導する性質を持つ。
- 注5) キンクターンRNA
- リボソームRNA中で発見された、天然RNA-たんぱく質の構造形成に重要な役割を果たすRNAモチーフの1つ。L7Aeが結合することで、RNAの構造変化(キンク)が誘導され、60度に折れ曲がる。このRNPは、結合親和性と特異性が高く、安定な複合体を細胞内外で保持できる。
- 注6) リボソーム
- 全ての生物の細胞内に存在し、生存に必須の機能性超分子複合体である。mRNAの遺伝情報を読み取ってたんぱく質へと変換する機構である翻訳が行われる場である。大小2つのサブユニットからなり、これらは50種類以上のたんぱく質(リボソームたんぱく、ribosomal protein)と少なくとも3種のRNA(リボソームRNA、rRNA;ribosomal RNA)の複合体である。2000年、X線構造解析により立体構造が決定され、キンクターン RNAを含む、さまざまなRNPモチーフが見つかっている。
<論文名>
“Synthetic RNA-protein complex shaped like an equilateral triangle”
(人工RNA-たんぱく質複合体を基盤とした正三角形構造体の創出)
doi: 10.1038/nnano.2010.268
<お問い合わせ先>
<研究に関すること>
齊藤 博英(サイトウ ヒロヒデ)
京都大学 次世代研究者育成センター(白眉プロジェクト) 特定准教授
科学技術振興機構 戦略的創造研究推進事業 総括実施型研究(ICORP)
「RNAシンセティックバイオロジープロジェクト」 グループリーダー
〒606-8502 京都府京都市左京区北白川追分町
Tel:075-753-3997 Fax:075-753-3996
E-mail:
<JSTの事業に関すること>
小林 正(コバヤシ タダシ)
科学技術振興機構 イノベーション推進本部 研究プロジェクト推進部
〒102-0075 東京都千代田区三番町5 三番町ビル
Tel:03-3512-3528 Fax:03-3222-2068
E-mail: