JST 課題解決型基礎研究の一環として、東京農工大学 光ナノ科学融合研究リングの三沢 和彦 教授らは、超短パルスレーザー光の位相を自由に制御・測定する技術を活用し、生きたイカの神経細胞内に注入した麻酔ガスの分子を検出することに成功しました。
麻酔ガスは医療現場で頻繁に使われていますが、どうして麻酔が効くのかはいまだに解明されていません。麻酔ガスが生体内で神経信号伝達を抑制する作用に関心が持たれていますが、神経組織内で麻酔ガス分子そのものの存在位置を特定する観測手法がないため、麻酔の作用機構を直接的に解明する研究を行うことは困難です。
本研究グループは、「位相制御コヒーレントラマン顕微分光法」と呼ばれる手法を独自に開発し、分子固有の構造に由来する光散乱信号(ラマンスペクトル注1))を顕微鏡下で高感度かつ簡便に測定することを実現しました。さらに、この方法を用いて、巨大軸索と呼ばれるイカの神経突起内に注入した麻酔薬(セボフルラン)のラマンスペクトルを細胞質から分離して測定し、細胞中での麻酔ガス分子の位置を特定することができました。
今後、神経信号伝達現象と麻酔ガス分子の局在を同時に計測することで、長年の謎である麻酔薬の分子薬理メカニズム解明につながるものと期待されます。
本研究は、東京医科歯科大学の寺田 純雄 教授らと共同で行われました。
本研究成果は、米国科学雑誌「The Journal of Chemical Physics」のオンライン速報版で近日中に公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域 |
: |
「新機能創成に向けた光・光量子科学技術」
(研究総括:伊澤 達夫 東京工業大学 理事・副学長(研究担当))
|
| 研究課題名 |
: |
「時空間モルフォロジーの制御による能動メゾ光学」 |
| 研究代表者 |
: |
五神 真(東京大学 光量子科学研究センター 教授) |
| 共同研究者 |
: |
三沢 和彦(東京農工大学 光ナノ科学融合研究リング/工学研究院 教授 ) |
| 研究期間 |
: |
平成18年10月~平成24年3月 |
JSTはこの領域で、光の発生、検知、制御および利用に関する革新的な技術の創出を目指しています。上記研究課題では、フォトニック結晶を用いて究極的な光の発生技術の開発を行い、超高効発光デバイスや大面積レーザーの創出、次世代量子通信・情報のための基礎を築くことを目指しています。
<研究の背景と経緯>
セボフルランをはじめとする、医療現場で常用されるガス麻酔は、経験則によって使用されています。なぜガス麻酔により神経信号の伝達機能が抑制され、再び回復することができるのか、その分子レベルでの機構はいまだ解明されていません。
麻酔の分子機構解明には、ガス麻酔下の神経組織で麻酔ガスの分子が機能を発揮する際に、麻酔ガスの分子が細胞のどこに局在するかを知ることが不可欠です。
しかし、麻酔ガスの分子の多くは原子が十数個程度の小分子なので、その局在を見えるようにするために螢光色素などのより大きな分子を標識として付けることは困難です。そのため、螢光標識などを付けずに、特定の分子が顕微鏡の視野内でどこに局在するかを検出する方法の実現が望まれています。
<研究の内容>
本研究では、分子固有の分子振動スペクトル(ラマンスペクトル)を測定し、そのスペクトル形状を分子の標識としました。この分子振動スペクトルを測定する新たな手法として、スペクトル位相を操作したパルスレーザー光を用いる「位相制御コヒーレントラマン顕微分光法」を開発しました。
コヒーレントラマン散乱は、まず、周波数の異なる2本のレーザー光を分子に同時に照射し、2本のうなりの周波数(それぞれのレーザー光の周波数の差に相当)を分子の持つ固有な振動の周波数に合わせることで、分子を強制的に振動させます。その強制的に振動を引き起こされた分子に、3本目のレーザー光を照射すると、入射した光の周波数と分子振動の周波数との和の周波数を持つ新しい光が放出されます。この信号光の周波数から、分子固有の振動周波数を知ることができます。
従来のコヒーレントラマン分光法では、これらの複数のレーザービームを別々に用意しています。しかし、顕微鏡下では、それら複数のビームを1点に正確に合わせる必要があるなど、レーザー分光学の専門家以外が測定するのは容易ではありません。
それに対して、本研究では、広いスペクトル帯域を持つ単一の超短パルスレーザー光を用いています。上で述べた3本の光の役割を担う各々の周波数成分を区別するために、回折格子と液晶空間光変調器からなる位相制御装置(図1)を用いて、パルス光に含まれる周波数成分の位相を個別に調整する方法を用いました。この方法では、1台のレーザー装置から出る単一のレーザービームを顕微鏡に導入するだけで済むため、生命科学や医療分野へ活用するのが容易になった点において革新的といえます。
麻酔ガスの多くは、生体に多量には存在しないハロゲン元素を含む化合物です。そこで、本方法を用いて、ハロゲン元素に関連した固有の分子振動を観測し、生体組織由来の分子振動と区別することを試みました。代表的な吸入麻酔薬であるセボフルランとイソフルランについて、純粋液体の状態でラマンスペクトルを測定した結果、分子の種類を同定できるスペクトルパターンを得ることができました(図2)。また、巨大軸索と呼ばれるイカの神経突起内にセボフルランの液滴を注入して観察・分析したところ、細胞中の麻酔ガス分子の位置を特定することができました(図3)。
<今後の展開>
今回の結果をもとに装置の開発を進めれば、セボフルランの生体組織における局在を可視化、画像化できます。今後、神経信号伝達現象と麻酔ガス分子の局在を同時に計測することで、長年の謎である麻酔薬の分子薬理メカニズムを解明することへの第1歩になると期待されます。
本方法は、吸入麻酔薬分子以外の分子についても、生体内でその分布を画像化することを可能にします。測定対象を選ぶことにより、生命科学や医療の分野で限りない応用が広がるものと考えられます。
<参考図>

図1 スペクトル位相制御装置の全景
回折格子により、光パルスに含まれる周波数成分に分け、液晶空間光変調器により、それぞれの周波数成分に最適な位相ずれを与える。相対的に位相ずれが与えられた全周波数成分を再び合成して、1本のレーザービームとして出力する。
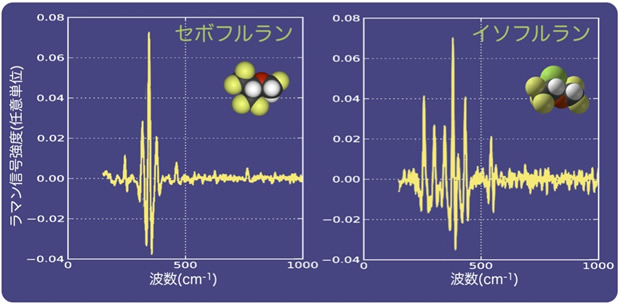
図2 吸入麻酔薬セボフルラン(左)とイソフルラン(右)のラマンスペクトル
それぞれの分子構造を挿入図で示した。1つのスペクトルに見られる複数の信号ピークの組み合わせパターンを、その分子の識別指標として用いる。
グラフの横軸は、照射した光のうなりの周波数を波数単位(cm-1)で表したものであり、縦軸は、試料から発せられたラマン信号の強度を表します。いくつかの特定の周波数で鋭いピークが見られるのは、これらの周波数を持つ分子の振動が強く引き起こされていることに対応します。
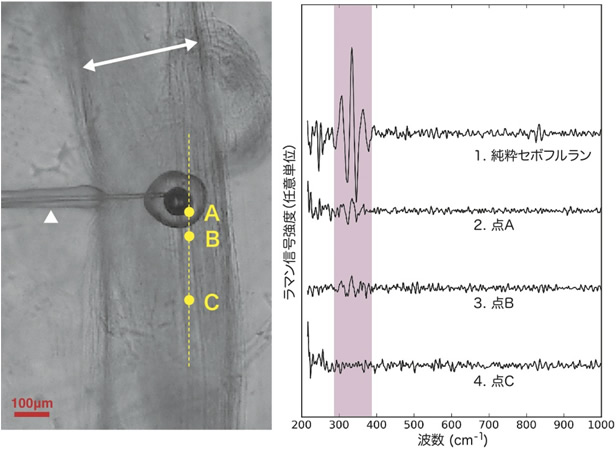
図3 イカの巨大軸索中に注入されたセボフルラン液滴の顕微鏡写真とラマンスペクトル
左: イカの巨大軸索中に注入されたセボフルラン液滴の顕微鏡写真。中央に黒く見える球状の部分が、注射器(△)によって軸索内に注入されたセボフルラン液滴。両矢印(⇔)は軸索の太さ方向である。点Aは液滴の中心付近、点Bは液滴の外周部、点Cは液滴から離れた位置。セボフルラン分子は、注入直後から細胞内部で急速に拡散していく。ただし、この顕微鏡写真だけでは、濃淡から形状が分かるだけで、そこに含まれる物質の組成は分からない。
右: 純粋セボフルランのラマンスペクトルおよび、顕微鏡写真中のA、B、C各点におけるラマンスペクトル。純粋セボフルランで網掛けの領域に現れるスペクトルパターンを指標とした。点Aと点Bではセボフルランに特徴的なパターンが見られることから、液滴の中心付近とにじみ出た外周部分にセボフルラン分子が存在することが確かめられた。一方、液滴中心から遠い点Cには、セボフルラン分子は検出限界以下であることも分かる。
<用語解説>
- 注1) ラマンスペクトル
- 多くの物質は、分子振動や格子振動といった、その物質に固有な原子核間の振動運動を示します。その物質に周波数ωの光を入射した場合に、物質の持つ振動運動の周波数Ωとの和(ω’=ω+Ω)あるいは差の周波数(ω’’=ω-Ω)を持つ新しい光(ラマン散乱光)が放出されることがあります。そのラマン散乱光の強度を周波数の関数としてグラフにしたものをラマンスペクトルと呼びます。グラフの横軸には、ラマン散乱光の周波数から入射した光の周波数を差し引いた値(ラマンシフト)を用います。このとき、縦軸の強度が大きいところの横軸の値を読み取れば、それらが物質固有の振動周波数に対応します。
<論文名および著者名>
“In-vivo molecular labeling of halogenated volatile anesthetics via intrinsic molecular vibrations using nonlinear Raman spectroscopy”
(非線形ラマン分光法を用いた、分子固有の振動による、ハロゲン化吸入麻酔薬の生体内分子標識)
Yu Nagashima, Takayuki Suzuki, Sumio Terada, Shoji Tsuji, and Kazuhiko Misawa*
(*責任著者)
doi: 10.1063/1.3526489
<お問い合わせ先>
<研究に関すること>
三沢 和彦(ミサワ カズヒコ)
東京農工大学 光ナノ科学融合研究リング/工学研究院 教授
〒184-8588 東京都小金井市中町2-24-16
Tel:042-388-7485 Fax:042-388-7485
E-mail:
寺田 純雄(テラダ スミオ)
東京医科歯科大学 大学院医歯学総合研究科/脳統合機能研究センター 教授
〒113-8519 東京都文京区湯島1-5-45
Tel:03-5803-5149 Fax:03-5803-5151
E-mail:
<JSTの事業に関すること>
長田 直樹(ナガタ ナオキ)
科学技術振興機構 イノベーション推進本部 研究領域総合運営部
〒102-0075 東京都千代田区三番町5 三番町ビル
Tel:03-3512-3524 Fax:03-3222-2064
E-mail: