JST 課題解決型基礎研究の一環として、東京医科歯科大学 難治疾患研究所の岡澤 均 教授らは、神経細胞保護的グリア細胞である「バーグマングリア注1)」の増殖に関与する新規分子「MAXER(マクセル)」を発見し、MAXERの減少が、小脳の主要な出力ニューロンであるプルキンエ細胞を保護する役割のバーグマングリアを介して、神経変性病態に関わる分子メカニズムを明らかにしました。
近年、神経細胞の変性にグリア細胞が関わることが注目されていますが、その詳細な分子メカニズムについて明らかになっていませんでした。
本研究グループは今回、脊髄小脳失調症注2)1型(SCA1)の小脳細胞で発現変化を示す分子の網羅的検索から、小脳細胞においてのみ遺伝子発現が低下し、ハンチントン病などの別の変性疾患では発現が変化しない新規分子MAXERを発見しました。解析の結果、MAXERは進化的に保存されている小胞体注3)膜分子であること、またMAXERが減少すると細胞周期がG1期に停滞すること、さらにMAXERが細胞質・核の間を行き来するサイクリンD1の抑制因子であるCDK5RAP3の局在制御を行い、これによって細胞周期を制御することが明らかになりました。同時に、SCA1におけるMAXERの減少がバーグマングリアの減少を招き、結果として神経細胞に対してグルタミン酸毒性が増加して神経細胞変性に関わることを示しました。
この成果は今後、バーグマングリア再活性化を介した神経変性疾患の治療開発につながるものと期待されます。
本研究は、東京医科歯科大学 大学院生(当時)の塩飽 裕紀 氏と共同で行われ、米国・ベイラー医科大学のゾービィ教授の協力を得ました。
本研究成果は、2010年6月8日(英国時間)に欧州分子生物学機構(EMBL)の科学誌「EMBO JOURNAL」のオンライン速報版で公開されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
戦略的創造研究推進事業 チーム型研究(CREST)
| 研究領域 |
: |
「精神・神経疾患の分子病態理解に基づく診断・治療へ向けた新技術の創出」
(研究総括:樋口輝彦 独立行政法人 国立精神・神経医療研究センター 理事長)
|
| 研究課題名 |
: |
「ポリグルタミン病の包括的治療法の開発」 |
| 研究代表者 |
: |
貫名 信行(独立行政法人 理化学研究所 チームリーダー) |
| 共同研究者 |
: |
岡澤 均(東京医科歯科大学 難治疾患研究所 教授) |
| 研究期間 |
: |
平成21年10月~平成27年3月 |
JSTはこの領域で、少子化・高齢化・ストレス社会を迎えた日本において社会的要請の強い認知・情動などをはじめとする高次脳機能の障害による精神・神経疾患に対して、脳科学の基礎的な知見を活用し、予防・診断・治療法などで新技術の創出を目標にしています。
上記研究課題では、本質的な治療法のない遺伝性神経変性疾患のポリグルタミン病について、異常たんぱく質凝集の抑制・分解過程の制御、転写異常などの病態過程の制御の観点からの治療法の開発を目指します。
<研究の背景と経緯>
脊髄小脳失調症は、アルツハイマー病、パーキンソン病に次いで患者数の多い神経変性疾患ですが、有効な治療法は確立されておらず、その病態解明と治療開発は喫緊の社会的問題です。
今回の研究の対象であるSCA1は、原因遺伝子の一部(ataxin-1遺伝子エキソン)のCAGリピート配列の異常伸長注4)によって生じることが明らかになっていました。グルタミンというアミノ酸をコードする3つの塩基配列(C=シトシン、A=アデニン、G=グアニン)が異常に伸長することから、他の複数の遺伝性脊髄小脳失調症(SCA2、SCA3、SCA6、SCA7、SCA17)、ハンチントン病、球脊髄性筋萎縮症などとともに、ポリグルタミン病注5)と呼ばれ、共通の病態を持つと考えられています。
一方、別の変性疾患グループである筋萎縮性側索硬化症(ALS)の病態においては近年、グリア細胞の関与が疑われており、グリア細胞の一種であるアストログリアが何らかの毒性物質を放出して神経細胞を障害することが想定されています。また、SCA7においてバーグマングリア細胞が神経変性に関与するという成果も報告されました。しかしながら、グリア細胞を介する神経変性病態である非自律的病態注6)が神経変性疾患の全てに共通するものかどうかは、大きな問題となっています。
また、具体的にどのような分子が如何なるメカニズムで神経細胞変性を担っているのかについては明らかではありませんでした。SCA7におけるバーグマングリア細胞による変性病態を制御する分子は分かっておらず、ALSにおいてもアストログリアとニューロン変性をつなぐ分子は今のところ確定されていません。そのため、グリア細胞を介した神経変性に直接関与する分子の同定が期待されています。
<研究の内容>
東京医科歯科大学の岡澤教授らはこれまで、脊髄小脳失調症1型原因たんぱく質(ataxin-1)とハンチントン病原因たんぱく質(huntingtin)の正常型並びに異常型を発現する3種類の初代培養ニューロン注7)(それぞれ大脳皮質、線条体、小脳由来。小脳ニューロン培養にはバーグマングリアも混入する)の網羅的発現解析を行ってきました。その際に、正常型発現に対して異常型発現で遺伝子発現に変化のある遺伝子を検討しました(Tagawa et al., The Journal of Neuroscience 2007)。都合6種類の組み合せのトランスクリプトームデータ注8)の比較から、異常型ataxin-1を発現した小脳ニューロン(含むバーグマングリア)においてのみ減少し、他の5種類の組み合せでは変動しない新規遺伝子をすでに発見していましたが、その発現・機能については未解決でした。
今回の研究では、上記の経緯から偶然発見し「MAXER」と命名した新規分子が、小脳バーグマングリアに多く発現していることを発見しました(図1)。これが発端となり、バーグマングリア増殖を制御する分子機構、さらにはSCA1病態との分子的関係が明らかになりました。具体的には、MAXERをEGFPという蛍光たんぱく質で光らせて観察しました。するとMAXERは小胞体特異的マーカーであるER-DsREDと細胞内の同じ場所に存在しており、さらに細胞内の小器官を遠心分離して大きさによって分離することによって、MAXERと小胞体は同じ区画に存在していることが明らかになりました(図2)。このことから、MAXERは小胞体に存在しているたんぱく質であることが分かりました。
また、同時にSCA1病態ではバーグマングリアが減少していることも確認しました(図3)。そして、MAXERの働きをRNAi法という手法を用いて抑制したところ細胞増殖が抑えられ、MAXERと相互作用するCDK5RAP3というたんぱく質の働きを抑えると細胞増殖が促進されました。つまり、MAXERは細胞増殖に関連するたんぱく質であり、CDK5RAP3の働きを抑えることで、バーグマングリア増殖を促進していたのです(図5)。このことから、小脳でMAXERが減少するとバーグマングリアが増殖できなくなり、プルキンエ細胞が保護されなくなることから、神経変性を発症するというメカニズムが解明されました。
MAXERは、バーグマングリア増殖に特異的に関与する分子として、そしてグリア細胞からニューロン変性への過程(非自律的病態)を担う分子として、世界で初めて発見された分子です。また、SCA1において非自律的病態が示されたのも世界で初めてのことです。
本研究は、東京医科歯科大学 大学院生(当時)の塩飽 裕紀 氏(現在、医学部 学生)と共同で行われ、米国・ベイラー医科大学のゾービィ教授からノックインマウス提供などの協力を得ました。
<今後の展開>
今回の研究成果で、バーグマングリアの小脳変性における重要性が示されました。バーグマングリアはニューロンとは異なって細胞増殖能を生後も保っており、一種の幹細胞であるという説も提唱されています。ここから、バーグマングリア細胞増殖を活性化することは可能と考えられます。
本研究成果から、バーグマングリアの数を増やす、あるいは個々のバーグマングリアの機能を向上させることを通じて脊髄小脳失調症にアプローチする新しい治療戦略が示されました。
<参考図>
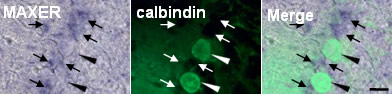
図1 MAXERはバーグマングリアに発現している
Calbindinで緑色に染色されるプルキンエ細胞(真ん中の図中、白い矢頭)の傍らに存在するバーグマングリア(白い矢印)にMAXERのin situ hybridization(左側の図)のシグナル(青色で染色、黒い矢印)が認められる。
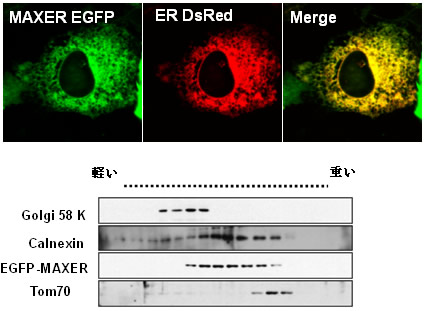
図2 MAXERは、小胞体たんぱくである
MAXER(上図、緑色)は小胞体のマーカーであるER-DsRED(上図、赤色)と細胞中の同じ場所に存在しており(上図、緑色と赤色が重なり合うと黄色で表示される)、ショ糖勾配による遠心分離でも小胞体マーカーたんぱく質Calnexinと同じ分画に分離される(下図、CalnexinとMAXERは同じ場所にバンドが現れる)。
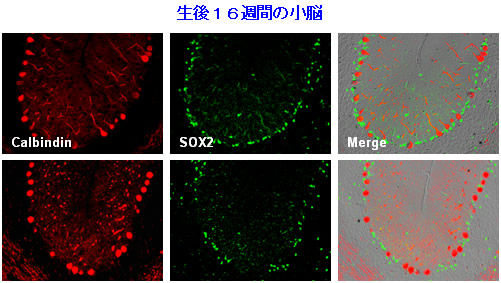
図3 SCA1モデルマウスでは、バーグマングリアはプルキンエ細胞に先行して減少する
変異ataxin-1ノックインマウスの小脳の染色を示す。Calbindin(図中の赤色)に染まるプルキンエ細胞の減少が目立たない段階(生後16週)で、すでにSOX2(図中の緑色)に染まるバーグマングリアは明瞭に減少している。
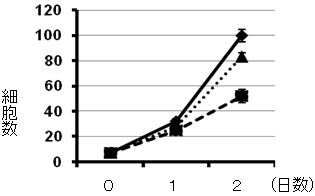
図4 細胞増殖(実線)に対するMAXERの影響
MAXERのRNAiによるノックダウンは細胞増殖を抑制し(太点線)、さらに加えてCDK5RAP3をノックダウンすると抑制が解除される(細点線)。
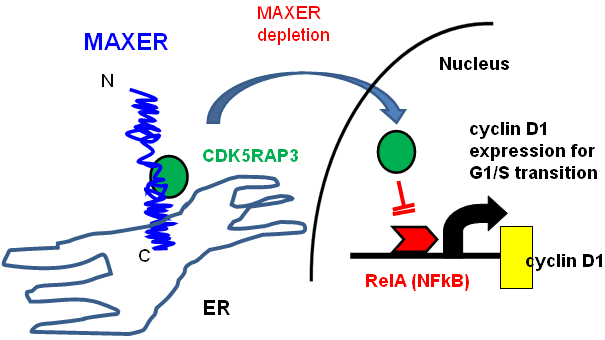
図5 MAXERが細胞周期に果たす役割
MAXER(青色で図示)は細胞周期を機能させるためのcyclin D1(黄色で図示)の転写に対して抑制的に働く転写補助因子CDK5RAP3(緑色で図示)を細胞質につなぎ止めている。MAXERが消失するとCDK5RAP3が核に移行し、cyclin D1を転写するためのRelA(NFκB)(赤色で図示)の働きを抑えるために、cyclin D1が減少し、細胞周期のG1/S移行が停滞する。
<用語解説>
- 注1) バーグマングリア
- 小脳の主要な出力系であるプルキンエ細胞の近傍に存在して、自身に発現するAMPA型グルタミン酸受容体によって、シナプス間隙にトランスミッターとして放出されたグルタミン酸を再吸収する。バーグマングリア機能に問題があるとシナプス間隙でのグルタミン酸濃度が上昇し、神経細胞に障害を与える。バーグマングリアは神経幹細胞特異的なたんぱく質(SOX2など)を発現しており、幹細胞として機能するのではという説もあるが、発生・再生の上での機能は未解明な部分が多い。
- 注2) 脊髄小脳失調症
- 小脳神経細胞(プルキンエ細胞、歯状核など)の変性を中心として、時に大脳基底核、網膜神経細胞、末梢神経などの変性を合併する一群の脳疾患。常染色体優性、常染色体劣性などの形式をとる遺伝性脊髄小脳失調症と、家族歴のはっきりしない弧発例がある。
- 注3) 小胞体
- 細胞の小器官の1つであり、表面にリボソームを持つ粗面小胞体とリボソームのない滑面小胞体がある。粗面小胞体ではリボソームでmRNAから翻訳されたたんぱく質が小胞体の内腔に取り込まれ、たんぱく質のフォールディングや切断、ジスルフィド結合、糖鎖付加などが行われる。さらにたんぱく質が異常な高次構造(コンフォメーション)を取った場合、コンフォメーションの修正が小胞体で行われる。コンフォメーション処理に失敗したたんぱく質はユビキチン・プロテアソーム系に運ばれ分解される。
- 注4) リピート配列の異常伸長
- SCA1を含むポリグルタミン病は、遺伝子エキソン内部のCAGリピート配列の繰り返し数が通常20-30未満であるところが40以上に増加すること(異常伸長)によって起こる。リピート配列はDNAの複製・組み換えなどにおいて不安定なことから、配偶子特に精子発生の段階で何らかの原因で異常伸長が生じるとされている。
- 注5) ポリグルタミン病
- 遺伝性脊髄小脳失調症の中で、原因遺伝子エキソン内のCAGリピート伸長が原因となって発症するグループを指す。エキソンのCAGはグルタミンに翻訳されるため原因たんぱくではポリグルタミン鎖の伸長につながる。SCA1、SCA2、SCA3、SCA6SCA7、SCA17、DRPLAはポリグルタミン病に属する。異常伸長したポリグルタミン鎖は2次構造としてβシートを取りやすく、これが基盤となってたんぱく凝集を起こしやすくなると言われている。
- 注6) 非自律的病態
- non-cell autonomous pathologyの和訳。神経細胞自体の異常に基づいて神経細胞の機能障害や細胞死が生じる自律的病態(cell autonomous pathology)に対して、神経細胞以外の細胞の異常によって神経細胞が機能障害や細胞死を起こすことを言う。多くはグリア細胞によるものである。変性疾患原因たんぱくがアストログリアに発現するために毒性因子がグリアから放出されて神経細胞を障害する場合、バーグマングリアのような保護的なグリアが変調を来すために起こる場合などが想定されている。
- 注7) 初代培養ニューロン
- ラットなどの動物個体から脳を取り出し、トリプシン処理で細胞ごとにバラバラにした後に、特定の血清、栄養因子などを加えた培地で細胞培養することが可能である。このようにして得た初代培養ニューロンは神経科学においてさまざまな実験に用いられている。
- 注8) トランスクリプトームデータ
- ヒト、マウス、ラットなどの全ての遺伝子に対応した合成DNAを小さなチップの上に固定化したジーンチップを用いて、全遺伝子の発現を網羅的に調べることが可能である。このようにして得た全遺伝子発現データをトランスクリプトームデータと呼ぶ。
<論文名>
“Suppression of the novel ER protein MAXER by mutant ataxin-1 in Bergman glia contributes to non-cell autonomous toxicity”
(新規小胞体たんぱくMAXERが変異ataxin-1によってバーグマングリアの中で抑制されることが非細胞自律的なニューロン変性につながる)
doi: 10.1038/emboj.2010.116
<お問い合わせ先>
<研究に関すること>
岡澤 均(オカザワ ヒトシ)
東京医科歯科大学 難治疾患研究所 神経病理学分野 教授
〒113-8510 東京都文京区湯島1-5-45
Tel:03-5803-5847 Fax:03-5803-5847
E-mail:
<JSTの事業に関すること>
長田 直樹(ナガタ ナオキ)
科学技術振興機構 イノベーション推進本部 研究領域総合運営部
〒102-0075 東京都千代田区三番町5 三番町ビル
Tel:03-3512-3524 Fax:03-3222-2064
E-mail: